محلول مائي
المحلول المائي هو عبارة عن محلول يكون فيه المذيب هو الماء،[1][2] ويشار إليه عادة في المعادلات الكيميائية بإضافة (aq) إلى المعادلة ذات الصلة. تعني كلمة «مائي»، متعلقاً بالماء أو شبيهاً به أو ذائباً فيه. بما أن الماء يعدّ مذيباً ممتازاً ومتوفراً أيضاً بطبيعة الحال، فإنه مذيب سائد في الكيمياء، والمحلول المائي خليط متجانس نحصل عليه بإذابة جسم (صلب-سائل-غاز) في ماء خالص.
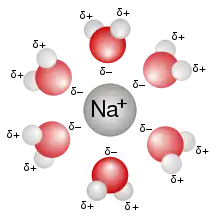
المواد التي تعدّ كارهة للماء «غير مائية» غالباً لا تذوب جيداً في الماء في حين أن المواد التي تعدّ محبة للماء «مائية» تذوب بشكل جيد فيه. ومثال على المواد المحبة للماء هو كلوريد الصوديوم (ملح الطعام العادي). تعدّ الأحماض والقواعد محاليل مائية، كجزء من تعاريف أرهينيوس الخاصة بهم.
تتحدد قدرة مادة ما على الذوبان في الماء بواسطة ما إذا كانت هذه المادة تستطيع أن تعادل أو تفوق قوى التجاذب القوية التي تولدها جزيئات الماء بين بعضها البعض. وإذا افتقدت المادة القدرة على الذوبان في الماء، فإن جزيئاتها تكون راسب.
المحاليل المائية التي توصل التيار الكهربائي بكفاءة تحتوي على إلكتروليتات «منحلات بالكهرباء» قوية، في حين أن تلك التي توصل التيار بضعف تحتوي على إلكتروليتات ضعيفة.مثال على ذلك حمض الخليك CH3COOH تلك الشوارد أو الإلكتروليتات القوية هي مواد تتأين بشكل كامل في الماء، بينما الشوارد أو الإلكتروليتات الضعيفة تظهر فقط درجة ضئيلة من التأين في الماء.
اللاإلكتروليتات هي عبارة عن مواد تذوب في الماء ولكنها تحافظ على سلامتها الجزيئية (أي لا تتفكك إلى أيونات). وتشتمل الأمثلة على السكر واليوريا والجليسرول وميثيل سلفونيل ميثان (MSM).
عند تنفيذ العمليات الحسابية المتعلقة بتفاعل واحد أو أكثر من المحاليل المائية، يجب معرفة عامة تركيز أو مولارية المحاليل المائية. ويعطى تركيز المحلول من حيث شكل المذاب قبل إذابته.
المراجع
- "معلومات عن محلول مائي على موقع jstor.org"، jstor.org، مؤرشف من الأصل في 28 يناير 2020.
- "معلومات عن محلول مائي على موقع zthiztegia.elhuyar.eus"، zthiztegia.elhuyar.eus، مؤرشف من الأصل في 17 يوليو 2019.
- بوابة الكيمياء