تصوير بالتجميد الإلكتروني
التصوير بالتجميد الإلكتروني (بالإنجليزية: Electron cryotomography أو CryoET) هي تقنية تصوير مستخدمة لإنتاج مناظر ثلاثية الأبعاد عالية الدقة (~ 1-4 نانومتر) للعينات، وعادةً ما تكون الجزيئات الضخمة البيولوجية والخلايا البيولوجية.[1][2]
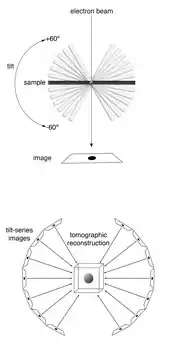
التصوير بالتجميد الإلكتروني (CryoET) هو تطبيق متخصص للتنظير المجهري الإلكتروني النافذ (CryoTEM) حيث يتم تصوير العينات أثناء إمالتها، مما ينتج عنه سلسلة من الصور ثنائية الأبعاد التي يمكن دمجها لإنتاج إعادة بناء ثلاثية الأبعاد، مشابه للفحص بالأشعة المقطعية لجسم الإنسان. وعكس تقنيات التصوير المقطعي الإلكتروني الأخرى، يتم تجميد العينات في الجليد غير البلوري («الزجاجي») والتصوير في ظروف التبريد العميق (<150 درجة مئوية)، مما يسمح بتصويرها دون الجفاف أو التثبيت الكيميائي، مما قد يؤدي إلى تعطيل أو تشويه الهياكل البيولوجية.[3][4]
وصف التقنية
في المجهر الإلكتروني (EM)، يتم تصوير العينات في فراغ عالي جدًا. مثل هذا الفراغ غير متوافق مع العينات البيولوجية مثل الخلايا؛ سيغلي الماء، وسيؤدي الاختلاف في الضغط إلى انفجار الخلية. في تقنيات المجهر الإلكتروني (EM) لدرجة حرارة الغرفة، يتم تحضير العينات بالتثبيت والجفاف. وهناك طريقة أخرى لتثبيت العينات البيولوجية، وهي تجميدها (الفحص المجهري الإلكتروني فائق البرودة). كما هو الحال في تقنيات الفحص المجهري الإلكتروني الأخرى، يتم تحضير عينات التصوير بالتجميد الإلكتروني (CryoET) (عادةً الخلايا الصغيرة (مثل البكتيريا أو العتائق أو الفيروسات) في وسط مائي قياسي وتطبيقها على شبكة المجهر الإلكتروني (EM). ثم يتم غمر الشبكة في مبرد (عادةً الإيثان) بكفاءة عالية لأن جزيئات الماء ليس لديها الوقت لإعادة ترتيبها في شبكة بلورية.[3] تسمى حالة الماء الناتجة «الجليد الزجاجي» وتحافظ على الهياكل الخلوية الأصلية، مثل الأغشية الدهنية، التي عادةً ما يتم تدميرها عن طريق التجميد. يتم تخزين العينات المجمدة الغاطسة لاحقًا وتصويرها في درجات حرارة النيتروجين السائل بحيث لا يسخن الماء بما يكفي لتتبلور.
يتم تصوير العينات في المجهر الإلكتروني النافذ (TEM). كما هو الحال في تقنيات التصوير المقطعي الإلكتروني الأخرى، يتم إمالة العينة إلى زوايا مختلفة بالنسبة لشعاع الإلكترون (عادةً كل درجة أو درجتين من حوالي -60 درجة إلى +60 درجة)، ويتم الحصول على صورة في كل زاوية.[5] يمكن بعد ذلك إعادة بناء سلسلة الصور هذه حسابيًا في عرض ثلاثي الأبعاد لموضوع الاهتمام.[6] وهذا ما يسمى بالتصوير المقطعي، أو إعادة البناء بالتصوير المقطعي.
تطبيقات
في المجهر الإلكتروني النافذ (TEM)، نظرًا لأن الإلكترونات تتفاعل بقوة مع المادة، فإن الدقة محدودة بسمك العينة. أيضًا، يزداد سمك العينة مع إمالة العينة، ويمكن للعينات الأكثر سمكًا أن تحجب شعاع الإلكترون تمامًا، مما يجعل الصورة مظلمة أو سوداء تمامًا. لذلك، بالنسبة للتصوير بالتجميد الإلكتروني (CryoET)، يجب أن تكون العينات أقل من 500 نانومتر تقريبًا لتحقيق دقة «جزيئية كبيرة» (4 نانومتر تقريبًا). لهذا السبب، ركزت معظم دراسات العلاج بالصدمات الكهربائية على المجمعات الجزيئية الكبيرة المنقاة، أو الفيروسات، أو الخلايا الصغيرة مثل تلك الموجودة في العديد من أنواع البكتيريا والعتائق.[1]
يمكن تحضير الخلايا الأكبر، وحتى الأنسجة، من أجل التصوير بالتجميد الإلكتروني (CryoET) عن طريق التخفيف، إما عن طريق التقسيم بالتبريد أو عن طريق طحن الحزمة الأيونية المركزة (FIB). في عملية التقطيع بالتبريد، يتم تقسيم الكتل المجمدة من الخلايا أو الأنسجة إلى عينات رفيعة باستخدام مشراح التجميد.[7] في الطحن بالحزمة الأيونية المركزة، تتعرض العينات المجمدة الغاطسة لحزمة مركزة من الأيونات، عادةً الغاليوم (Gallium)، والتي تقلل بدقة المواد من أعلى وأسفل العينة، تاركة صفيحة رقيقة مناسبة للتصوير بالصدمات الكهربائية..[8]
يؤدي التفاعل القوي للإلكترونات مع المادة أيضًا إلى تأثير دقة متباين الخواص. عندما تميل العينة أثناء التصوير، تتفاعل الأشعة الإلكترونية مع مساحة مقطع عرضي أكبر نسبيًا بزوايا ميل أعلى. في الممارسة العملية، زوايا الميل الأكبر من حوالي 60-70 درجة لا تسفر عن الكثير من المعلومات وبالتالي لا يتم استخدامها. ينتج عن هذا «إسفين مفقود» من المعلومات في الرسم البياني النهائي يقلل الدقة الموازية لشعاع الإلكترون.[6]

بالنسبة للهياكل الموجودة في نسخ متعددة في صورة مقطعية واحدة أو متعددة، يمكن الحصول على دقة أعلى (حتى ≤1 نانومتر) عن طريق متوسط الرسم البياني الفرعي. مشابه لتحليل الجسيم الفردي، ويجمع الرسم البياني الفرعي المتوسط الحسابي صورًا لأجسام متطابقة لزيادة نسبة الإشارة إلى الضوضاء.[9][10]
تتمثل إحدى العوائق الرئيسية في التصوير بالتجميد الإلكتروني (CryoET) في تحديد الهياكل ذات الأهمية داخل البيئات الخلوية المعقدة. يتمثل أحد الحلول في تطبيق الفحص المجهري للضوء الفلوري المترابط،[11] وحتى الفحص المجهري الضوئي فائق الدقة (مثل cryo-PALM[12]) والتصوير بالتجميد الإلكتروني (CryoET). في هذه التقنيات، يتم تجميد عينة تحتوي على بروتين ذي علامات فلورية ذات أهمية ويتم تصويرها أولاً في مجهر ضوئي مجهز بمرحلة خاصة للسماح بالاحتفاظ بالعينة عند درجات حرارة تبلور فرعية (<150 درجة مئوية). يتم تحديد موقع إشارة الفلورسنت ونقل العينة إلى المجهر الإلكتروني النافذ (CryoTEM)، حيث يتم بعد ذلك تصوير نفس الموقع بدقة عالية بواسطة التصوير بالتجميد الإلكتروني (CryoET).
مراجع
- Gan, Lu؛ Jensen, Grant J. (01 فبراير 2012)، "Electron tomography of cells" (PDF)، Quarterly Reviews of Biophysics، 45 (1): 27–56، doi:10.1017/S0033583511000102، ISSN 1469-8994، PMID 22082691، مؤرشف من الأصل (PDF) في 2 ديسمبر 2017.
- Dodonova, Svetlana O؛ Aderhold, Patrick؛ Kopp, Juergen؛ Ganeva, Iva؛ Röhling, Simone؛ Hagen, Wim J H؛ Sinning, Irmgard؛ Wieland, Felix؛ Briggs, John A G (16 يونيو 2017)، "9Å structure of the COPI coat reveals that the Arf1 GTPase occupies two contrasting molecular environments"، eLife (باللغة الإنجليزية)، 6، doi:10.7554/eLife.26691، ISSN 2050-084X، PMC 5482573، PMID 28621666.
- Dubochet, J.؛ Adrian, M.؛ Chang, J. J.؛ Homo, J. C.؛ Lepault, J.؛ McDowall, A. W.؛ Schultz, P. (01 مايو 1988)، "Cryo-electron microscopy of vitrified specimens" (PDF)، Quarterly Reviews of Biophysics، 21 (2): 129–228، doi:10.1017/s0033583500004297، ISSN 0033-5835، PMID 3043536، مؤرشف من الأصل (PDF) في 27 نوفمبر 2020.
- Oikonomou, CM؛ Jensen, GJ؛ Chang, YW (أبريل 2016)، "A new view into prokaryotic cell biology from electron cryotomography."، Nature Reviews. Microbiology، 14 (4): 205–20، doi:10.1038/nrmicro.2016.7، PMC 5551487، PMID 26923112.
- R. Hovden؛ D. A. Muller (2020)، "Electron tomography for functional nanomaterials"، MRS Bulletin، 45 (4): 298–304، arXiv:2006.01652، doi:10.1557/mrs.2020.87.
- Lučič, Vladan؛ Rigort, Alexander؛ Baumeister, Wolfgang (05 أغسطس 2013)، "Cryo-electron tomography: the challenge of doing structural biology in situ"، The Journal of Cell Biology، 202 (3): 407–419، doi:10.1083/jcb.201304193، ISSN 1540-8140، PMC 3734081، PMID 23918936.
- Al-Amoudi, Ashraf؛ Chang, Jiin-Ju؛ Leforestier, Amélie؛ McDowall, Alasdair؛ Salamin, Laurée Michel؛ Norlén, Lars P. O.؛ Richter, Karsten؛ Blanc, Nathalie Sartori؛ Studer, Daniel (15 سبتمبر 2004)، "Cryo-electron microscopy of vitreous sections"، The EMBO Journal، 23 (18): 3583–3588، doi:10.1038/sj.emboj.7600366، ISSN 0261-4189، PMC 517607، PMID 15318169.
- Villa, Elizabeth؛ Schaffer, Miroslava؛ Plitzko, Jürgen M.؛ Baumeister, Wolfgang (01 أكتوبر 2013)، "Opening windows into the cell: focused-ion-beam milling for cryo-electron tomography"، Current Opinion in Structural Biology، 23 (5): 771–777، doi:10.1016/j.sbi.2013.08.006، ISSN 1879-033X، PMID 24090931.
- Briggs, John A. G. (01 أبريل 2013)، "Structural biology in situ—the potential of subtomogram averaging"، Current Opinion in Structural Biology، 23 (2): 261–267، doi:10.1016/j.sbi.2013.02.003، ISSN 1879-033X، PMID 23466038.
- Schur, Florian K. M.؛ Dick, Robert A.؛ Hagen, Wim J. H.؛ Vogt, Volker M.؛ Briggs, John A. G. (15 أكتوبر 2015)، "The Structure of Immature Virus-Like Rous Sarcoma Virus Gag Particles Reveals a Structural Role for the p10 Domain in Assembly"، Journal of Virology، 89 (20): 10294–10302، doi:10.1128/JVI.01502-15، ISSN 1098-5514، PMC 4580193، PMID 26223638.
- Zhang, Peijun (01 أكتوبر 2013)، "Correlative cryo-electron tomography and optical microscopy of cells"، Current Opinion in Structural Biology، 23 (5): 763–770، doi:10.1016/j.sbi.2013.07.017، ISSN 1879-033X، PMC 3812453، PMID 23962486.
- Chang, Yi-Wei؛ Chen, Songye؛ Tocheva, Elitza I.؛ Treuner-Lange, Anke؛ Löbach, Stephanie؛ Søgaard-Andersen, Lotte؛ Jensen, Grant J. (01 يوليو 2014)، "Correlated cryogenic photoactivated localization microscopy and cryo-electron tomography"، Nature Methods، 11 (7): 737–739، doi:10.1038/nmeth.2961، ISSN 1548-7105، PMC 4081473، PMID 24813625.
وصلات خارجية
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي