ثيويوريا
ثيويوريا هو مركب كيميائي صيغته CH4N2S، والتي يمكن كتابتها على الشكل SC(NH2)2، ويوجد على شكل صلب أبيض.
| ثيويوريا | |
|---|---|
 ثيويوريا |
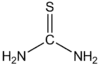 ثيويوريا |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Thiourea[1] | |
| أسماء أخرى | |
Thiourea | |
| المعرفات | |
| CAS | 62-56-6 |
| بوب كيم | 2723790 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | CH4N2S |
| الكتلة المولية | 76.12 غ/مول |
| المظهر | صلب أبيض |
| الكثافة | 1.41 غ/سم3 |
| نقطة الانصهار | 176–178 °س |
| نقطة الغليان | يتفكك |
| الذوبانية في الماء | 137 غ/ل ماء |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
يعد الثيويوريا ذا صلة بمركب اليوريا، حيث تحل فيه ذرة كبريت مكان ذرة أكسجين.
التحضير
يحضر المركب من تسخين مركب ثيوسيانات الأمونيوم حيث يحدث توازن بين الصيغيتين:[4]
أما التحضير التقني للمركب فيمكن أن يتم انطلاقاً من تمرير كبريتيد الهيدروجين على محلول من مستعلق من سياناميد الكالسيوم:[4]
الخواص
يوجد المركب في الشروط القياسية على شكل صلب بلوري أبيض اللون؛ وهو جيد الانحلال في الماء. للمركب بنية جزيئية مستوية، ويبلغ فيها طول الرابطة C=S مقدار 1.71 أنغستروم؛ أما الرابطة C-N فيبلغ طولها 1.33 أنغستروم.[5]
التطبيقات
لا توجد الكثير من التطبيقات العملية لمركب الثيويوريا، ويمكن أن يستخدم لتحضير ثنائي أكسيد الثيويوريا، والمستخدم من ضمن المختزلات في الصناعات النسيجية.[4]
طالع أيضاً
مراجع
- Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book)، Cambridge: Royal Society of Chemistry، 2014، ص. 98, 864، doi:10.1039/9781849733069، ISBN 978-0-85404-182-4.
- العنوان : THIOUREA — مُعرِّف "بَب كِيم" (PubChem CID): https://pubchem.ncbi.nlm.nih.gov/compound/2723790 — تاريخ الاطلاع: 19 نوفمبر 2016 — الرخصة: محتوى حر
- مُعرِّف "بَب كِيم" (PubChem CID): https://pubchem.ncbi.nlm.nih.gov/compound/2723790
- Mertschenk, B.; Knott, A.; Bauer, W.: Thiourea and Thiourea Derivatives, in: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2013; دُوِي:10.1002/14356007.a26_803.pub3.
- D. Mullen؛ E. Hellner (1978)، "A Simple Refinement of Density Distributions of Bonding Electrons. IX. Bond Electron Density Distribution in Thiourea, CS(NH2)2, at 123K"، Acta Crystallogr.، B34: 2789–2794، doi:10.1107/S0567740878009243.
- بوابة الكيمياء
