كلوريد ثنائي إيثيل الألومنيوم
كلوريد ثنائي إيثيل الألومنيوم هو مركب ألومنيوم عضوي شديد الخطورة وهو من أحماض لويس صيغته الكيميائية C4H10AlCl .[1][2][3]
| كلوريد ثنائي إيثيل الألومنيوم | |
|---|---|
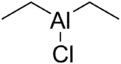 كلوريد ثنائي إيثيل الألومنيوم | |
| الاسم النظامي (IUPAC) | |
Chlorodiethylalumane | |
| أسماء أخرى | |
Chlorodiethylaluminium | |
| المعرفات | |
| رقم CAS | 96-10-6 |
| بوب كيم (PubChem) | 7277 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | C4H10AlCl |
| كتلة مولية | 120.56 غ.مول−1 |
| الكتلة المولية | 120.56 غ/مول |
| الكثافة | 0.96 غ/سم3 |
| نقطة الانصهار | −50 °س، 223 °ك، -58 °ف |
| نقطة الغليان | 125 - 126 °س، 272 °ك، -70 °ف |
| ضغط البخار | 3 مم زئبقي (عند 60 °س) |
| المخاطر | |
| رمز الخطر وفق GHS |   |
| وصف الخطر وفق GHS | خطر |
| نقطة الوميض | -18 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
التحضير
يحضر المركب من اختزال ثلاثي كلوريد ثلاثي إيثيل ثنائي الألومنيوم باستخدام الصوديوم:[4]
كما يحضر من تفاعل ثلاثي إيثيل الألومنيوم مع حمض الهيدروكلوريك:
الخواص
يوجد المركب في الشروط القياسية على شكل سائل مصفر، وتتألف بنيته من ثنائي وحدات (ديمير)، وتكون لذرة الألومنيوم المركزية فيه بنية رباعية السطوح.[5][6]
يعد المركب ذو نشاط كيميائي كبير، حتى أنه تلقائي الاشتعال.[7]
الاستخدامات
يستخدم كلوريد ثنائي إيثيل الألومنيوم ضمن حفازات تسيغلر-ناتا من أجل بلمرة الألكينات.[8]
طالع أيضاً
المراجع
- "معلومات عن كلوريد ثنائي إيثيل الألومنيوم على موقع echa.europa.eu"، echa.europa.eu، مؤرشف من الأصل في 11 مايو 2017.
- "معلومات عن كلوريد ثنائي إيثيل الألومنيوم على موقع fdasis.nlm.nih.gov"، fdasis.nlm.nih.gov، مؤرشف من الأصل في 13 ديسمبر 2019.
- "معلومات عن كلوريد ثنائي إيثيل الألومنيوم على موقع chemspider.com"، chemspider.com، مؤرشف من الأصل في 04 مارس 2016.
- Krause, Michael J.؛ Orlandi, Frank؛ Saurage, Alfred T.؛ Zietz, Joseph R. (2000)، "Aluminum Compounds, Organic"، Ullmann's Encyclopedia of Industrial Chemistry (باللغة الإنجليزية)، Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA، ص. 592–593، doi:10.1002/14356007.a01_543، ISBN 978-3-527-30673-2
- Brendhaugen, Kristen؛ Haaland, Arne؛ Novak, David P.؛ Østvold, Terje؛ Bjørseth, Alf؛ Powell, D. L. (1974)، "The Molecular Structure of Dimethylaluminium Chloride Dimer, [(CH3)2Al Cl]8, Redetermined by Gas Phase Electron Diffraction"، Acta Chemica Scandinavica، 28a: 45–47، doi:10.3891/acta.chem.scand.28a-0045.
- McMahon, C. Niamh؛ Francis, Julie A.؛ Barron, Andrew R. (1997)، "Molecular structure of [(t Bu)2Al(μ-Cl)]2"، Journal of Chemical Crystallography، 27 (3): 191–194، doi:10.1007/BF02575988، S2CID 195242291.
- Snider, Barry B.؛ Ramazanov, Ilfir R.؛ Dzhemilev, Usein M. (2009)، "Ethylaluminum Dichloride"، Encyclopedia of Reagents for Organic Synthesis، doi:10.1002/047084289X.re044.pub2، ISBN 978-0471936237.
- Fisch, A. G. (2000)، "Ziegler–Natta Catalysts"، Kirk‐Othmer Encyclopedia of Chemical Technology (باللغة الإنجليزية)، Wiley، ص. 1–22، doi:10.1002/0471238961.2609050703050303.a01.pub2، ISBN 978-0-471-48494-3، مؤرشف من الأصل في 11 فبراير 2021.
- بوابة الكيمياء
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.