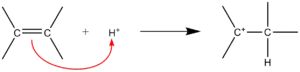Adición electrofílica
En mecanismos de reacción en química orgánica, una reacción de adición electrofílica (AEx o AdEx) es una reacción de adición donde en un compuesto químico, el sustrato de la reacción, se pierde un enlace pi para permitir la formación de dos nuevos enlaces sigma. En las reacciones de adición electrofílica, los sustratos más comunes tienen enlaces dobles o enlaces triples carbono-carbono.


Y-Z + C=C → Y-C-C-Z
Mecanismos de Adición Electrofílica
La fuerza motriz de la reacción es la formación de un enlace covalente entre el electrófilo (que tiene un LUMO de baja energía) con los átomos de carbono insaturados, por medio del orbital π que los une, formando un enlace π de 2-electrones-3-centros.
Si el electrófilo tiene carga positiva, parte de ella es transferida a los átomos de carbono.
Adición electrofílica formando un complejo π
Cuando el electrófilo es un átomo pequeño, como el ion hidrón (H+), no es posible un buen traslape entre el pequeño orbital 1s y el orbital pi del sustrato, el producto de la reacción es un carbocatión, con enlace σ de 2-electrones-2-centros entre un átomo de carbono y el átomo de hidrógeno.
Adición electrofílica de un catión H+, formando un carbocatión
En la etapa 2 de una Adición Electrofílica, el intermediario con carga positiva se combina con un nucleófilo, para formar un segundo enlace covalente.
Segundo paso en la adición electrofílica, involucrando intermediarios de 3-centros
Segundo paso en la adición electrofílica, involucrando carbocationes
En las reacciones de adición electrofílica a carbono con un reactivo electrófilo asimétrico, la regioselectividad es importante, y suele estar determinada por la regla de Markovnikov.
El ataque de un electrófilo al sistema π de un anillo aromático suele conducir a la sustitución electrofílica aromática en vez de una reacción de adición.
Orden de las reacciones de adición electrofílica
Generalmente, las reacciones de adición electrofílica son de segundo orden o bimoleculares, con etapa limitante en la formación del carbocatión o del intermediario de 3 centros. En este caso, la diferencia entre la etapa 1 y 2 del mecanismo de reacción es marcada, con lo que la reacción se denomina adición electrofílica bimolecular (AdE2 o AE2). Sin embargo, también se reportan cinéticas más compleja, que sugiera ser de tercer orden. La reacción en este caso es adición electrofílica termolecular ((AdE3 o AE3).[1]
Reacciones típicas AdEx
- Halogenación electrofílica: X2
- Hidrohalogenación:HX
- Reacción de hidratación: H2O
- Reacción de hidrogenación H2
- Reacción de solvomercuración: acetato de mercurio(II), solvente nucleofílico
- Reacción de hidroboración : diborano
- la reacción de Prins : formaldehído, agua
Referencias
- Carey, F.; Sundberg, R. (2000). Advanced Organic Chemistry (en inglés) (4ª edición). Springer. pp. 364-366. ISBN 0306462435.