Constante de Madelung
La constante de Madelung es un factor de corrección que contempla las interacciones electrostáticas de los iones más alejados que la simple pareja anión-catión y depende exclusivamente de la geometría del cristal iónico.[1] Se puede calcular como una suma de la contribución de los iones vecinos más cercanos, más la de los segundos vecinos más cercanos, y así sucesivamente.[2] La halló el físico alemán Erwin Madelung en 1918.[3]
Expresión formal
La constante de Madelung permite el cálculo del potencial eléctrico Vi en la posición ri debido a los iones en las posiciones rj:
donde rij =|ri - rj| es la distancia entre los iones i-ésimo y j-ésimo. Además,
- zj = número de cargas del ion j-ésimo
- e = 1.6022×10-19 C
- 4 π ϵ0 = 1.112×10-10 C²/(J m).
Si se normalizan las distancias rij a la distancia del vecino más cercano r0, el potencial se puede escribir
donde es la constante de Madelung (adimensional) del ion i-ésimo
La energía electrostática del ion en la posición es el producto de su carga por el potencial:
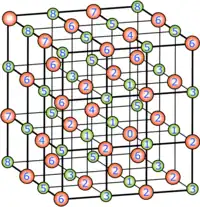
Cualquier cristal macroscópico se puede aproximar muy bien por un cristal infinito, ya que incluso un cristal de un millón de átomos de lado albergaría átomos, por lo que sería un cristal del orden de miligramos, aún microscópico. En un cristal infinito los átomos sólo se diferencian por su tipo y por el lugar que ocupen en la celdilla elemental, ya que no hay átomos más cercanos al borde que otros. En dicha estructura cristalina hay una constante de Madelung por cada ion que ocupe un sitio distinto en la red. Por ejemplo, para el cristal de cloruro sódico hay dos constantes de Madelung – una para el Na+ y otra para el Cl-. Ya que ambos iones, sin embargo, ocupan sitios de la red con la misma simetría ambos tienen la misma magnitud y difieren solo en el signo. Se asume que la carga eléctrica de los iones Na+ y Cl- es positiva y negativa, respectivamente, y . La distancia a primeros vecinos es la mitad del parámetro de red de la celda unidad cúbica y la constante de Madelung queda

La prima indica que se excluye el término . Ya que esta suma es condicionalmente convergente no es adecuado como definición de la constante de Madelung a menos que el orden de la suma se especifique. Hay dos maneras obvias de calcular esta serie, como límite de cubos o como límite de esferas infinitamente grandes. El último, a pesar de que no hay cristales esféricos, es el más popular debido a su simplicidad. Por ello, el siguiente desarrollo se encuentra frecuentemente en la literatura:[4]
Sin embargo, esto es incorrecto ya que estas series divergen como demostró Emersleben en 1951.[5][6] El límite de los cubos converge al valor correcto. Borwein, Borwein y Taylor dan una definición matemática sin ambigüedad por medio de la extensión analítica de series absolutamente convergentes.
Hay muchos métodos prácticos para calcular la constante de Madelung ya sea usando una suma directa (por ejemplo, el método de Evjen[7]) o una transformada integral en el método de Ewald.[8]
| Ion en compuesto cristalino | (basado en ) | (basado en ) |
|---|---|---|
| Cl− y Na+ en halita NaCl | ±1.748 | ±3.495 |
| S2− y Zn2+ en blenda ZnS | ±1.638 | ±3.783 |
| S22− en pirita FeS2 | … | 1.957 |
| Fe2+ en pirita FeS2 | … | -7.458 |
Generalización
En el cálculo de las constantes de Madelung la carga de un ion se considera puntual. Esto es correcto si la distribución de electrones del ion tiene simetría esférica. En casos particulares, sin embargo, cuando los iones residen los nudos de la red de ciertos grupos cristalográficos, puede ser necesaria la inclusión de momentos de orden superior, es decir, momentos multipolares de la distribución de carga. La electrostática nos dice que la interacción entre dos cargas puntuales solo es el primer término de una serie de Taylor que describe la interacción entre dos distribuciones de carga de forma arbitraria. En consecuencia, la constante de Madelung solo representa el término monopolo-monopolo.
El modelo de interacción electrostática de iones en sólidos se extiende así a un modelo multipolar que también incluye momentos multipolares más altos como dipolos, cuadrupolos, etc. [10][11][12] Estos modelos requieren la determinación de constantes de Madelung de orden superior, llamadas constantes de red electrostática. En su caso, en lugar de la distancia vecina más cercana , se usa otra longitud estándar como la raíz cúbica del volumen de la celda unidad para propósitos de normalización. Por ejemplo, la constante de Madelung queda como
El cálculo adecuado de las constantes de la red electrostática tiene que considerar los grupos cristalográficos de los sitios de redes iónicas; por ejemplo, los momentos dipolares solo pueden surgir en sitios polares de la red, es decir exhibiendo una simetría de sitio C1, C1h, Cn o Cnv (n = 2, 3, 4 o 6).[13] Estas constantes de Madelung de segundo orden tienen efectos significativos sobre la energía reticular y otras propiedades físicas de los cristales heteropolares. [14]
Aplicación a sales orgánicas
La constante de Madelung también sirve para el cálculo de la energía de la red de sales orgánicas. Izgorodina y su equipo han descrito un método generalizado (llamado el método de EUGEN) para calcular la constante de Madelung para cualquier estructura cristalina.[15]
Véase también
Referencias
- Gilreath, E.S (1958). Fundamental concepts of inorganic chemistry. McGraw-Hill.
- Magnitudes, unitades y símbolos en química física. Volum 3 de Nomenclatura de química. Barcelona. 2004. p. 58. ISBN 9788472837331.
- Madelung, E (1918). «Das elektrische Feld in Systemen von regelmäßig angeordneten Punktladungen». Phys. Zs. XIX: 524-533.
- Charles Kittel: Introducción a la Física del estado Sólido., Wiley 1995, ISBN 0-471-11181-3
- O. Emersleben: Mathematische Nachrichten 4 (1951), 468
- D. Borwein, J. M. Borwein, K. F. Taylor: "Convergence of Lattice Sums and Madelung's Constant", J. Math. Phys. 26 (1985), 2999–3009, doi 10.1063/1.526675
- H. M. Evjen: "On the Stability of Certain Heteropolar Crystals", Phys. Rev. 39 (1932), 675–687, http://link.aps.org/abstract/PR/v39/p675
- P. P. Ewald: "Die Berechnung optischer und elektrostatischer Gitterpotentiale", Ann. Phys. 64 (1921), 253–287, doi 10.1002/andp.19213690304
- Bailey, David; Borwein, Jonathan; Kapoor, Vishaal; Weisstein, Eric (9 de marzo de 2006). «Ten Problems in Experimental Mathematics». The American Mathematical Monthly 113 (6).
- J. Kanamori; T. Moriya; K. Motizuki & T. Nagamiya (1955). «Methods of Calculating the Crystalline Electric Field». J. Phys. Soc. Jap. 10: 93-102. Bibcode:1955JPSJ...10...93K. doi:10.1143/JPSJ.10.93. Parámetro desconocido
|last-author-amp=ignorado (ayuda) - B. R. A. Nijboer & F. W. de Wette (1957). «On the calculation of lattice sums». Physica 23: 309-321. Bibcode:1957Phy....23..309N. doi:10.1016/S0031-8914(57)92124-9.
- E. F. Bertaut (1978). «The equivalent charge concept and its application to the electrostatic energy of charges and multipoles». J. Phys. (Paris) 39: 1331-48. Bibcode:1978JPCS...39...97B. doi:10.1016/0022-3697(78)90206-8.
- M. Birkholz (1995). «Crystal-field induced dipoles in heteropolar crystals – I. concept». Z. Phys. B 96: 325-332. Bibcode:1995ZPhyB..96..325B. doi:10.1007/BF01313054.
- M. Birkholz (1995). «Crystal-field induced dipoles in heteropolar crystals – II. physical significance». Z. Phys. B 96 (3): 333-340. Bibcode:1995ZPhyB..96..333B. doi:10.1007/BF01313055.
- E. Izgorodina (2009). «The Madelung Constant of Organic Salts». Crystal Growth & Design 9: 4834-4839. doi:10.1021/cg900656z.
Enlaces externos
- Glasser, Leslie (2012). «Solid-state energetics and electrostatics: Madelung constants and Madelung energies». Inorg. Chem. 51: 2420-2424. doi:10.1021/ic2023852.
- Sakamoto, Y. (1958). «Madelung constants of simple crystals expressed in terms of Born's basic potentials of 15 figures». J. Chem. Phys. 28: 164. Bibcode:1958JChPh..28..164S. doi:10.1063/1.1744060.
- Sakamoto, Y. (1958). «Errata 2: Madelung constants of simple crystals expressed in terms of Born's basic potentials of 15 figures». J. Chem. Phys. 28: 1253. Bibcode:1958JChPh..28.1253S. doi:10.1063/1.1744387.
- Zucker, I. J. (1975). «Madelung constants and lattice sums for invariant cubic lattice complexes and certain tetragonal structures». J. Phys. A: Math. Gen. 8 (11): 1734. Bibcode:1975JPhA....8.1734Z. doi:10.1088/0305-4470/8/11/008.
- Zucker, I. J. (1976). «Functional equations for poly-dimensional zeta functions and the evaluation of Madelung constants». J. Phys. A: Math. Gen. 9 (4): 499. Bibcode:1976JPhA....9..499Z. doi:10.1088/0305-4470/9/4/006.
- Weisstein, Eric W. «Madelung Constants». En Weisstein, Eric W, ed. MathWorld (en inglés). Wolfram Research.
- (sucesión A085469 en OEIS)