Diastereoisómero
Los diastereoisómeros o diastereómeros son una clase de estereoisómeros tales que no son superponibles pero tampoco son imagen especular uno del otro, es decir, no son enantiómeros.
El diastereomerismo se produce cuando dos o más estereoisómeros de un compuesto tienen configuraciones diferentes en una o más, pero no todas las equivalentes relacionadas. Los estereocentros no son imágenes especulares uno del otro. Cuando dos diastereoisómeros se diferencian entre sí en un solo estereocentro, son epímeros. Cada estereocentro da lugar a dos configuraciones diferentes y por lo tanto aumenta el número de estereoisómeros en un factor de dos.
Los diastereoisómeros se diferencian de los enantiómeros ya que estos últimos son los pares de estereoisómeros que difieren de todos los estereocentros y por lo tanto son reflejos uno del otro. Los enantiómeros de un compuesto con más de un estereocentro también son llamados diastereoisómeros de los otros estereoisómeros del compuesto que no es su imagen especular. Los diastereómeros tienen diferentes propiedades físicas y diferente reactividad, a diferencia de los enantiómeros.[1]
Isomería cis-trans y isomería conformacional son también formas de diastereomerismo.
'Diastereoselectividad' es la preferencia por formación de uno o más diastereómero sobre otro en una reacción orgánica.
Eritro / treo
Dos prefijos comunes utilizados para distinguir los diastereoisómeros son treo y
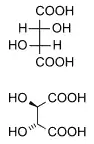
(que corresponden a las etiquetas anti y syn respectivamente). Cuando se dibuja en la proyección de Fischer el isómero eritro tiene dos sustituyentes idénticas en el mismo lado y el isómero Treo las tiene en lados opuestos. Cuando se dibuja como una cadena en zig-zag, el isómero eritro tiene dos sustituyentes idénticos en distintos lados del plano (isómero anti). Los nombres eritro y treo se derivan de aldosa eritrosa (un jarabe) y aldosa treosa (punto de fusión 126 °C).
Un compuesto con una proyección de Fisher del tipo eritro (sustituyentes del mismo lado), mostrará en la proyección de cuñas la etiqueta anti (sustituyentes a lados diferentes del plano). En cambio, un compuesto con una proyección de Fisher del tipo treo (sustituyentes en lados opuestos), mostrará en la proyección de cuñas la etiqueta sin (sustituyentes a lados diferentes del plano). Como es lógico, al pasar una Fisher con sustituyentes del mismo lado a proyección en cuñas, obtendremos los sustituyentes en lados opuestos del plano, y lo contrario si en Fisher se encuentran en lados opuestos.
Las etiquetas eritro y treo están en desuso, prácticamente se emplean sólo anti y sin.
Otro componente treo es la treonina, uno de los aminoácidos esenciales. El diastereoisómero eritro se llama allo-treonina.
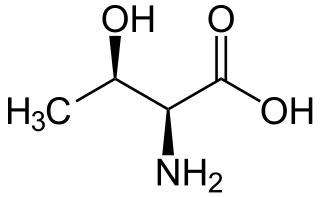 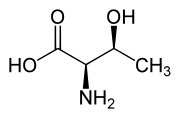 |
| L -treonina (2 S, 3 R) y D -treonina (2 R, 3 S) |
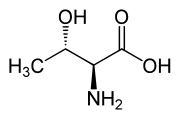 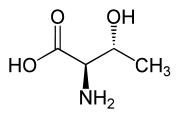 |
| L - allo - treonina (2 S, 3 S) y D - allo - treonina (2 R, 3 R) |
Estereocentros múltiples
Si una molécula contiene dos átomos de carbono asimétricos, hay hasta 4 configuraciones posibles, y no todas pueden ser imágenes idénticas no sobrepuestas. Las posibilidades continuarán multiplicándose a medida que existen centros más asimétricos en una molécula. En general, el número de isómeros configuracional de una molécula puede determinarse calculando 2 n , siendo n; el número de centros quirales en una molécula. Esto se aplica salvo en casos donde la molécula tiene forma meso.
Ejemplos
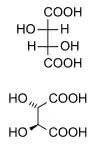
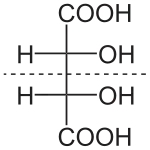
El Ácido tartárico contiene dos centros asimétricos, pero dos de los "isómeros" son equivalentes y juntos se denominan compuesto meso. Esta configuración no es ópticamente activa, mientras que los restantes dos isómeros son D - y L -imágenes especulares, es decir , enantiómeros. La forma meso es un diastereoisómero de otras formas.
|
|
 |
 |
|
(natural) ácido tartárico |
D-(-)-ácido tartárico |
ácido mesotartárico |
|
(1:1) |
||
Las familias de 4, 5 y 6 carbonos carbohidratos contienen muchos diastereoisómeros debido a la gran cantidad de centros asimétricos en estas moléculas.
Aplicaciones
Como se ha explicado anteriormente, dos enantiómeros tienen propiedades químicas idénticas, al contrario que los diastereoisómeros. Este conocimiento se aprovecha en la síntesis quiral para separar una mezcla de enantiómeros. Este es el principio de la resolución quiral. Después de preparar los diastereoisómeros, éstos se separan por cromatografía o recristalización. Se debe tener en cuenta también el ejemplo de la estereoquímica de cetonización de enoles y enolatos.
Por lo tanto, de dos diastereoisómeros, se observaron dos picos cuando los analizaron mediante NMR.
Características
Los diastereoisómeros difieren en sus propiedades físicas y químicas. Por ello pueden separarse mediante procedimientos de destilación, cristalización o cromatografía.
Dentro del grupo de los diastereómeros se encuentran los isómeros cis-trans (antes conocidos como isómeros geométricos), los confórmeros o isómeros conformacionales y, en las moléculas con varios centros quirales, los isómeros que pertenecen a distintas parejas de enantiómeros.
Si una molécula tiene varios centros quirales obtendremos diastereómeros cambiando la configuración absoluta de uno de los centros quirales y manteniendo la del resto; veámoslo en el ácido tartárico:
COOH COOH
| |
(R) H-C-OH HO-C-H (S)
| |
(S) H-C-OH H-C-OH (S)
| |
COOH COOH
Un ejemplo de los diastereómeros cis-trans es el ácido 2-butenodioico, que tiene 2 estereoisómeros:
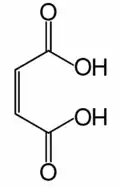 Ácido Z-2-butenodioico (ácido maleico). |
 Ácido E-2-butenodioico (ácido fumárico). |
Véase también
- Isomería.
- Enantiómero.
- Reglas de prioridad de Cahn-Ingold-Prelog para la nomenclatura.
Referencias
- «Diastereoisómeros». Consultado el 14 de septiembre de 2022.