EspectroscopÍa de resonancia magnética nuclear
La espectroscopía de resonancia magnética nuclear (RMN) es una técnica empleada principalmente en la elucidación de estructuras moleculares, aunque también se puede emplear con fines cuantitativos y en estudios cinéticos y termodinámicos.
Algunos núcleos atómicos sometidos a un campo magnético externo absorben radiación electromagnética en la región de las frecuencias de radio o radiofrecuencias. Como la frecuencia exacta de esta absorción depende del entorno de estos núcleos, se puede emplear para determinar la estructura de la molécula en donde se encuentran estos.
Para que se pueda emplear la técnica los núcleos deben tener un momento magnético distinto de cero. Esta condición no la cumplen los núcleos con número másico y número atómico par (como el 12C, 16O, 32S). Los núcleos más importantes en química orgánica son: 1H, 13C, 31P, 19F y 15N. Otros núcleos importantes: 7Li, 11B, 27Al, 29Si, 77Se, 117Sn, 195Pt, 199Hg, 203Tl, 205Tl, 207Pb
Se prefieren los núcleos de número cuántico de espín nuclear igual a 1/2, ya que carecen de un momento cuadrupolar eléctrico que produce un ensanchamiento de las señales de RMN. También es mejor que el isótopo sea abundante en la naturaleza, ya que la intensidad de la señal dependerá de la concentración de esos núcleos activos. Por eso, uno de los más útiles en la elucidación de estructuras es el 1H, dando lugar a la espectroscopia de resonancia magnética nuclear de protón. También es importante en química orgánica el 13C, aunque se trata de un núcleo poco abundante y poco sensible.
La técnica se ha empleado en química orgánica, química inorgánica y bioquímica. La misma tecnología también ha terminado por extenderse a otros campos, por ejemplo en medicina, en donde se obtienen imágenes por resonancia magnética.
Historia
La primera detección de Resonancia Magnética Nuclear debida a la formación de una diferencia en las energías de ciertos núcleos en presencia de un campo magnético fue reportada independientemente por el grupo de Felix Bloch de la Stanford University (para el agua líquida) y el grupo de Edward Mills Purcell en la Harvard University (para la cera de parafina) en 1946. Purcell y Bloch compartieron en 1952 el Premio Nobel de Física por estos descubrimientos.[1] La aplicación química de la RMN fue descubierta a principios de los cincuenta, al observarse que la frecuencia de resonancia de un núcleo dependía fuertemente de su entorno químico (chemical shift). A partir de los años setenta, el desarrollo de nuevas técnicas y mayores campos magnéticos (que incrementan tanto la sensibilidad como la resolución de las señales) permitieron estudiar moléculas cada vez más grandes. El advenimiento de la RMN multidimensional y el uso del marcaje 13C y 15N marcó el inicio de la RMN biológica.
Tipos de espectroscopias de RMN
Espectroscopia de RMN con onda continua (CW: Continuous Wave)
Desde sus comienzos hasta finales de los 60, la espectroscopia de RMN utilizó una técnica conocida como espectroscopia de onda continua (CW). La manera de registrar un espectro de RMN en el modo de CW era, bien mantener constante el campo magnético e ir haciendo un barrido de frecuencias con un campo oscilante, o bien, lo que era usado más a menudo, se mantenía constante la frecuencia del campo oscilante, y se iba variando la intensidad del campo magnético para encontrar las transiciones (picos del espectro). En la RMN de CW las señales del espectro se registran como señales en resonancia.
La espectroscopia CW está limitada por su baja sensibilidad, ya que cada señal se registra una sola vez por cada barrido y la técnica de resonancia magnética nuclear ya es de por sí no demasiado sensible; esto quiere decir que la técnica sufre de una baja relación señal-ruido. Afortunadamente, en RMN es posible mejorar la relación señal-ruido mediante el promediado de señal. El promediado de señal consiste en repetir la adquisición del experimento e ir sumando los espectros que se obtienen. De esta manera, las zonas del espectro en que existen señales se suman de manera constructiva, mientras que, por su parte, las zonas en que hay ruido, por su carácter aleatorio, se acumula más lentamente que la señal. Mediante el promediado de señal se incrementa la relación señal-ruido en un valor que es la raíz cuadrada del número de espectros que se han acumulado. Esta relación se cumple con espectros de RMN en los que intervienen un solo tipo de núcleos, por ejemplo, sólo 1H, 13C, etc., también llamados espectros homonucleares.
Espectroscopia de RMN de pulsos y transformada de Fourier
La técnica de RMN con transformada de Fourier (FT-NMR) es la que se utiliza en los espectrómetros actuales. Uno de los pioneros en este campo es Richard R. Ernst, que la desarrolló a partir del año 1966 y por la que fue galardonado con el Premio Nobel de Química en 1991.
FT-NMR permite disminuir drásticamente el tiempo que requiere adquirir una acumulación (scan) del espectro completo de RMN. En vez de realizar un barrido lento de la frecuencia, una en cada instante, esta técnica explora simultánea e instantáneamente todo un rango de frecuencias. Dos desarrollos técnicos fueron fundamentales para poder hacer realidad la técnica FT-NMR: ordenadores capaces de llevar a cabo las operaciones matemáticas necesarias para pasar desde el dominio de tiempo al de la frecuencia, es decir, para obtener el espectro; y el conocimiento sobre cómo poder excitar simultáneamente todo un rango de frecuencias.
La FT-NMR funciona con la muestra (espines nucleares) sometida a un campo magnético externo constante. Se irradia la muestra con un pulso electromagnético de muy corta duración en la región de las radiofrecuencias. La forma que suele usarse para este pulso es rectangular, es decir, la intensidad de la radiofrecuencia oscila entre un máximo y un mínimo que es constante mientras dura el pulso. Un pulso de corta duración tiene una cierta incertidumbre en la frecuencia (principio de indeterminación de Heisenberg). La descomposición de fourier de una onda rectangular contiene contribuciones de una de todas las frecuencias. El pulso que se genera es por tanto policromático y cuanto más corto sea, es capaz de excitar un mayor rango de frecuencias.
La aplicación de un pulso policromático en una región estrecha de la banda de radiofrecuencias (MHz) afecta a aquellos espines nucleares que resuenen en esa región. Un pulso policromático con una anchura en frecuencia de unos pocos kHz puede llegar a excitar simúltaneamente sólo a los espines nucleares de un mismo tipo de núcleo atómico dentro de una molécula, por ejemplo, todos los núcleos de hidrógeno (1H). Antes del pulso el vector de polarización neta de cada uno de los espines nucleares se encuentra en situación de equilibrio alineado en la dirección del campo magnético. Durante el tiempo que se aplica el pulso, el pulso introduce un segundo campo magnético en una dirección perpendicular al campo principal del imán y el vector polarización realiza un determinado movimiento de precesión. Tras cesar el pulso, el vector polarización de todos los espines afectados puede formar un cierto ángulo con el eje del campo magnético principal. En este momento, los espines, comportándose como pequeños imanes polarizados, comienzan a precesionar con su frecuencia característica en torno al campo magnético externo, induciendo una pequeña corriente oscilante de RF en una bobina receptora situada en las inmediaciones de la muestra. A medida que los núcleos van regresando poco a poco a la situación inicial de equilibrio alineados con en el campo magnético principal, la señal detectada va disminuyendo de intensidad hasta hacerse cero. Esta caída de la señal se conoce como caída libre de la inducción (Free Induction Decay) (FID) y da lugar al espectro de RMN.
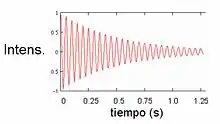
La FID es una onda que contiene todas las señales del espectro en una forma que es dependiente del tiempo. Esta onda puede convertirse en un espectro de señales en función de su frecuencia. Para ello se utiliza una función matemática conocida como transformada de Fourier. El resultado es lo que se conoce como un espectro de RMN (espectro de frecuencias).
RMN multidimensional
La posibilidad de excitar la muestra con uno o más pulsos de radiofrecuencia (RF), cada uno de ellos aplicado con una potencia, duración, frecuencia, forma y fase particulares, e introducirlos en momentos específicos de tiempo durante el experimento de RMN, generalmente antes de que el sistema haya regresado al equilibrio por relajación, permite diseñar toda una gama de secuencias de pulsos de las que se puede extraer información molecular muy variada.
Una secuencia de pulsos es una distribución en el tiempo de alguno o varios de los siguientes elementos: i) un cierto número de pulsos de RF que afecten a uno o más tipos de núcleos, ii) tiempos de espera en los que no se hace nada sino esperar a que el sistema evolucione de una determinada forma. Estos tiempos de espera pueden ser fijos o bien incrementables si su duración se va aumentando a medida que se repite el experimento. iii) gradientes de campo magnético y iv) una etapa final en la que se adquiere la FID.
En un experimento de RMN multidimensional la secuencia de pulsos debe constar de al menos dos pulsos y éstos deben separados por un periodo de espera incrementable. La secuencia de pulsos se repite un número de veces adquiriéndose una FID en cada ocasión. La fase de alguno de los pulsos puede alterarse en cada repetición así como incrementarse la duración de uno o más tiempos de espera variables. Si la secuencia de pulsos tiene un tiempo de espera incrementable el experimento tendrá dos dimensiones, si tiene dos será de tres dimensiones, si tiene tres el experimento será de cuatro dimensiones. Aunque en teoría no existe límite en el número de dimensiones de un experimento, experimentalmente hay limitaciones impuestas por la consiguiente pérdida de señal por relajación que conlleva la detección de las distintas dimensiones. Los tiempos de registro de los experimentos de RMN multidimensional se pueden acortar drásticamente con las técnicas rápidas de RMN desarrolladas en la presente década.
Los experimentos multidimensionales se pueden clasificar en dos tipos principales:
Experimentos de correlación homonuclear: Son aquellos en los que todas las dimensiones corresponden al mismo núcleo. Ejemplos: COSY (COrrelation SpectroscopY), TOCSY (TOtal Correlation SpectroscopY), NOESY (Nuclear Overhauser Effect SpectroscopY).
Experimentos de correlación heteronuclear: En este experimentos se obtienen espectros cuyas dimensiones pertenecen a diferentes núcleos. Ejemplos: HMQC (Heteronuclear Multiple Quantum Correlation), HSQC (Heteronuclear Simple Quantum Correlation), HMBC (Heteronuclear Multiple Bond Correlation), HOESY (Heteronuclear Overhauser Effect SpectroscopY).
Grosso modo, las interacciones que pueden detectarse por RMN se pueden clasisficar en dos tipos:
- Las interacciones a través de enlaces se basan en el acoplamiento escalar
- Las interacciones a través del espacio se basan en el acoplamiento dipolar. En el caso de muestras en disolución, el acoplamiento dipolar se manifiesta como efecto Overhauser nuclear que permite determinar la distancia entre los átomos.
Richard Ernst en 1991 y Kurt Wüthrich en el 2002 fueron galardonados con el premio Nobel de Química por su contribuciones al desarrollo de la RMN de 2-dimensiones y multidimensional con transformada de Fourier. Los avances conseguidos por ellos y por otros grupos de investigadores han expandido la RMN a la bioquímica, y en particular a la determinación de la estructura en disolución de biopolímeros como proteínas o incluso ácidos nucleicos de tamaño pequeño.
Sólidos
La RMN en disolución es complementaria de la cristalografía de rayos X ya que la primera permite estudiar la estructura tridimensional de las moléculas en fase líquida o disuelta en un cristal líquido, mientras que la cristalografía de rayos-X, como su nombre indica, estudia las moléculas en fase sólida.
La RMN puede utilizarse también para el estudio de muestras en estado sólido. Si bien en su estado actual queda lejos de poder proporcionar con buen detalle la estructura tridimensional de una biomolécula.
En el estado sólido las moléculas están estáticas y no existe, como ocurre con las moléculas en disolución, un promediado de la señal de RMN por el efecto de la rotación térmica de la molécula respecto a la dirección del campo magnético. Las moléculas de un sólido están prácticamente inmóviles, y cada una de ellas experimenta un entorno electrónico ligeramente diferente, dando lugar a una señal diferente. Esta variación del entorno electrónico disminuye la resolución de las señales y dificulta su interpretación. Raymond Andrew fue uno de los pioneros en el desarrollo de métodos de alta resolución para resonancia magnética nuclear en estado sólido. Él fue quien introdujo la técnica de la rotación en el ángulo mágico Magic Angle Spinning (MAS) que permitió incrementar la resolución de los espectros de sólidos varios órdenes de magnitud. En MAS, las interacciones se promedian rotando la muestra a una velocidad de varios kilohertzios.
Alex Pines en colaboración con John Waugh revolucionaron también la RMN de sólidos introduciendo la técnica de la polarización cruzada (CP) que consigue incrementar la sensibilidad de núcleos poco abundantes gracias a la transferencia de polarización de los protones a los núcleos más insensibles cercanos, generalmente 13C, 15N o 29Si.
A caballo entre la RMN en disolución y en fase sólida, se encuentra la técnica de HR-MAS (High Resolution with Magic Angle Spinning), cuya aplicación fundamental es el análisis de geles y materiales semisólidos. El fundamento del HR-MAS es hacer girar la muestra, al ángulo mágico, a una velocidad muy superior que en sólidos habituales. El efecto conseguido son espectros mono y bidimensionales de gran calidad, próxima a la RMN en disolución. La principal aplicación de esta técnica es el análisis de matrices biológicas y poliméricas, como resinas para síntesis en fase sólida solvatadas.
Sensibilidad
Debido a que la intensidad de la señal de RMN, y la sensibilidad de la técnica depende de la fortaleza del campo magnético, desde los inicios de la RMN ha existido gran interés por el desarrollo de imanes más potentes. En la actualidad los imanes comerciales más potentes están en torno a los 22.31 T, o 950 MHz frecuencia de resonancia de 1H. Los avances en la tecnología audio-visual e informática también han mejorado los aspectos de generación de pulsos y la recepción de señal y el procesado de la información.
La sensibilidad de las señales también depende de la presencia de núcleos magnéticamente-susceptibles a la RMN y, por tanto, de la abundancia natural de tales núcleos. Para el caso de biomoléculas los núcleos más abundantes y magnéticamente susceptibles son los isótopos de hidrógeno 1H y fósforo 31P. Por el contrario, núcleos como carbono y nitrógeno tienen isótopos útiles a la RMN, 13C y 15N, respectivamente, pero se presentan en baja abundancia natural. Para hacer frente a esta dificultad existe la posibilidad de enriquecer las moléculas de la muestra con estos isótopos (ej. sustitución de 12C por 13C y/o de 14N por 15N) para poder estudiarlos por RMN con la suficiente sensibilidad. Se trata de isótopos perfectamente estables que no producen más que una pequeña variación en la masa molecular de la molécula, sin afectar para nada a otras propiedades estructurales o químicas de la muestra.
Instrumentación en resonancia magnética nuclear: el espectrómetro
Un espectrómetro de RMN consta de las siguientes partes fundamentales:
- Un imán que genere un campo magnético estable, el cual puede ser de una intensidad variable, definiendo la frecuencia de resonancia de cada núcleo. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del protón, así en un imán de 7.046 Tesla, los núcleos de 1H resuenan a 300 MHz, y por tanto sería un espectrómetro de 300 MHz. Por el momento el imán de mayor campo magnético del mundo lo ha instalado Bruker en la Unviersiad de ciencia y tecnología Rey Abdullah en Arabia Saudita, de 950 MHz (22.3 Tesla).[2]
- Una sonda, que se sitúa dentro del imán, en la que se introduce la muestra y que consta de las bobinas responsables de emitir y recibir las radiofrecuencias (RF). El número de bobinas y su disposición determinan el tipo y las aplicaciones de cada sonda.
- Una consola en la que se generan los pulsos de RF y se controla el resto de la parte electrónica del espectrómetro.
- Un ordenador que sirve de interfaz con el espectrómetro y con el que se analiza toda la información obtenida.
Información obtenida mediante RMN
La aplicación fundamental de la espectroscopia de RMN es la determinación estructural, ya sea de moléculas orgánicas, organometálicas o biológicas. Para ello es necesario la realización de diferentes tipos de experimentos de los cuales se obtiene una determinada información.
Para la elucidación estructural de moléculas orgánicas y organometálicas los experimentos más utilizados son los siguientes:
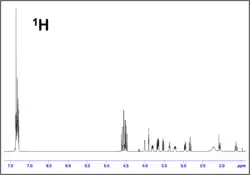
- Espectro monodimensional de 1H: Da información del número y tipo de hidrógenos diferentes que hay en la molécula. La posición en el espectro (desplazamiento químico) determina el entorno químico del núcleo, y por tanto da información de grupos funcionales a los que pertenecen o que están cerca. La forma de la señal da información de los protones cercanos acoplados escalarmente.
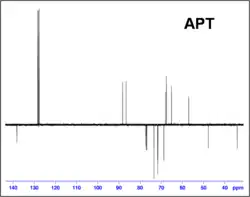
- Espectro monodimensional de 13C: Al igual que en 1H el desplazamiento químico da información de los grupos funcionales. Dependiendo del tipo de experimento realizado se puede obtener información del número de hidrógenos unidos a cada carbono.
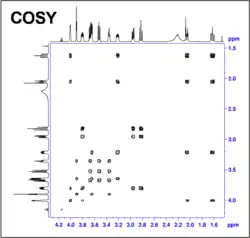
- Espectros bidimensionales homonucleares: Los experimentos COSY y TOCSY dan información de las relaciones entre los protones de la molécula, por acoplamiento escalar o dipolar (NOESY)
- Espectros bidimensionales heteronucleares: Los experimentos HMQC y HSQC indican qué hidrógenos están unidos a qué carbonos. El experimento HMBC permite determinar relaciones entre protones y carbonos a mayor distancia (2 o 3 enlaces)
- Experimentos con otros núcleos: Si la molécula posee otros núcleos activos en RMN es posible su medida a través de experimentos monodimensionales o bidimensionales (por detección indirecta)
Referencias
- «Background and Theory Page of Nuclear Magnetic Resonance Facility». Mark Wainwright Analytical Centre - University of Southern Wales Sydney. 9 de diciembre de 2011. Archivado desde el original el 27 de enero de 2014. Consultado el 9 de febrero de 2014.
- Instalaciones científicas de la U.C.T.R.A. (KAUST)