Factor de compresibilidad
El factor de compresibilidad (Z), conocido también como el factor de compresión, es la razón del volumen molar de un gas con relación al volumen molar de un gas ideal a la misma temperatura y presión. Es una propiedad termodinámica útil para aplicar la ley de los gases ideales al comportamiento de un gas real.[1] En general, la desviación del comportamiento ideal se vuelve más significativa cuanto más cercano esté un gas a un cambio de fase, sea menor la temperatura o más grande]] la cual toma constantes empíricas de compuestos específicos como datos de entrada. Para un gas que sea una mezcla de dos o más gases puros (aire o gas natural, ejemplo), es requerida una composición del gas para que la compresibilidad sea calculada.
De manera alternativa, el factor de compresibilidad para gases específicos puede ser leído a partir de gráficos de compresibilidad generalizados[1] que grafiquen como una función de la presión a temperatura constante.
Definición y significado físico
El factor de compresibilidad es definido como
donde es el volumen molar, es el volumen molar del correspondiente gas ideal, es la presión, es la temperatura, y es la constante universal de los gases ideales. Para aplicaciones de ingeniería, es expresado frecuentemente como
donde es la densidad del gas y es la constante de los gases específica,[2] y es la masa molar.
Para un gas ideal, el factor de compresibilidad es por definición. En muchas aplicaciones del mundo real, los requerimientos de precisión demandan que las desviaciones del comportamiento de un gas, esto es, el comportamiento de un gas real, sean tomadas en cuenta. El valor de generalmente se incrementan con la presión y decrecen con la temperatura; a altas presiones las moléculas colisionan más a menudo, y esto permite que las fuerzas repulsivas entre las moléculas tengan un efecto notable, volviendo al volumen molar del gas real () más grande que el volumen molar del correspondiente gas ideal (), lo que causa que sea mayor a 1.[3] Cuando las presiones son menores, las moléculas son libres de moverse; en este caso, dominan las fuerzas de atracción, haciendo que . Cuanto más cercano esté el gas a su punto crítico o su punto de ebullición, se desviará más del caso ideal.
Gráficas de factor de compresibilidad generalizados para gases puros
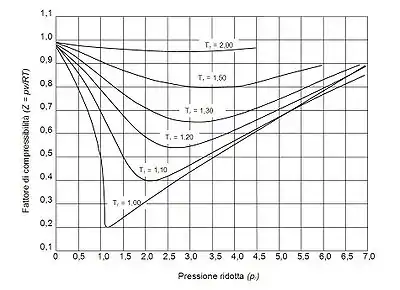
La relación única entre el factor de compresibilidad, la temperatura y presión reducidas, y respectivamente, fue reconocida en principio por Johannes van der Waals en 1873 y es conocida como el teorema de los estados correspondientes de dos parámetros. El principio de estados correspondientes expresa la generalización de las propiedades de un gas, las cuales dependen de las fuerzas moleculares, están relacionadas con las propiedades críticas del gas en una forma universal. Eso provee una base más importante para desarrollar correlaciones de propiedades moleculares.
En cuanto a la compresibilidad de los gases, el principio de estados correspondientes indica que cualquier gas puro a la misma temperatura reducida, , y presión reducida, , debe tener el mismo factor de compresibilidad.
La temperatura y la presión reducidas están definidas por
- y
Aquí y son la temperatura crítica y la presión crítica del gas, respectivamente. Estas son características de cada gas específico, siendo la temperatura sobre la cual no es posible licuar un gas dado y es la presión mínima requerida para licuar un gas en su temperatura crítica. Juntos ellos definen el punto crítico de un fluido sobre el cual no existe una distinción entre las fases líquida y gaseosa de un fluido dado.
Los datos de presión-volumen-temperatura (PVT) para gases reales varían de un gas puro a otro. Sin embargo, cuando los factores de compresibilidad de varios gases de un solo componente se grafican en contra de la presión junto con isotermas de temperatura, muchos de los gráficos exhiben similares formas de isotermas.
Para obtener un gráfico generalizado que pueda ser usado para muchos diferentes gases, la presión y temperatura reducidas, y , se utilizan para normalizar los datos del factor de compresibilidad. La figura mostrada es un ejemplo de un gráfico de factor de compresibilidad generalizado derivado de cientos de datos experimentales PVT de 10 gases puros, que fueron metano, etano, eteno, propano, n-butano, i-pentano, n-hexano, nitrógeno, dióxido de carbono y vapor.
Existen gráficos de factor de compresibilidad generalizados más detallados basados en tantos como 25 o más gases puros diferentes, tales como los gráficos Nelson-Obert graphs. Dichos gráficos se dice que tienen una precisión dentro del 1-2 por ciento para valores de mayores que 0.6 y dentro del 4-6 por ciento para valores de entre 0.3-0.6.
Los gráficos de factor de compresibilidad generalizados pueden ser considerablemente erróneos para gases fuertemente polares, los cuales son gases para los que los centros de carga positiva y negativa no coinciden. En tales casos, el estimado de puede ser erróneo del 15-20 por ciento.
Los gases cuánticos hidrógeno, helio y neón no se ajustan al comportamiento de estados correspondientes y la presión y temperatura reducidas para esos tres gases deberían ser redefinidas de la siguiente forma para mejorar la precisión al predecir sus factores de compresibilidad cuando se utilizan los gráficos generalizados:
y
donde las temperaturas están en kelvin y las presiones en atmósferas.[4]
Modelos teóricos
La ecuación del virial es especialmente útil para describir las causas de la no-idealidad a nivel molecular (muy pocos gases son monoatómicos) ya que se deriva directamente de la mecánica estadística:
donde los coeficientes en el numerador se conocen como coeficientes viriales y son funciones de la temperatura.
Los coeficientes viriales tienen en cuenta las interacciones entre grupos sucesivamente más grandes de moléculas. Por ejemplo, toma en cuenta interacciones entre pares, toma en cuenta interacciones entre tres moléculas de gas, y así sucesivamente. Debido a que las interacciones entre grandes números de moléculas son raros, la ecuación del virial es usualmente truncada después del tercer término.[5]
Valores experimentales
Es extremadamente difícil generalizar a qué valores de presión o temperatura se vuelve importante la desviación del comportamiento de gas ideal. Como regla general, la ley de los gases ideales es razonablemente precisa hasta una presión de alrededor de 2 atmósferas, e incluso mayor para moléculas pequeñas no asociantes. Por ejemplo para el clorometano, una molécula altamente polar y por tanto con fuerzas intermoleculares significativas, el valor experimental para el factor de compresibilidad es de a una presión de 10 atm y una temperatura de 100 °C.[6] Para el aire (pequeñas moléculas no polares) en aproximadamente las mismas condiciones, el factor de compresibilidad es de solo (véase la tabla debajo para 10 bars, 400 K).
Compresibilidad del aire
El aire normal se comprende en números crudos de alrededor de 80 por ciento de nitrógeno N2 y 20 por ciento de oxígeno O2. Ambas moléculas son pequeñas y no polares (y por tanto, no asociantes). Se puede por tanto esperar que el comportamiento del aire dentro de rangos amplios de temperatura y presión pueda ser aproximado con razonable precisión como el de un gas ideal. Los valores experimentales para el factor de compresibilidad confirman esto.
- Z para el aire como función de la presión 1-500 bar
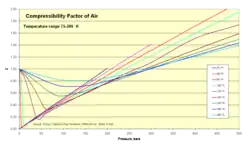 Isotermas a 75-200 K
Isotermas a 75-200 K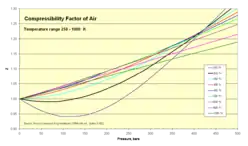 Isotermas a 250-1000 K
Isotermas a 250-1000 K
| Presión, bar (absoluta) | ||||||||||||||
| Temp, K | 1 | 5 | 10 | 20 | 40 | 60 | 80 | 100 | 150 | 200 | 250 | 300 | 400 | 500 |
| 75 | 0.0052 | 0.0260 | 0.0519 | 0.1036 | 0.2063 | 0.3082 | 0.4094 | 0.5099 | 0.7581 | 1.0125 | ||||
| 80 | 0.0250 | 0.0499 | 0.0995 | 0.1981 | 0.2958 | 0.3927 | 0.4887 | 0.7258 | 0.9588 | 1.1931 | 1.4139 | |||
| 90 | 0.9764 | 0.0236 | 0.0453 | 0.0940 | 0.1866 | 0.2781 | 0.3686 | 0.4681 | 0.6779 | 0.8929 | 1.1098 | 1.3110 | 1.7161 | 2.1105 |
| 100 | 0.9797 | 0.8872 | 0.0453 | 0.0900 | 0.1782 | 0.2635 | 0.3498 | 0.4337 | 0.6386 | 0.8377 | 1.0395 | 1.2227 | 1.5937 | 1.9536 |
| 120 | 0.9880 | 0.9373 | 0.8860 | 0.6730 | 0.1778 | 0.2557 | 0.3371 | 0.4132 | 0.5964 | 0.7720 | 0.9530 | 1.1076 | 1.5091 | 1.7366 |
| 140 | 0.9927 | 0.9614 | 0.9205 | 0.8297 | 0.5856 | 0.3313 | 0.3737 | 0.4340 | 0.5909 | 0.7699 | 0.9114 | 1.0393 | 1.3202 | 1.5903 |
| 160 | 0.9951 | 0.9748 | 0.9489 | 0.8954 | 0.7803 | 0.6603 | 0.5696 | 0.5489 | 0.6340 | 0.7564 | 0.8840 | 1.0105 | 1.2585 | 1.4970 |
| 180 | 0.9967 | 0.9832 | 0.9660 | 0.9314 | 0.8625 | 0.7977 | 0.7432 | 0.7084 | 0.7180 | 0.7986 | 0.9000 | 1.0068 | 1.2232 | 1.4361 |
| 200 | 0.9978 | 0.9886 | 0.9767 | 0.9539 | 0.9100 | 0.8701 | 0.8374 | 0.8142 | 0.8061 | 0.8549 | 0.9311 | 1.0185 | 1.2054 | 1.3944 |
| 250 | 0.9992 | 0.9957 | 0.9911 | 0.9822 | 0.9671 | 0.9549 | 0.9463 | 0.9411 | 0.9450 | 0.9713 | 1.0152 | 1.0702 | 1.1990 | 1.3392 |
| 300 | 0.9999 | 0.9987 | 0.9974 | 0.9950 | 0.9917 | 0.9901 | 0.9903 | 0.9930 | 1.0074 | 1.0326 | 1.0669 | 1.1089 | 1.2073 | 1.3163 |
| 350 | 1.0000 | 1.0002 | 1.0004 | 1.0014 | 1.0038 | 1.0075 | 1.0121 | 1.0183 | 1.0377 | 1.0635 | 1.0947 | 1.1303 | 1.2116 | 1.3015 |
| 400 | 1.0002 | 1.0012 | 1.0025 | 1.0046 | 1.0100 | 1.0159 | 1.0229 | 1.0312 | 1.0533 | 1.0795 | 1.1087 | 1.1411 | 1.2117 | 1.2890 |
| 450 | 1.0003 | 1.0016 | 1.0034 | 1.0063 | 1.0133 | 1.0210 | 1.0287 | 1.0374 | 1.0614 | 1.0913 | 1.1183 | 1.1463 | 1.2090 | 1.2778 |
| 500 | 1.0003 | 1.0020 | 1.0034 | 1.0074 | 1.0151 | 1.0234 | 1.0323 | 1.0410 | 1.0650 | 1.0913 | 1.1183 | 1.1463 | 1.2051 | 1.2667 |
| 600 | 1.0004 | 1.0022 | 1.0039 | 1.0081 | 1.0164 | 1.0253 | 1.0340 | 1.0434 | 1.0678 | 1.0920 | 1.1172 | 1.1427 | 1.1947 | 1.2475 |
| 800 | 1.0004 | 1.0020 | 1.0038 | 1.0077 | 1.0157 | 1.0240 | 1.0321 | 1.0408 | 1.0621 | 1.0844 | 1.1061 | 1.1283 | 1.1720 | 1.2150 |
| 1000 | 1.0004 | 1.0018 | 1.0037 | 1.0068 | 1.0142 | 1.0215 | 1.0290 | 1.0365 | 1.0556 | 1.0744 | 1.0948 | 1.1131 | 1.1515 | 1.1889 |
Fuente: Perry's chemical engineers' handbook (6a edición). MCGraw-Hill. 1984. ISBN 0-07-049479-7. (tabla 3-162). Los valores de son calculados a partir de valores de presión, volumen (o densidad), y temperatura en Vassernan, Kazavchinskii, y Rabinovich, Thermophysical Properties of Air and Air Components; Moscú, Naúka, 1966, y NBS-NSF Trans. TT 70-50095, 1971: y Vassernan y Rabinovich, Thermophysical Properties of Liquid Air and Its Component, Moscú, 1968, y NBS-NSF Trans. 69-55092, 1970.
Referencias
- (en inglés) Propiedades de los gases naturales Archivado el 6 de febrero de 2011 en Wayback Machine. Incluye un gráfico de factores de compresibilidad contra presión reducida y temperatura reducida (en la última página del documento PDF) Consultado el 7 de marzo de 2013.
- Zucker, Robert D. and Biblarz, Oscar (2002). Fundamentals of Gas Dynamics (2a edición). Wiley Books. ISBN 0-471-05967-6. p. 327
- McQuarrie, Donald A.; Simon, John D. (1999). Molecular Thermodynamics (en inglés). Ilustrada. University Science Books. p. 55. ISBN 9781891389054. Consultado el 7 de marzo de 2013.
- Rao, Y. V. C. (1997). Chemical Engineering Thermodynamics (en inglés). Universities Press. p. 63. ISBN 9788173710483. Consultado el 7 de marzo de 2013.
- Smith, J. M.; Van Ness, H. C.; Abbott, M. M. (2005). Introduction to chemical engineering thermodynamics (en inglés). Ilustrada (7a edición). McGraw-Hill. p. 73. ISBN 9780073104454.
- Perry's chemical engineers' handbook (6a edición). MCGraw-Hill. 1984. ISBN 0-07-049479-7. pp. 3-268
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Factor de compresibilidad.
Wikimedia Commons alberga una categoría multimedia sobre Factor de compresibilidad.- (en inglés) Compressibility factor (gases) Artículo en Citizendium.
- (en inglés) Gases Reales incluye una discusión de factores de compresibilidad.
- (en inglés) Calculador de factores de compresibilidad en EnggCyclopedia basado en propiedades críticas
- (en inglés) Calculador de factores de compresibilidad en EnggCyclopedia para gas natural
- Esta obra contiene una traducción derivada de «Compressibility factor» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.