Faloidina
La faloidina es un heptapéptido bicíclico tóxico, presente en diferentes setas pertenecientes a la familia Amanitaceae. Concretamente, está presente en el género Amanita, dentro del cual se encuentran la mayor parte de las setas que son tóxicas para los humanos, destacando por su toxicidad Amanita phalloides, Amanita virosa y Amanita verna. La ingesta de estas setas produce efectos tóxicos a nivel renal, hepático y central por su contenido en amatoxinas, falotoxinas y virotoxinas.[1]
Tiene una elevada toxicidad pero a diferencia de las amatoxinas, no se absorbe por vía oral por lo que apenas contribuye a la toxicidad por setas del género Amanita.[1]
Fue identificada por primera vez por Wieland en 1937 en A. phalloides.[1]
Estructura
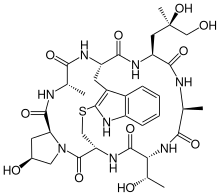
La faloidina es un compuesto cíclico formado por siete aminoácidos. Un grupo tioéter conecta las cadenas laterales de dos aminoácidos en el lado contrario del anillo, que son triptófano y cisteína, lo que se relaciona con el efecto citotóxico de la molécula.[2][1]
Pertenece al grupo de falotoxinas, un grupo formado por al menos siete componentes diferentes con estructura heptapeptídica bicíclica, siendo estos: faloidina, faloina, profalina, falisina, falacina, falacidina y falasacina.[3]
Propiedades fisicoquímicas
| Nomenclatura sistemática (IUPAC) | (1S,14R,18S,20S,23S,28S,31S,34R)-28-[(2R)-2,3-dihidroxi-2-metilpropil]-18-hidroxi-34-[(1S)-1-hidroxiethil]-23,31-dimetil-12-tia-10,16,22,25,27,30,33,36-octazapentaciclo[12.11.11.03,11.04,9.016,20]hexatriaconta-3(11),4,6,8-tetraene-15,21,24,26,29,32,35-heptona |
|---|---|
| Fórmula molecular | C35H48N8O11S |
| Masa molar | 788,97g/mol |
| Solubilidad (logP) | -5,58 |
| Solubilidad en agua | 500mg/L |
| Número CAS | 17466-45- |
Mecanismo de acción
Las falotoxinas se unen fuertemente a las estructuras que contienen filamentos, en particular tienen gran afinidad por filamentos de actina (F-actina) de las células. No tiene gran afinidad por los monómeros de actina (G-actina). Afecta al equilibrio entre filamentos y monómeros hacia filamentos, disminuyendo la concentración crítica para la polimerización por una disminución en la constante de disociación de las subunidades de actina.[3][1][4][5]
Por tanto, evita la despolimerización de los filamentos de actina y afecta al equilibrio entre monómeros y filamentos de actina, impidiendo el correcto funcionamiento del citoesqueleto de las células.[5][4][3][1]
La estequiométrica que sigue la faloidina en su unión a los filamentos de actina es de 1:1 o 1:2, lo que quiere decir que una molécula de faloidina es capaz de unir uno o dos promotores de actina.[5]
Para ejercer su actividad debe ser administrada por vía parenteral, dado que no se absorbe por vía oral. Utiliza un transportador de ácidos orgánicos (mayoritariamente para ácidos biliares) para ser introducido dentro de los hepatocitos (este también es capaz de transportar antamanida y somatostatinas cíclicas). Concretamente, utiliza el receptor Oatp 1b1/3 (humanos) o Oatp 1b2 (roedores), que es un péptido transportador de aniones orgánicos.[6] Se trata de un transporte activo secundario dependiente de sodio.[4]
Varios estudios señalan que la faloidina no es un compuesto tóxico per se, sino que forma un metabolito activo in situ en los hepatocitos, que es el causante del daño. Además, la citotoxicidad está asociada al enlace tioéter entre las moléculas de azufre de los aminoácidos cisteína y triptófano.[4]
Absorción, distribución y eliminación
Existen diferencias de biodisponibilidad dependiendo de la edad. En un estudio, tanto in vitro como in vivo, se comprobó que las ratas jóvenes alcanzaban mayores concentraciones posiblemente por una menor eliminación, pero sorprendentemente tenían también una mayor tolerancia a los efectos tóxicos. Por ello no se encontró relación entre la concentración y la toxicidad.[6]
El órgano que ataca, de forma muy selectiva, es el hígado. Para llegar a los hepatocitos utiliza un sistema de transporte transporte multiespecífico de ácidos biliares Oatp 1b2 en roedores y Oatp 1b1 y 1b3 en humanos. Es un transporte activo de ácidos orgánicos dependiente de sodio activado por voltaje. Una vez dentro del hepatocito, se alcanza una alta concentración de faloidina que se explica por una extremadamente baja constante de disociación.[6]
Esta absorción puede ser limitada por las silimarinas del cardo mariano, que en este caso protegen el hígado compitiendo por el transporte disminuyendo así su absorción.[7]
Toxicidad
Cuando se ingiere por vía oral, no es absorbida por lo que no puede causar el efecto tóxico hepáticos, que es el más importante de esta toxina. Sin embargo, cuando se produce una intoxicación por alguna seta de la especie Amanita, se produce un cuadro gastrointestinal similar a una gastroenteritis viral, el cual se asocia a la presencia de faloidina y sus metabolitos activos.[1][3]
Los efectos gastrointestinales se producen de manera abrupta, entre 6 y 24 horas después de la ingestión. Los más comunes son náuseas, vómitos y diarrea (en ocasiones con sangre), aunque también se puede producir dolor abdominal y hematuria. Esta fase generalmente dura entre 12 y 36 horas y durante ella también se pueden producir otros síntomas como fiebre, taquicardia, desórdenes metabólicos, deshidratación y desequilibrio electrolítico.[3]
Cuando se administra por vía parenteral, afecta a los filamentos de actina y desencadena la formación de vacuolas en los hepatocitos, acompañado de un fallo en la excreción biliar y, finalmente, hemorragia hepática. El grado de sangrado depende de la dosis de faloidina administrada y de la perfusión.
El sangrado se debe a la formación de vacuolas en los hepatocitos, cuya muerte es calcio-dependiente. Con el sangrado, se produce una pérdida rápida de K+. Mg2+ y Ca2+ intracelular y de enzimas lisosomales. La liberación de estas enzimas lisosomales probablemente sea la responsable de los efectos extrahepáticos, junto con la liberación de productos de degradación del hígado dañado.[4]
Cuando se administra una dosis letal de faloidina a una rata, esta muere en menos de 2-3 horas con un shock hemorrágico, debido a la disminución de la perfusión de sangre desde el tracto gastrointestinal hacia el corazón. Estos efectos no se producen cuando la faloidina es administrada por vía oral, lo que demuestra que no se absorbe por vía oral. A dosis por debajo de las letales produce colestasis canalicular debido a su acción sobre la actina.[4]
En hepatocitos tratados con faloidina, se puede observar la formación de vacuolas y protrusiones en la superficie de las células. Las vacuolas que se forman son largas, cavernosas y con ondulaciones. La formación de estas vacuolas siempre está acompañada de movimientos anormales, incluyendo movimientos contráctiles sostenidos, formaciones de vacuolas complementarias y contracciones hemicanaliculares.[8][9]
Los efectos en la formación de vacuolas y formación de protrusiones son dosis-dependientes.
A pesar de todos los cambios morfológicos, no se ve afectada la salida del volumen de agua intracelular, potasio, ATP y urea, mientras la ácido láctico deshidrogenasa es expulsada en un valor muy pequeño. Esto quiere decir que los hepatocitos tratados con faloidina preservan su función.[8][9]
A nivel de la excreción de triglicéridos, se ve afectada de manera dosis-dependiente. Se acompaña de una acumulación de triglicéridos dentro de los hepatocitos. Probablemente debido a que la excreción de triglicéridos requiere la síntesis de proteínas, y esta función se ve afectada cuando se administra faloidina.[8]
Además, también afecta a nivel de la motilidad del conducto biliar, produciendo una gran prolongación de la contractilidad. En un tratamiento agudo con faloidina, el conducto biliar presenta formas irregulares y prolongación de los filamentos de actina en el canalículo.
Administrado por vía endovenosa el primer efecto que se ve al añadir la toxina es la colestasis, por ello es un prototipo de agente colestático . Esta disminución del flujo de bilis es proporcional a la disminución de excreción de ácidos biliares.[10]
Diferentes valores de DL50 están representados en la tabla:
| Organismo | Vía de administración | Dosis Letal 50 (DL50) |
|---|---|---|
| Perro | Intravenosa | >10mg/kg |
| Ratón | Intraperitoneal | 2mg/kg |
| Rata | Intraperitoneal | 1mg/kg |
Tratamiento
Cuando se ingieren setas del género Amanita y no han pasado aún más de 5-6 horas desde la ingesta, se puede administrar carbón activado, que adsorbe en su superficie las diferentes toxinas y evitará su absorción y/o efectos, o hacer un lavado gástrico. Esta medida está contraindicada en el caso de pacientes que estén inconscientes o conscientes pero hayan perdido el reflejo protector de las vías respiratorias.[1] Además, son importantes las medidas de estabilización, para restablecer el equilibrio de electrolitos y fluidos que se puede haber perdido durante la fase gastrointestinal.[1]
En cuanto a la toxicidad por vía intravenosa, se han desarrollado varios tratamientos que disminuyen su toxicidad.
El tratamiento con espironolactona sola o combinada con dihidroestreptomicina, nifuroxazina y levadura ha demostrado disminuir entre un 30 y un 45% la mortalidad en ratones.[11]
Aparentemente, dibenzotiolina, al igual que otros componentes estabilizadores, ejerce una acción protectora frente al daño tóxico que puede producir la faloidina mediante una estabilización inespecífica de las membranas plasmáticas, probablemente por la liberación de radicales tiol.[12]
La administración de somatostatina es un método que se utiliza para el tratamiento de lesiones vasculares hepáticas en humanos y otros mamíferos. Cuando se administra por vía parenteral en ratas 30 minutos antes y 30 minutos después de una dosis de faloidina, disminuye las lesiones hepáticas que ésta produce, reduciendo la mortalidad al menos un 20%.[13]
Identificación
Para hacer una determinación rápida a un paciente, o saber si la muestra del hongo ingerido contiene amatoxinas en general, se puede hacer la Prueba de Meixner, una reacción con lignina que forma un polímero azul (catalizada por ácido concentrado). Es una prueba sencilla que se puede hacer tomando una muestra y depositándola en un periódico (contiene lignina) hasta que se seque y añadiendo una gota de ácido clorhídrico. Cabe destacar que tiene varias interferencias con compuestos derivados de hidroxilo triptamina que dan falsos positivos, como la psilocina.
También se puede analizar en orina hasta máximo las 36 horas post ingestión mediante radionmunoensayo o inmunosorción.[3]
Para evaluar la concentración de estas toxinas en setas se puede utilizar HPLC en fase inversa (RP-HPLC), electroforesis capilar acoplada a espectrometrías de masas, cromatografía líquida acoplada a espectrometría de masas, cromatografía líquida o tándem de ionización de electrospray acoplado a espectrometría de masas o cromatografía líquida.
El método más utilizado para la identificación es la cromatografía líquida de alto rendimiento en fase inversa, pero la cromatografía líquida acoplada a espectrometría de masas aporta los resultados más reales y sensibles.[3]
Aplicaciones prácticas
Por su toxicidad selectiva sobre los hepatocitos, se utilizaba vía endovenosa como modelo para evaluar la eficacia de compuestos hepatoprotectores. Hoy no se considera de utilidad por la elevada especificidad que presenta su mecanismo de acción ya que un modelo para probar protectores generales del hígado debería tener un mecanismo tóxico general.[4]
Por su mecanismo de acción, la faloidina se utiliza como sonda conjugada con un fluoróforo (es capaz de conjugarse con diversos fluoróforos) en estudios de inmunofluorescencia y en técnicas de identificación y separación de proteínas como Western Blot, para realizar estudios donde se deba visualizar el citoesqueleto,[8] introducida en células previamente permeabilizadas.[4] Esto es posible debido a que, por su propio mecanismo de acción, tiene una gran afinidad por la actina-F. Dicha unión es bloqueable por la nebulina, una proteína de los filamentos finos del músculo esquelético.[10]
Existe gran variedad de conjugados de fluoróforos con faloidina por ejemplo la rodamina [14] que forma la llamada RT-faloidina. Se utilizan ampliamente en estudios de formación de ramificaciones de actina por el complejo Arp2/3.
Se han realizado estudios del mecanismo de entrada de faloidina en la célula, especialmente en células ciliadas ya que no es capaz de entrar en todas las células con la misma facilidad.
Microscopía

Las capacidades de la faloidina de unir específicamente microfilamentos y de estabilizarlos la facultan para ensayos de microscopía empleando una variante marcada fluorescentemente con un fluorocromo; el resultado, una vez permeada la muestra in vitro con la sustancia, es apto para microscopía de fluorescencia y microscopía confocal. De hecho, se ha relacionado la fluorescencia medible con la cantidad de filamentos de actina presentes, empleando cantidades saturantes de faloidina
Referencias
- Tavassoli, Milad (2019). «Toxicological profile of Amanita virosa- A narrative review.». Toxicology Reports.
- Gosselin, R.E. «Clinical Toxicology of Commercial Products». Baltimore.
- Garcia, Juliana (2015). «Amanita phalloides poisoning: Mechanisms of toxicity and treatment.». Food and Chemical Toxicology.
- Frimmer, Max (1987). «What we have learned about phalloidin». Toxicology Letters.
- Cooper, John A. (1987). «Effects of Cytochalasin and phalloidin on Actin». J Cell Bio.
- «Foreign compound metabolism in mammals, a review of the literature published between 1970 and 1971». The Chemical Society. 1972.
- Catalina, M.V. «Toxicidad hepática por ingesta de setas: curso clínico y nuevas perspectivas de tratamiento». Servicio de aparato digestivo, Hospital General Universitario Gregorio Marañón.
- Sumio Watanabe, M. «Acute phalloidin toxicity in living hepatocites. Evidence for a possible disturbance in membrane flow and for multiple functions in actin and in the liver cell.». Toxicity.
- Prentki, Marc. «Actin microfilamnets, cell shape and secretory processes in isolated rat hepatocytes. Effects of phalloidin and Cytochalasin.». JCB Home.
- Elias, E. «Phalloidin-induced cholestasis: a microfilament-mediated change in junctional complex permeability.». Hepatology.
- Larcan, A (1975). «agressologie». Treatment of phalloidin poisoning. p. 307.
- Tongiani R Et al.; Protective effect of a new thiolic compound (dibenzothioline) on the hepatocytes of phalloidin and alpha-amanitin poisoned rats. A quantitative cytochemical evaluation by microinterferometry drugs exp clin res 8(1) 61 (1982)
- Szabo S, usadel kh; Use of somatostatin in the prevention and cure of vascular, membrane, or organ lesions; Us patent number 4366148 12/28/82 (Brigham and women's hospital)
- Termofisher, Invitrogen™ Rhodamine Phalloidin, acceso el 10 noviembre de 2019. Disponible en https://www.thermofisher.com/order/catalog/product/R415#/R415