Hemateína
Hemateina o haemateina es un derivado oxidado de hematoxilina, que se utiliza en la tintura. Haemateina no debe confundirse con la hematina, que es un pigmento de color marrón que contiene hierro negro formado por la descomposición de la hemoglobina. En el Índice de Color (pero ningún otro lugar), haemateina se llama haematina, una palabra confusa que erróneamente implica que el compuesto es una amina.
| Hemateína | ||
|---|---|---|
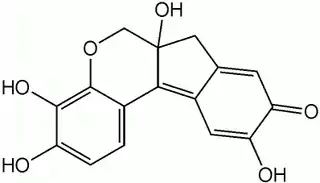 | ||
| Nombre IUPAC | ||
| 3,4,6a,10-Tetrahydroxy-6,7-dihydroindeno[2,1-c]chromen-9-one | ||
| General | ||
| Otros nombres | Haemateina; Haematein | |
| Fórmula molecular |
C 16H 12O 6 | |
| Identificadores | ||
| Número CAS | 475-25-2[1] | |
| ChEBI | 90116 | |
| ChEMBL | 1360563 | |
| ChemSpider | 9732 | |
| PubChem | 10138 | |
| UNII | 88Q1SYD10B | |
|
C1C2=CC(=O)C(=CC2=C3C1(COC4=C3C=CC(=C4O)O)O)O
| ||
| Propiedades físicas | ||
| Masa molar | 300,26 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Hemateína exhibe propiedades indicadoras similares, siendo azul y menos soluble en condiciones alcalinas acuosas, y rojo y más solubles en condiciones ácidas alcohólicas. Haemateina disuelta reacciona lentamente con el oxígeno atmosférico, produciendo productos que no son útiles.
En soluciones ácidas, complejos de hemateína con metales (por lo general de aluminio o de hierro, como también de cromo, zirconio y varios otros) se utilizan como manchas biológicas. Aluminio-haematein (haemalum) es la mancha de "rutina" para los núcleos celulares en secciones de tejidos humanos y otros animales. Manchas de metal-haematein están disponibles también para objetos distintos núcleos, incluyendo las vainas de mielina de las fibras nerviosas y diversos orgánulos citoplasmáticos. El color de los objetos manchados depende de la sal utilizada. Complejos de aluminio-haematein son generalmente de color azul, mientras que los complejos férricos son de color azul muy oscuro o negro.
Complejos de aluminio-haematein (haemalum) se unen a la cromatina de los núcleos de las células. Aunque los métodos de tinción haemalum han estado en uso desde la década de 1860, la identidad química de la sustancia o sustancias que se unen el complejo colorante-metal aún no sabe con certeza. Algunas investigaciones histoquímicas indican claramente que un complejo de aluminio-haematein catiónico es atraído a los aniones de fosfato de ADN. Otros implican los residuos de arginina de las histonas nucleares como el sustrato de la tinción nuclear por haemalum.[2]
Las estructuras que se tiñen con el aluminio-hemateína (haemalum) a menudo se dice que son basófilos, pero el mecanismo de tinción no es tan simple como para los colorantes básicos (catiónico) con moléculas más pequeñas. Verdaderamente las estructuras basófilas son los que contienen ácidos nucleicos u otros polianiones tales como glicosaminoglicanos de la matriz extracelular o glicoproteínas ácidas en muchos tipos de moco. Tal como se utiliza por lo general, las manchas de aluminio-hemateína sólo la cromatina nuclear y algunos otros materiales, tales como gránulos de queratohialina y depósitos calcificados. Soluciones muy diluidas de aluminio-haemateina, utilizados a pH 3,2 (mayor de lo que es habitual para la tinción), contienen un complejo catiónico de tinte de metal y poco a poco se manchan los ácidos nucleicos.[3] Las soluciones de haemalum utilizadas para la tinción de rutina están más concentrados y más ácidas (pH 2-2,5) y son capaces de teñir los núcleos después de la extracción química o enzimática de ADN y ARN a partir del tejido.[4]
Referencias
- Número CAS
- Puchtler, H., Meloan, S.N., Waldrop, F.S. (1986). «Application of current chemical concepts to metal-haematein and -brazilein stains». Histochemistry 85 (5): 353-364. PMID 2430916. doi:10.1007/BF00982665.
- Bettinger, C. & Zimmermann, H.W. (1991). «New investigations on hematoxylin, hematein, and hematein-aluminium complexes. 2. Hematein-aluminium complexes and hemalum staining». Histochemistry 96 (3): 215-228. PMID 1717413. doi:10.1007/BF00271540.
- Lillie, R.D., Donaldson, P.T. & Pizzolato, P. (1976). «The effect of graded 60C nitric acid extraction and of deoxyribonuclease digestion on nuclear staining by metachrome mordant dye metal salt mixtures». Histochemistry 46 (4): 297-306. PMID 57109. doi:10.1007/BF02464419.
Enlaces externos
- Esta obra contiene una traducción derivada de «Hematein» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.