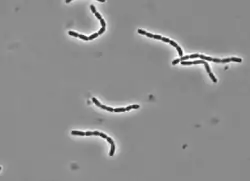
Lacticaseibacillus rhamnosus
Lacticaseibacillus rhamnosus (anteriormente Lactobacillus rhamnosus)[1] es una bacteria que originalmente fue considerada como una subespecie de L. casei, pero investigaciones genéticas posteriores permitieron considerarla como una especie separada. Algunas cepas de L. rhamnosus están siendo utilizadas como probióticos. Esta especie es a veces utilizada en la fabricación de yogur y productos lácteos como leche fermentada y pasteurizada y queso semiduro. Se han realizado estudios sobre sus efectos in vivo. Normalmente es considerada como un organismo beneficioso, aunque se ha descubierto que L. rhamnosus puede ser patógeno en circunstancias raras, principalmente en situaciones de sistema inmunitario debilitado.[2]
| Lacticaseibacillus rhamnosus | ||
|---|---|---|
 | ||
| Taxonomía | ||
| Dominio: | Bacteria | |
| División: | Firmicutes | |
| Clase: | Bacilli | |
| Orden: | Lactobacillales | |
| Familia: | Lactobacillaceae | |
| Género: | Lacticaseibacillus | |
| Especie: |
L. rhamnosus (Hansen 1968) Zheng et al. 2020 | |
| Sinonimia | ||
Lactobacillus rhamnosus (Hansen 1968) Collins et al. 1989 | ||
Lacticaseibacillus rhamnosus GG
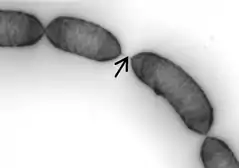
Lacticaseibacillus rhamnosus GG es una cepa de L. rhamnosus que fue aislada en 1983 del tracto intestinal de un ser humano sano. Patentado el 17 de abril de 1985, por Sherwood Gorbach y Barry Goldin el 'GG' del nombre deriva de las iniciales de sus apellidos.[3] La patente se refiere a una cepa de "L. acidophilus GG" con número 53103 en la American Type Culture Collection (ATCC). Más tarde fue reclasificada como una cepa de L. rhamnosus. La patente dice que la cepa L. rhamnosus GG (ATCC 53103) es estable en ácido -y bilis-, tiene una avidez grande para las células mucosas del intestino humano, y produce ácido láctico. Desde el descubrimiento de la cepa L. rhamnosus GG (ATCC 53103), han sido estudiados extensamente sus beneficios para la salud y actualmente la cepa L. rhamnosus GG (ATCC 53103) es la bacteria probiótica más estudiada del mundo con más de 800 estudios científicos.
La secuencia de genoma de Lacticaseibacillus rhamnosus GG (ATCC 53103) ha sido resuelta. [4] [5]
Investigaciones médicas y uso
Aunque Lacticaseibacillus rhamnosus GG (ATCC 53103) es capaz de sobrevivir en las condiciones ácidas y la presencia de bilis en el estómago e intestino, [6] esta bacteria coloniza el tracto digestivo y equilibra la microbiota intestinal. Existen evidencias que sugieren que Lactobacillus rhamnosus probablemente puede ser un habitante transitorio, y no autóctono.[7] De todas formas, es considerado un probiótico útil para el tratamiento de varias enfermedades, ya que trabaja a varios niveles. Aun así, la mayoría de los mecanismos moleculares no son conocidos.
Alergia de cacahuete
Las investigaciones están mostrando que L. rhamnosus usado como probiótico podría parar reacciones alérgicas a cacahuetes en el 80% de los niños.[8]
Diarrea
Lacticaseibacillus rhamnosus GG ha mostrado beneficios en la prevención del rotavirus diarreico en niños. Se ha mostrado tanto la prevención como el tratamiento de varios tipos de diarrea en niños y en adultos.[9] [10] [11] [12]
Infecciones de vía respiratoria
L. rhamnosus GG puede parar infecciones de vía respiratoria en niños.[13] [14]
Dermatitis atópica, eccema
Lacticaseibacillus rhamnosus GG también ha mostrado potencial en el tratamiento y prevención primaria de la dermatitis atópica, pero los resultados de las pruebas de intervención han sido variados.[15] Una prueba clínica con un seguimiento de siete años muestra que L. rhamnosus GG es útil en la prevención de dermatitis atópica en niños con alto riesgo de alergia.[16] [17]
Tracto urogenital
Los efectos de salud clínicos de L. rhamnosus GG han sido ampliamente estudiados. Tanto L. rhamnosus GG como L. rhamnosus GR-1 parece que pueden proteger el tracto urogenital ya que excretan biosurfactantes que inhibirían la adhesión de patógenos vaginales y urinarios.
Permeabilidad de tracto intestinal
Se ha mostrado que L. rhamnosus puede reducir la permeabilidad intestinal en niños que sufren el síndrome del intestino irritable,[18] y también se ha mostrado que puede contrarrestar la permeabilidad intestinal relacionada con el alcohol.[19] [20]
Transporte gastrointestinal de VRE
En 2005, L. rhamnosus GG fue utilizado exitosamente para tratar el transporte gastrointestinal de Enterococcus resistente a vancomicina (VRE) en pacientes renales. [21]
Síndrome de Asperger y Trastorno por Déficit de Atención e Hiperactividad (TDAH)
Un estudio de 2015 concluyó que la administración temprana de suplementos probióticos puede reducir el riesgo de desarrollo de trastornos neuropsiquiátricos más adelante en la infancia. Los bebés en el estudio longitudinal fueron aleatorizados para recibir L. Rhamnosus GG (ATCC 53103) o placebo durante sus primeros seis meses y luego fueron seguidos durante 13 años. A la edad de 13 años, el 17.1% (6/35) de los niños en el grupo placebo fueron diagnosticados con síndrome de Asperger o TDAH, mientras que ninguno de los niños que recibieron L. rhamnosus fue diagnosticado (0/40). [22]
Ansiedad
Investigaciones publicadas en el Proceedings of the National Academy of Sciences el 29 de agosto de 2011 informaban que esta bacteria puede tener efectos sobre los receptores del neurotransmisor GABA. Ratones que fueron alimentados con L. rhamnosus mostraron menos ansiedad y tuvieron niveles diferentes de sensores químicos del cerebro y hormonas del estrés.[23]
Pérdida de peso
Investigaciones publicadas} en British Journal of Nutrition en 2013 sugieren que Lacticaseibacillus rhamnosus puede aumentar la pérdida de peso en mujeres que se están realizando una dieta. La investigación fue comenzada después de que varios estudios mostraran que las bacterias del intestino en individuos obesos difieren significativamente de aquellas en personas delgadas. Las mujeres en el estudio perdieron casi el doble de peso que el grupo placebo. Sin embargo, no se observó ninguna diferencia en hombres.[24]
Riesgos
El uso de L. rhamnosus GG como terapia probiótica ha sido relacionado con casos muy raros de sepsis en ciertos grupos de riesgo, principalmente personas con un sistema inmunitario debilitado y niños.[25] La ingestión de L. rhamnosus GG es, no obstante, considerada segura, y datos procedentes de Finlandia muestran que un crecimiento significativo en el consumo de L. rhamnosus GG en la población no ha conllevado un aumento en el número de casos de bacteriemia por Lactobacillus.[26]
Referencias
- Zheng, Jinshui; Wittouck, Stijn; Salvetti, Elisa; Franz, Charles M.A.P.; Harris, Hugh M.B.; Mattarelli, Paola; O’Toole, Paul W.; Pot, Bruno; Vandamme, Peter; Walter, Jens; Watanabe, Koichi; Wuyts, Sander; Felis, Giovanna E.; Gänzle, Michael G.; Lebeer, Sarah (1 de abril de 2020). «A taxonomic note on the genus Lactobacillus: Description of 23 novel genera, emended description of the genus Lactobacillus Beijerinck 1901, and union of Lactobacillaceae and Leuconostocaceae». International Journal of Systematic and Evolutionary Microbiology (en inglés) 70 (4): 2782-2858. PMID 32293557. doi:10.1099/ijsem.0.004107. Consultado el 5 de mayo de 2021.
- Avlami A, Kordossis T, Vrizidis N, Sipsas NV (2001). «Lactobacillus rhamnosus endocarditis complicating colonoscopy». J. Infect. 42 (4): 283-5. PMID 11545575. doi:10.1053/jinf.2001.0793.
- Silva M, Jacobus NV, Deneke C, Gorbach SL (1987). «Antimicrobial substance from a human Lactobacillus strain». Antimicrob. Agents Chemother. 31 (8): 1231-1233. PMID 3307619. doi:10.1128/aac.31.8.1231.
- Kankainen M; Paulin, L.; Tynkkynen, S.; von Ossowski, I.; Reunanen, J.; Partanen, P.; Satokari, R.; Vesterlund, S.; Hendrickx, A. P. A.; Lebeer, S.; De Keersmaecker, S. C. J.; Vanderleyden, J.; Hamalainen, T.; Laukkanen, S.; Salovuori, N.; Ritari, J.; Alatalo, E.; Korpela, R.; Mattila-Sandholm, T.; Lassig, A.; Hatakka, K.; Kinnunen, K. T.; Karjalainen, H.; Saxelin, M.; Laakso, K.; Surakka, A.; Palva, A.; Salusjarvi, T.; Auvinen, P.; De Vos, W. M.; et al. (2009). «Comparative genomic analysis of Lactobacillus rhamnosus GG reveals pili containing a human-mucus binding protein». roc Natl Acad Sci USA. P 106 (40): 17193-17198. PMID 19805152. doi:10.1073/pnas.0908876106.
- Morita H, Toh H, Oshima K, Murakami M, Taylor TD, Igimi S, Hattori M (2009). «Complete genome sequence of the probiotic Lactobacillus rhamnosus ATCC 53103». J. Bacteriol. 191 (24): 7630-7631. PMID 19820099. doi:10.1128/JB.01287-09.
- Conway PL, Gorbach SL, Goldin BR (January 1987). «Survival of lactic acid bacteria in the human stomach and adhesion to intestinal cells». Journal of Dairy Science 70 (1): 1-12. PMID 3106442. doi:10.3168/jds.S0022-0302(87)79974-3.
- Walter J (2008). «Ecological role of lactobacilli in the gastrointestinal tract: implications for fundamental and biomedical research». Applied and Environmental Microbiology 74 (16): 4985-96. PMC 2519286. PMID 18539818. doi:10.1128/AEM.00753-08.
- Scott, Sophie. «Peanut allergies: Australian study into probiotics offers hope for possible cure".». abc.net.au.
- Canani RB, Cirillo P, Terrin G, Cesarano L, Spagnuolo MI, De Vincenzo A, Albano F, Passariello A, De Marco G, Manguso F, Guarino A (August 2007). «Probiotics for treatment of acute diarrhoea in children: randomised clinical trial of five different preparations». BMJ 335 (7615): 340. PMC 1949444. PMID 17690340. doi:10.1136/bmj.39272.581736.55.
- Osterlund P, Ruotsalainen T, Korpela R, Saxelin M, Ollus A, Valta P, Kouri M, Elomaa I, Joensuu H (2007). «Lactobacillus supplementation for diarrhoea related to chemotherapy of colorectal cancer: a randomised study». British Journal of Cancer 97 (8): 1028-1034. PMC 2360429. PMID 17895895. doi:10.1038/sj.bjc.6603990.
- Guandalini S, Pensabene L, Zikri MA, Dias JA, Casali LG, Hoekstra H, Kolacek S, Massar K, Micetic-Turk D, Papadopoulou A, de Sousa JS, Sandhu B, Szajewska H, Weizman Z (2000). «Lactobacillus GG administered in oral rehydration solution to children with acute diarrhea: a multicenter European trial». Journal of Pediatric Gastroenterology and Nutrition 30 (1): 54-60. PMID 10630440. doi:10.1097/00005176-200001000-00018.
- Vanderhoof,Jon A.; et al. (1999). «LactobacillusGG in the prevention of antibiotic-associated diarrhea in children». The Journal of Pediatrics 135 (5): 564-568. Consultado el 15 de abril de 2012.
- Hojsak, I; Snovak N; Abdović S; Szajewska H; Mišak Z; Kolaček S (2009). «Lactobacillus GG in the prevention of gastrointestinal and respiratory tract infections in children who attend day care centers: A randomized, double-blind, placebo-controlled trial». Clin. Nutr. 29 (3): 312-316. PMID 19896252. doi:10.1016/j.clnu.2009.09.008.
- Hatakka, K; Savilahti E; Pönkä A; Meurman JH; Poussa T; Näse L; Saxelin M; Korpela R (2001). «Effect of long term consumption of probiotic milk on infections in children attending day care centres: double blind, randomised trial». BMJ. 322 (7238): 1327. PMC 32161. PMID 11387176. doi:10.1136/bmj.322.7298.1327.
- Boyle RJ, Bath-Hextall FJ, Leonardi-Bee J, Murrell DF, Tang ML (2009). «Probiotics for the treatment of eczema: a systematic review». Clin Exp Allergy. 39 (8): 1117-1119. PMID 19573037. doi:10.1111/j.1365-2222.2009.03305.x.
- Kalliomäki, M; Salminen S; Poussa T; Isolauri E (2007). «Probiotics during the first 7 years of life: a cumulative risk reduction of eczema in a randomized, placebo-controlled trial». J Allergy Clin Immunol. 119 (4): 1019-21. PMID 17289135. doi:10.1016/j.jaci.2006.12.608.
- Kalliomäki, M; Salminen S; Arvilommi H; Kero P; Koskinen P; Isolauri E (2001). «Probiotics in primary prevention of atopic disease: a randomised placebo-controlled trial». The Lancet 357 (9262): 1076-1079. PMID 11297958. doi:10.1016/S0140-6736(00)04259-8.
- Francavilla, R.; Miniello, V.; Magistà, AM.; De Canio, A.; Bucci, N.; Gagliardi, F.; Lionetti, E.; Castellaneta, S.; et al. (2010). «A randomized controlled trial of Lactobacillus GG in children with functional abdominal pain». Pediatrics. 126 (6): 1445-1452. PMID 21078735. doi:10.1542/peds.2010-0467.
- Wang, Y.; Liu, Y.; Sidhu, A.; Ma, Z.; McClain, C.; Feng, W. (2012). «Lactobacillus rhamnosus GG culture supernatant ameliorates acute alcohol-induced intestinal permeability and liver injury». Am J Physiol Gastrointest Liver Physiol. 303 (1): G32-41. PMID 22538402. doi:10.1152/ajpgi.00024.2012.
- Forsyth, CB.; Farhadi, A.; Jakate, SM.; Tang, Y.; Shaikh, M.; Keshavarzian, A. (2009). «Lactobacillus GG treatment ameliorates alcohol-induced intestinal oxidative stress, gut leakiness, and liver injury in a rat model of alcoholic steatohepatitis». Alcohol. 43 (2): 163-172. PMID 19251117. doi:10.1016/j.alcohol.2008.12.009.
- Manley KJ, Fraenkel MB, Mayall BC, Power DA (2007). «Probiotic treatment of vancomycin-resistant enterococci: a randomised controlled trial». Med J Aust. 186 (9): 454-457. PMID 17484706.
- Pärtty A, Kalliomäki M, Wacklin P, Salminen S, Isolauri E (June 2015). «A possible link between early probiotic intervention and the risk of neuropsychiatric disorders later in childhood: a randomized trial». Pediatric Research 77 (6): 823-828. PMID 25760553. doi:10.1038/pr.2015.51.
- Hesman T. (2011). «Genes & cells: Belly bacteria can boss the brain: Gut microbes lower stress hormones and anxiety in mice». Science News.
- British Journal of Nutrition,
- Gupta, V; Garg, R (2009). «Probiotics». Indian Journal of Medical Microbiology. 27 (3): 202-209. PMID 19584499. doi:10.4103/0255-0857.53201.=.
- Salminen, MK; Tynkkynen S; Rautelin H; Saxelin M; Vaara M; Ruutu P; Sarna S; Valtonen V; Järvinen A (2002). «Lactobacillus bacteremia during a rapid increase in probiotic use of Lactobacillus rhamnosus GG in Finland». Clin. Infect. Dis. 35 (10): 1155-1160. PMID 12410474. doi:10.1086/342912.
Enlaces externos
- Esta obra contiene una traducción parcial derivada de «Lactobacillus rhamnosus » de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.