Nimesulida
La nimesulida es un antiinflamatorio francamente COX-2 selectivo, con efectos analgésico y antipirético, clase o familia sulfonanilida. Está aprobado como indicación para el tratamiento del dolor agudo, la sintomatología de la osteoartritis y de la dismenorrea en adolescentes y en adultos, por arriba de los 12 años de edad. Debido al potencial riesgo de hepatotoxicidad, la nimesulida ha sido retirada del mercado en algunos países.[1]
| Nimesulida | ||
|---|---|---|
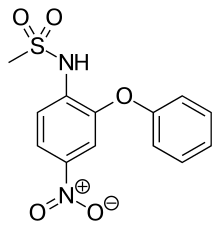 | ||
| Nombre (IUPAC) sistemático | ||
| N-(4-Nitro-2-fenoxifenil)metanesulfonamida | ||
| Identificadores | ||
| Número CAS | 51803-78-2 | |
| Código ATC | M01AX17 | |
| PubChem | 4495 | |
| Datos químicos | ||
| Fórmula | C13H12N2O5S | |
Historia
Fue lanzado en México por "Aulin & Mesulid" en 1985, estando al presente disponible en más de 50 países. La Nimesulida nunca fue aprobado por la FDA de Estados Unidos, y, por tanto, nunca entró al mercado en ese país. En 2002 el perfil beneficio/riesgo fue revisado por la EMEA siguiéndose con la decisión de suspender temporalmente esta droga del mercado a partir de marzo de 2002, en relación con los reportes de efectos adversos hepáticos en pacientes tratados con nimesulida. Más tarde se demostró que la ocurrencia de reacciones adversas hepáticas con la nimesulida es similar a otros antiinflamatorios no esteroides como lo confirmó un estudio publicado por el British Medical Journal en 2003.[2]
EMEA reporta relación beneficio/riesgo favorable
El 1 de agosto de 2003 el Committee for Proprietary Medicinal Products (CPMP) de la EMEA reportó que el "perfil beneficio/riesgo" de la nimesulida para uso sistémico y tópico es favorable y se deberían mantener las autorizaciones de comercialización. La CPMP recomienda restringir su uso a indicaciones de tratamiento del dolor agudo, tratamiento sintomático de dolorosas osteoartritis, dismenorreas y tendinitis aguda con formulación tópica.[3] Está prohibido su uso en pacientes por debajo de los doce años.[4]
Comercialización en la India
En India, la industria farmacéutica no reconoce las contraindicaciones, por lo que se sigue usando también en niños. Los proveedores indios de Nimesulida alegan que este fármaco compite con el Paracetamol y el Ibuprofeno.
Retiro del mercado en México para niños
En México, la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) suspendió la comercialización en el territorio nacional de este medicamento para uso pediátrico a partir del 24 de octubre de 2012, aunque se siguió permitiendo su uso en adultos. Derivado de diversas investigaciones, se ha determinado que la nimesulida de uso pediátrico causa reacciones adversas graves a nivel hepático.[5][6] El 30 de mayo de 2019, la COFEPRIS recomendó evitar totalmente la prescripción de dicho medicamento.[7]
Para mayor información, véase también
Referencias
- «Prohiben comercialización de nimesulida». Archivado desde el original el 14 de marzo de 2016. Consultado el 22 de marzo de 2016.
- No differences between nimesulide and other NSAIDs liver toxicity
- European Commission CPMP favourable opinion on nimesulide
- «The end begins». Archivado desde el original el 25 de febrero de 2007. Consultado el 26 de febrero de 2009.
- Alerta SST por consumo de Nimesulida de uso pediátrico en: Milenio Diario. Consultado el 01-11-2012.
- COFEPRIS restringe fármaco pediátrico en: El Universal. Consultado el 07-11-2012.
- «Aviso sobre los riesgos del consumo y uso de los medicamentos que contengan en su formulación Nimesulida». gob.mx. Consultado el 31 de mayo de 2019.
Enlaces externos
- (en inglés) nimesulide.net, por Helsinn Healthcare
- (en inglés) PubMed document
- (en inglés) NCBI document
- (en español) Nimesulida por la UNAM.
- (en español) Nimesulida por Chinoin Productos Farmacéuticos.
- (en español) Nimesulida por Hoffmann-La Roche.
- (en español) Nimesulida por Laboratorios Pisa.
- (en español) Nimesulida por Maver.