Danio rerio
El pez cebra o danio cebra (Danio rerio) es un ciprínido[2] emparentado con las carpas y los barbos, originario del sudeste asiático, habita mayormente en lagos, ríos y lagunas de la India, de uso frecuente en acuarios, así como para la investigación científica, siendo el primer vertebrado en clonarse.[3] Frecuentemente, se lo vende con el nombre cebra danio.[4] Está muy relacionado parentalmente, con Danio kyathit.[5] Y también emparentado cerradamente, con el género Devario, como demuestra el árbol filogenético.[6] Por muchos años, el pez cebra era referido en la literatura científica como Brachydanio rerio hasta ser reasignado al genus Danio.[7]
| Danio rerio | ||
|---|---|---|
 Ejemplar con fenotipo normal | ||
| Estado de conservación | ||
 Preocupación menor (UICN 3.1)[1] | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Chordata | |
| Clase: | Actinopterygii | |
| Infraclase: | Teleostei | |
| Orden: | Cypriniformes | |
| Familia: | Cyprinidae | |
| Género: | Danio | |
| Especie: |
D. rerio (Hamilton-Buchanan, 1822) | |
| Sinonimia | ||
| ||
Son peces alargados, fusiformes, con una única aleta dorsal, boca dirigida hacia arriba y un par de finas barbillas que son difíciles de ver salvo que el animal esté parado. Presentan dimorfismo sexual tanto en el tamaño como en el color. La hembra suele ser más grande que el macho y tiene un color de fondo plateado. El macho, sin embargo, adquiere tonalidades más doradas. Sobre los flancos y longitudinalmente se presentan de 5 a 9 bandas de color azul oscuro que comienzan detrás del opérculo y llegan hasta el final del animal (incluyendo la cola), dándole un aspecto cebrado del que toma el nombre. El opérculo es azulado y la zona ventral de un tono blanquecino rosado. Es transparente, lo que permite visualizar sin problemas la evolución de experimentos.[8] Alcanza 5 cm como talla máxima.
Ontogenia
Segmentación
El pez cebra presenta cigotos de tipo telolecítico, por lo cual la segmentación ocurre solo en una región libre de vitelo denominada el blastodisco. Debido a que el cigoto presenta una gran cantidad de vitelo, las segmentaciones son incompletas y, dado que el blastodisco es la zona donde se dan los clivajes, se dice que esta segmentación es meroblástica discoidal.[9]
La fecundación del cigoto desencadena unas ondas de calcio que estimulan la contracción del citoesqueleto de actina, lo que ocasiona una distribución exclusiva del vitelo hacia el polo vegetal, dejando una región del polo animal libre de vitelo. Este proceso determina la formación del blastodisco.[10]
La primera división es ecuatorial y la segunda meridional. Las primeras divisiones son muy sincrónicas, rápidas y conforman el blastodermo, que se observa como un bulto de células en la parte apical o distal del cigoto.[9]
Hacia el décimo clivaje empieza la transición a blástula media. Esto se hace evidente gracias a que las divisiones celulares se hacen más lentas, menos sincrónicas, comienza la transcripción génica y las células o blastómeras empiezan a migrar[11] generando tres capas celulares distinguibles:
- CSV (Capa Sincitial Vitelina): formada por la fusión de las células en el borde vegetal del blastodermo, se fusionan con la célula vitelínica subyacente. Esta capa a su vez se diferencia en CSV interna y CSV externa.[9]
- Capa de la envoltura: compuesta por las células más superficiales del blastodermo. Esta capa se convertirá en el peridermo.[9]
Entre la CSV y la capa de la envoltura se encuentran ubicadas las células profundas que dan origen al embrión.[9]
Los mapas celulares de destino parecen establecerse antes de la gastrulación.[12]
Durante el estadio de blástula, las tubulinas (subunidades de los microtúbulos y componentes de los centrosomas) se mantienen en un estado oligomérico que evita que se ensamblen constituyendo microtúbulos. La cantidad de tubulina soluble aumenta durante la gastrulación. La γ-tubulina asociada a complejos de proteínas, puede estar involucrada en la regulación de las dinámicas de la tubulina durante la oogénesis y embriogénesis del pez cebra.[13]
Gastrulación
La gastrulación se caracteriza por varios movimientos dentro de los que se incluyen la epibolia, invaginación y delaminación.
El primer movimiento de gastrulación en el pez cebra es el de epibolia de las células del blastodermo sobre el vitelo. Durante este movimiento, las células internas del blastodermo migran hacia fuera para intercalarse y cubrir las células superficiales completamente y de manera autónoma.[9] La CSV y la capa de la envoltura provocan este movimiento al expandirse.[14]
Durante la epibolía, un lado del blastodermo se engrosa. Este lado marcará el sitio de la futura superficie dorsal del embrión.[15]
Capas germinales
El engrosamiento del blastodermo, que luego originará la futura superficie dorsal del embrión, es denominada anillo germinal y se compone de dos capas:
- Epiblasto: capa externa
- Hipoblasto: capa interna
Las células de estas dos capas se intercalan formando el escudo embrionario que precede al labio dorsal del embrión. Este escudo embrionario es homólogo al labio dorsal del blastoporo en anfibios; es decir, cumple la misma función organizadora que el labio dorsal del blastoporo.[16] Sin embargo, estas estructuras difieren en algunas de sus actividades: la placa precordal en peces parece estar involucrada en la formación de estructuras neurales ventrales, pero las regiones anteriores del cerebro se desarrollan en su ausencia, mientras que esto no se aplica para anfibios.
Los movimientos de las células del epiblasto y del hipoblasto forman otra capa celular conocida como cordamesodermo, que es el precursor de la notocorda y la quilla neural, la cual está compuesta por células del hipoblasto ubicadas hacia la línea media dorsal. Las células remanentes del epiblasto constituirán el ectodermo.[9]
Formación de eje dorsoventral
La región más importante en la formación del eje dorsoventral en Danio rerio, y en peces en general, es el escudo embrionario. Esta región engrosada puede convertir al mesodermo lateral y ventral en mesodermo dorsal y también puede convertir el ectodermo en neural en lugar de epidérmico.[17]
Bioquímica del eje dorsoventral
El eje dorsoventral se construye gracias a la acción de varias familias de proteínas, dentro de las que se encuentran:
- BMP
- Algunas Wnt
Las proteínas BMP y Wnt inducirán al ectodermo a convertirse en epidermis. Un ligando mutante denominado BMP2B induce a las células a adquirir destinos ventral y lateral. Dicho mutante es epistático. Wnt8 es otro mutante que lateraliza, posterioriza y ventraliza los tejidos del embrión.[9]
La notocorda secreta factores que bloquean la inducción de estas familias de proteínas y permiten que el ectodermo se convierta en neural. Investigaciones previas sugirieron que uno de los factores que bloquean la inducción de BMP y Wnt, es el denominado Cordina (Chordin).[18] Sin embargo, estudios posteriores arrojan resultados que contradicen lo postulado con anterioridad, al encontrar que la pérdida de Cordino, en lugar de incrementar los niveles de señalización de BMP en el sistema, los disminuía y se perdía tejido ventral en la cola del embrión. Estos resultados sugieren que el Cordino es un antagonista y a la vez un promotor de la acción de BMP.[19]
Formación del eje anteroposterior
Al igual que en la formación del eje dorsoventral, las familias de proteínas que intervienen principalmente en su estableciemiento son las BMP y las Wnt, cuyos antagonistas incluyen factores como Cordina, Dickkopf y Nogina.
Neurulación
Es el proceso de conversión de la placa neural en tubo neural.
La neurulación del pez cebra incluye dos procesos conocidos como neurulación primaria y neurulación secundaria.
- Neurulación primaria: se refiere a la proliferación, invaginación y separación de las células de la placa neural.
- Neurulación secundaria: proceso mediante el cual el tubo neural se origina a partir de las células mesenquimáticas para formar un cordón sólido que posteriormente se cavita formando un tubo hueco.[9]
Desarrollo de las aletas
En Danio rerio, solo el tubo neural de la cola se construye por neurulación secundaria.[9]
Uso en laboratorios

Es especialmente apreciado por su homología genética con el humano (compartimos con estos peces más del 80 % del genoma) que permite que los resultados obtenidos de los fármacos probados en estos animales sean potencialmente extrapolables al humano.
Sus embriones son transparentes, algo que hace posible observar los efectos de estos medicamentos en sus órganos internos en formación.
Otra de las ventajas de este pez es su capacidad reproductiva —la hembra pone hasta 200 huevos—, continua -se reproducen durante todo el año- y rápido desarrollo -sus órganos se forman en solo 24 h, gracias a los cuales se pueden realizar diferentes experimentos en una misma generación de animales, investigar la evolución de las patologías e identificar las causas de las enfermedades investigadas.
Este pez tropical posee también la cualidad de regenerar los órganos que le son parcialmente amputados, lo que amplía las capacidades de investigación en este campo que tiene como horizonte la recuperación de las lesiones medulares.
Pueden criarse de tal modo que los mutantes pueden ser investigados y propagados, y es además el primer vertebrado en el que se ha intentado una mutagénesis intensiva.[9]
Su pequeño tamaño facilita su almacenaje, ya que caben hasta un centenar de animales en contenedores de un litro de agua, y su por sencillo mantenimiento decantan finalmente a favor del pez cebra las preferencias de los científicos como animal de laboratorio en el siglo XXI.
Los genes del pez cebra son muy dóciles de estudiar, ya que los embriones son sensibles a las moléculas antisentido de Morfolino y, por tanto, este método puede utilizarse para analizar si un gen dado es importante para una función en particular.[9]
Experimentos del desarrollo
Los experimentos genéticos en Danio rerio se basan en el método tradicional de estudio, en donde el pez progenitor macho es sometido a tratamientos con un mutágeno químico. Este mutágeno es llamado "ENU", también conocido como N-etil-N-nitrosourea, un muy potente mutágeno capaz de introducir una nueva mutación cada 700 locis y es tóxico en dosis altas. Este mutágeno causa mutaciones al azar en sus células germinales.[20] Cada macho mutante es apareado con una hembra silvestre de manera aleatoria para producir una descendencia F1. Las mutaciones serán heredadas solo del padre y, por tanto, si son dominantes, se expresarán y si son recesivas, no lo harán. Luego se produce una F2 al cruzar o aparear cualquier individuo de la F1 con un individuo silvestre.[9] Desarrollo de las aletas Asimismo, el pez cebra se ha establecido como un organismo modelo en el área de la regeneración (Véase Regeneración (biología)).
Posteriormente a la inducción del mutágeno ENU en GO, al secuenciar el DNA rico en exones, se puede identificar este mutágeno en la F1 y así predecir las consecuencias en la codificación de las proteínas con las mutaciones inducidas (mutaciones nonsense y mutaciones essential splice-site, es decir, a nivel de proteína estas últimas), para las cuales se generaron unos SNP con el fin de facilitar la identificación en las siguientes generaciones. De esta manera se pudo confirmar el 95% de las mutaciones candidatas para sucesivas generaciones.[20]
Secuenciación del exoma
Un método de secuenciación de exomas del pez cebra es el siguiente:
- El ADN se toma de la F1 que o bien se vuelve a cruzar o bien se criopreserva su esperma para mantener las posibles mutaciones. La criopreservación es útil para conservar la información genética y así demostrar que ese alelo produce un fenotipo para los siguientes experimentos o secuenciar más completamente todo el genoma. Del ADN se secuencia solo el exoma, y para ello este método lo que hace es realizar una genoteca de manera que lo que realizan es una hibridación del ADN genómico fragmentado con el RNA marcado con biotina, por lo que se obtendría un fragmento en el que quedarían hibridados los exones, de modo que podemos descartar lo que no es exon. Posteriormente, se descarta la doble cadena de RNA que no corresponde a los exones. Y por último se digiere el RNA que está marcado con biotina, puesto que solo servía como cebo para captar el exon, y después su secuenciación.[20] En la parte de enlaces externos pueden acceder a la página de "Zebrafish Mutation Project" que está indicada en el artículo "A systematic genome-wide analysis of zebrafish protein-coding gene function" http://www.sanger.ac.uk/Projects/D_rerio/zmp/
A continuación en el dibujo se muestran en azul los exones y en rojo del DNA genómico no codificante.
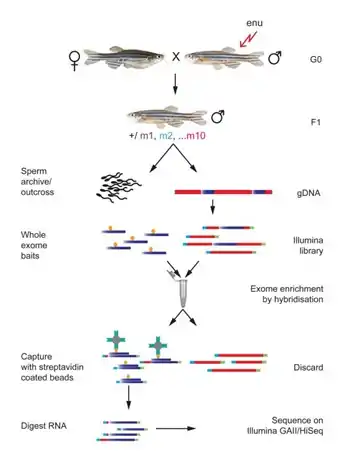
Genoma
Recientemente se ha secuenciado el genoma completo del pez cebra, lo que ha permitido conocer más a fondo las características de este pez. Tiene el mayor número de genes codificantes de los vertebrados (26479 genes, que se han podido analizar gracias a estudios de clonación posicional, mutagénesis de inserción, resecuenciación selectiva, etc.).[20] Esto puede ser debido a un proceso de duplicación extra del genoma que sufrió un antecesor común a este tipo de peces, frente a los más de 22.000 genes que codifican para proteínas analizados en ratones, lo que supone una ventaja para su uso en laboratorio en pro del pez cebra].[20] Este proceso se conoce como duplicación teleóstea específica del genoma (TSD), y además de proporcionarle un gran número de genes codificantes, también le aportó muchos genes específicos de especie (más que los humanos, los ratones o los pollos).
Gracias a la secuenciación completa del genoma, se ha podido observar asimismo que el 70 % de los genes humanos tienen, al menos, un ortólogo en pez cebra, por lo que este pez se puede usar como modelo animal para averiguar las funciones de algunos genes de vertebrados y caracterizar ciertas enfermedades hereditarias humanas.[21]
Se han podido identificar y fenotipar las mutaciones perjudiciales en cada gen que codifica para proteínas, utilizando un genoma de referencia secuenciado, como se ha comentado anteriormente, una secuenciación de alto rendimiento y una mutagénesis química eficiente. De manera que introducían mutaciones y posteriormente secuenciaban los exones para ver qué genes codificadores de proteínas habían sido dañados y así asociar fenotipo-mutación. Y como estos genes también están en la especie humana, eran capaces de asociar potencial-daño en esos genes a un potencial fenotipo que puede aparecer en los humanos, y así facilitar el auge de la comprensión respecto a la cantidad de enfermedades humanas cuyo gen responsable se desconoce.[20]
La comunidad que trabaja con él comparte libremente su genoma en repositorios en línea de acceso abierto. El pez cebra y el humano comparten el 70% de la información genética y más del 80% de los genes responsables de enfermedades humanas .[8]
Los laboratorios del Instituto Sanger están confeccionando un catálogo de mutantes. Se pretende mutar todos los genes del pez, uno a uno, y estudiar los efectos de cada mutación en la anatomía, fisiología y comportamiento.
Genotipado
Existen varias formas de genotipados, que no es más que llevar a cabo una PCR y secuenciarla. En el artículo al cual hace referencia esta información[20] se centran en un sistema de genotipado de SNPs KASP que utiliza un tipo de genotipado por fluorescencia.
El ensayo KASP es capaz de discriminar, mediante una PCR alelo específica competitiva, los alelos de un SNP en un locus específico a partir de un DNA genómico. Este ensayo utiliza una Taq polimerasa modificada sin actividad 3'-5' exonucleasa. Esta tecnología emplea primers que generan productos de PCR fluorescentes y que permiten genotipar el SNP en un único paso, por lo que este tipo de sistema de genotipado es útil para ensayos de genes de referencia, ensayos de alelos wild type y ensayos de alelos mutantes.[20]
Este tipo de sistema SNPs KASP se compone de un cebador específico de alelo que detecta el alelo mutante y de un bloqueador de oligonucleótidos que suprime al alelo wild type. Cada alelo tendrá un fluorocromo distinto y tiene una sonda en el medio, de modo que al realizar la PCR, el láser nos informa del producto que se ha amplificado, cuál de los dos primers específicos de cada alelo se ha unido, emitiendo un color u otro, de forma que se sabrá qué alelo se tiene.[20]
Referencias
- Vishwanath, W. (2010). «Danio rerio». Lista Roja de especies amenazadas de la UICN 2016.2 (en inglés). ISSN 2307-8235. Consultado el 14 de noviembre de 2016.
- "Danio rerio". En FishBase (Rainer Froese y Daniel Pauly, eds.). Consultada en marzo de 2007. N.p.: FishBase, 2007.
- «In Memory of George Streisinger, "Founding Father" of Zebrafish Developmental and Genetic Research». University of Oregon. Archivado desde el original el 29 de septiembre de 2015. Consultado el 23 de septiembre de 2015.
- «Zebra Danio». Aquatics To Your Door. Archivado desde el original el 28 de marzo de 2013. Consultado el 10 de abril de 2013.
- Mayden, Richard L.; Tang, Kevin L.; Conway, Kevin W.; Freyhof, Jörg; Chamberlain, Sarah; Haskins, Miranda; Schneider, Leah; Sudkamp, Mitchell et al. (2007). «Phylogenetic relationships of Danio within the order Cypriniformes: A framework for comparative and evolutionary studies of a model species». Journal of Experimental Zoology Part B: Molecular and Developmental Evolution. 308B (5): 642-54. PMID 17554749. doi:10.1002/jez.b.21175.
- Parichy, D M (2006). «Evolution of danio pigment pattern development». Heredity 97 (3): 200-10. PMID 16835593. doi:10.1038/sj.hdy.6800867.
- «The Zebrafish Book». ZFIN. Consultado el 3 de julio de 2013.
- http://esmateria.com/2013/04/17/la-transparencia-del-pez-cebra-le-convierte-en-el-mejor-raton-de-laboratorio/
- [Gilbert, Scott (2005). «Biología del Desarrollo». Panamericana 7. ISBN 950-06-0869-3].
- [Leung, C; Webb, S. E; Miller, A (2000). «On the mechanism of ooplasmic sgregation in zebrafish embryos». Dev. Growth Diff 40: 313-326.].
- [Kane, D.A; Kimmel, C.B (1993). «The zebrafish midblastula transition». Development 119: 447-456.].
- [Kimmel, C.B; Warga, R.M; Schilling, T.F (1990). «Origin and organization of the zebrafish fate map». Development 108: 581-594.].
- [Liu, Jianxiong; Lessman, Charles.A (2007). «Soluble tubulin complexes, y-tubulin, and their changing distribution in the zebrafish (Danio rerio) ovary, oocyte and embryo». Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology 147: 56-73.].
- [Trinkaus, J.P (1992). «The midblastula transition, the YSL transition, and the onset of gastrulation in Fundulus». Development: 75-80.].
- [Schmitz, B; Campos-Ortega, J.A (1994). «Dorso-ventral polarity of the zebrafish embryo is distinguishable prior to the onset of gastrulation». Wilhelm Roux Arch. Dev. Biol. 203: 374-380.].
- [Ho, R.K (1992). «Axis formation in the embryo of the zebrafish, Brachydanio rerio». Sem. Dev. Biol. 3: 53-64.].
- [Koshida, S; Shinya, M; Mizuno, T; Kuroiwa, A; Takeda, H (1998). «Initial anteroposterior pattern of zebrafish central nervous system is determined by differential competence of the epiblast». Development 125: 1957-1966.].
- [Kishimoto, Y; Lee, K.H; Zon, L; Hammerschmidt, M; Schulte-Merker, S (1997). «The molecular nature of sebrafish swirl: BMP2 function is essential during early dorsoventral pattering». Development 124: 4457-4466.].
- [Wagner, Daniel. S; Mullins, Mary. C (2001). «Modulation of BMP activity in dorsal-ventral pattern formation by the Chordin and Ogon antagonists». Developmental Biology 245: 109-123.].
- Kettleborough, Ross N. W.; Busch-Nentwich, Elisabeth M.; Harvey, Steven A.; Dooley, Christopher M.; de Bruijn, Ewart; van Eeden, Freek; Sealy, Ian; White, Richard J.; Herd, Colin; Nijman, Isaac J.; Fényes, Fruzsina; Mehroke, Selina; Scahill, Catherine; Gibbons, Richard; Wali, Neha; Carruthers, Samantha; Hall, Amanda; Yen, Jennifer; Cuppen, Edwin; Stemple, Derek L. (17 de abril de 2013). «A systematic genome-wide analysis of zebrafish protein-coding gene function». Nature (en inglés) 496 (7446): 494-497. doi:10.1038/nature11992.
- Howe, Kerstin, et al. "The zebrafish reference genome sequence and its relationship to the human genome." Nature (2013),.
Bibliografía
- "Danio rerio". En FishBase (Rainer Froese y Daniel Pauly, eds.). Consultada en febrero de 2012. N.p.: FishBase, 2012.
- «'Danio rerio' (TSN 163699)». Sistema Integrado de Información Taxonómica (en inglés).
- Lambert, Derek J (1997). Freshwater Aquarium Fish. Edison, New Jersey: Chartwell Books. p. 19. ISBN 0-7858-0867-1.
- Sharpe, Shirlie. «Zebra Danio». Your Guide to Freshwater Aquariums. Archivado desde el original el 7 de diciembre de 2016. Consultado el 15 de diciembre de 2004.
- Kocher, Thomas D.; Jeffery, WR; Parichy, DM; Peichel, CL; Streelman, JT; Thorgaard, GH (2005). «Fish Models for Studying Adaptive Evolution and Speciation». Zebrafish 2 (3): 147-56. PMID 18248189. doi:10.1089/zeb.2005.2.147.
- Bradbury, Jane (2004). «Small Fish, Big Science». PLoS Biology 2 (5): e148. PMC 406403. PMID 15138510. doi:10.1371/journal.pbio.0020148.
- Westerfield, M. (2007). The zebrafish book. A guide for the laboratory use of zebrafish (Danio rerio) (5th edición). Eugene, OR: University of Oregon Press.
- Guttridge, Nicky (2012). «Targeted gene modification can rewrite zebrafish DNA». Nature. doi:10.1038/nature.2012.11463.
- «A Point Of View: Fly, Fish, Mouse and Worm». BBC. 14 de junio de 2013. Consultado el 15 de junio de 2013.
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Danio rerio.
Wikimedia Commons alberga una categoría multimedia sobre Danio rerio. Wikispecies tiene un artículo sobre Danio rerio.
Wikispecies tiene un artículo sobre Danio rerio.- Ciencia al Cubo. RNE Historia del pez cebra
- Ficha de Danio rerio
- The Zebrafish Information Network
- Danio rerio
- Imágenes del desarrollo embrionario de Danio rerio
- "Proyecto Zebrafish Mutation"
- Danio rerio, en Danios.info
- Sanger Institute Zebrafish Mutation Resource
- Genoma de Danio rerio, vía Ensembl
- Genoma de Danio rerio (versión GRCz11/danRer11), vía UCSC Genome Browser
- Ficha del genoma de Danio rerio, vía NCBI
- Ficha de la versión del genoma de Danio rerio GRCz11/danRer11, vía NCBI
- FishforScience.com, – uso del pez cebra para estudios médicos
- FishForPharma
- Por qué el pez cebra genera su médula espinal y los humanos no