Quetoglobosina
Las quetoglobosinas son alcaloides mixtos aislados de hongos del género Chaetomium. Están relacionadas biosintéticamente con las citocalasinas.
Abundancia
Los principales hongos que producen quetoglobosinas pertenecen a los géneros Cladosporium, Stenocarpella, Calonectria y Chaetonium.[1] Las penocalasinas son producidas por hongos del género Penicillium.
Tipos de quetoglobosinas
| Nombre | Estructura | Fórmula molecular | CAS | Masa molecular (g/mol) | Estado | Fuente natural | Otras propiedades |
|---|---|---|---|---|---|---|---|
| Quetoglobosina A (Mucidina) |  |
C32H36N2O5 | 50335-03-0 | 528.647 | Prismas color amarillo pálido(CH2Cl2) PF = 188 °C | Aislado de los hongos Chaetomium cochliodes, Chaetomium globosum NRRL12718, Chaetomium subaffine, Penicillium aurantiogriseum, Cylindrocladium floridanum y Ascotricha chartarum[2] | [α]D= -270 (MeOH). Soluble en metanol y poco soluble en agua. UV: [neutral]λmax222 (ε36300 ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) (MeOH) [neutral]λmax196 (ε42700) ;220 (ε41600) ;271 (ε6600) ;280 (ε6600) ;290 (ε5360) (MeOH) [neutral]λmax223 (ε40740) ;274 (ε6610) ;282 (ε6607) ;292 (ε5370) (EtOH) |
| 19-O-Acetilquetoglobosina A. | Ac - O19 - Quetoglobosina A | C34H38N2O6 | 50939-69-0 | 570.684 | Cristales amarillos (PhH) PF = 224 °C | Aislado del hongo Chaetomium globosum[3] | [α]20D = -304 (c,0.5 en CHCl3) Poco soluble en hexano. UV: [neutral]λmax196 (log ε4.65) ;220 (log ε4.64) ;271 (log ε3.83) ;280 (log ε3.83) ;289 (log ε3.74) (EtOH). |
| Quetoglobosina B |  |
C32H36N2O5 | 50335-04-1 | 528.647 | Agujas amarillo pálido (PhH). PF = 187 °C | Aislado de los hongos Chaetomium cochliodes, Chaetomium rectum, Chaetomium mollipilum y Chaetomium globosum. | Citotóxico para las células HeLa. [α]D = -176 (c, 0.1 en MeOH). Soluble en metanol y poco soluble en agua. UV: [neutral]λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) (MeOH)[neutral]λmax222 (ε43650) ;274 (ε7940) ;281 (ε7950) ;290 (ε6760) (EtOH). |
| 19-O-Acetilquetoglobosina B | 19-O19-Quetoglobosina B | C34H38N2O6 | 80375-18-4 | 570.684 | Agujas amarillas (PhH) PF = 155 °C | Aislado del hongo Chaetomium globosum y de una especie marina no identificada de Acremonium.[4] | [α]20D = -148 (c, 0.5 en CHCl3) Poco soluble en hexano. UV: [neutral]λmax221 (log ε4.64) ;272 (log ε3.83) ;279 (log ε3.83) ;289 (log ε3.74) (EtOH). |
| Quetoglobosina C | 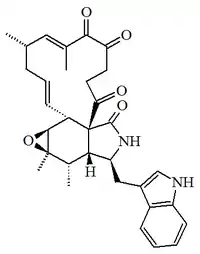 |
C32H36N2O5 | 50645-76-6 | 528.647 | Sólido PF = 260 °C | Aislado del hongo Chaetomium cochliodes y Chaetomium globosum | [α]D= -30 (c, 0.1 en MeOH); soluble en metanol, éter etílico y poco soluble en agua. UV: [neutral]λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) (MeOH) [neutral]λmax220 (ε47860) ;248 (ε9800) ;281 (ε6610) ;290 (ε5490) (EtOH) |
| Quetoglobosina D | 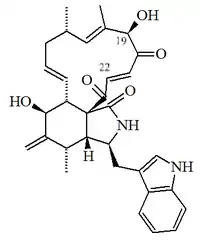 |
C32H36N2O5 | 55945-73-8 | 528.647 | Prismas amarillo pálido (CH2Cl2) PF = 216 °C | Aislado de los hongos Chaetomium cochliodes y Chaetomium globosum | Citotóxico; [α]D = -269 (c, 0.1 en MeOH). Soluble en metanol, éter etílico y poco soluble en agua. UV: [neutral] λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) ( MeOH) [neutral] λmax221 (ε43650) ;273 (ε9162) ;281 (ε9160) ;290 (ε7590) (EtOH) |
| 19-O-Acetilquetoglobosina D | Ac-O19-quetoglobosina D. | C34H38N2O6 | No disponible | 570.684 | Prismas amarillos PF = 240 °C | Aislado del hongo Chaetomium globosum y de una especie marina de Acremonium. | [α]D = -176 (c, 0.5 en CHCl3) poco soluble en hexano. UV: [neutral] λmax221 (log ε4.64) ;272 (log ε3.83) ;279 (log ε3.83) ;289 (log ε3.74) (EtOH) [neutral] λmax224 (ε43600) ;272 (ε6760) ;279 (ε6760) ;289 (ε5500) (MeOH). |
| Quetoglobosina E |  |
C32H38N2O5 | 55945-74-9 | 530.663 | Agujas (MeOH) PF = 280 °C | Aislado de los hongos Chaetomium cochliodes, Chaetomium subaffine ATCC22132, Chaetomium mollipilum y Chaetomium globosum.[5] | Citotóxico a las células HeLa; [α]D = +158 (c, 0.1 en MeOH). Soluble en metanol, éter etílico y pococ soluble en agua. UV: [neutral]λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) (MeOH) [neutral] λmax221 (ε56200) ;275 (ε7080) ;281 (ε7080) ;291 (ε6800) (EtOH) |
| Quetoglobosina F |  |
C32H38N2O5 | 55945-75-0 | 530.663 | Hojuelas (PhH) PF = 178 °C | Aislado de los hongos Chaetomium cochliodes, Chaetomium subaffine y Chaetomium globosum NRRL12718[6] | Citotóxico a las células HeLa; [α]D= -69 (c, 0.10 en CHCl3); soluble en metanol y éter etílico. Poco soluble en agua. UV: [neutral]λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) (MeOH) [neutral]λmax222;276;283;292 (EtOH) |
| Quetoglobosina Fex | 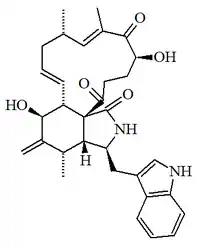 |
C32H38N2O5 | 149457-95-4 | 530.663 | Cristales PF = 152 °C | Aislado del hongo Chaetomium subaffine y Chaetomium globosum QEN-14.[7] | [α]D = +63.8 (c, 0.16 en MeOH) UV: [neutral]λmax221 (log ε4.59) ;274 (log ε3.78) ;283 (log ε3.8) ;291 (log ε3.72) (MeOH) |
| Quetoglobosina G | 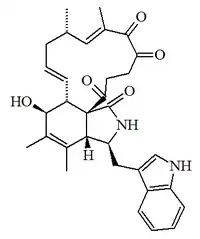 |
C32H36N2O5 | 65773-98-0 | 528.647 | Hojuelas (MeOH) PF = 252 | Aislado de los hongos Chaetomium cochliodes y Chaetomium subaffine ATCC22132.[8] | [α]D = +89 (c, 0.10 en MeOH); UV: [neutral]λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) (MeOH) [neutral]λmax222;275;282;291 (EtOH) |
| Quetoglobosina J | 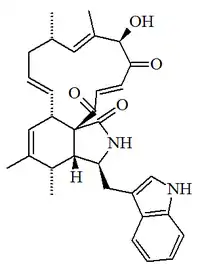 |
C32H36N2O4 | 65745-47-3 | 512.647 | Prismas amarillo pálido 150 °C | Aislado de los hongos Chaetomium cochliodes, Chaetomium globosum y Chaetomium subaffine[8] | [α]D = +41 (c, 0.1 en MeOH); UV: [neutral] λmax222 (ε36300) ;273 (ε6760) ;281 (ε6760) ;291 (ε5750) ( MeOH) [neutral]λ max224;270;280;290 (EtOH). |
| Quetoglobosina K | 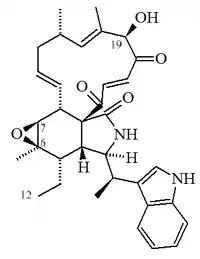 |
C34H40N2O5 | 72509-61-6 | 556.700 | Prismas amarillos (Acetona) PF = 235 - 240 °C | Aislado del hongo Diplodia macrospora | Inhibidor del crecimiento de plantas; tóxico para pollos. UV: [neutral]λmax221 (ε43700) ;273 (ε9120) ;281 (ε9120) ;290 (ε7590) (EtOH) [neutral] λmax219 (ε44800) ( EtOH). |
| Quetoglobosina L | 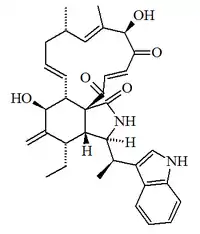 |
C34H40N2O5 | 83481-23-6 | 556.700 | Goma amarilla | Aislado del hongo Diplodia macrospora y Stenocarpella maydis[9] | No obtenido completamente puro. |
| Quetoglobosina M | 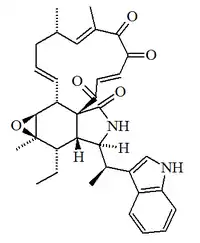 |
C34H38N2O5 | 119212-28-1 | 554.685 | Goma amarilla | Aislado del hongo Diplodia macrospora DM7 | [α]22D = -18.3 (c, 0.92 en CH2Cl2) Soluble en metanol, cloroformo y poco soluble en agua. UV: [neutral] λmax230 (ε12300) ;290 (ε3980) ( CH2Cl2) |
| Quetoglobosina N | 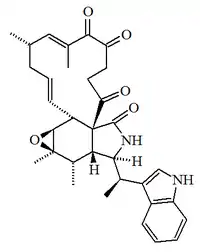 |
C33H38N2O5 | 156980-59-5 | 542.674 | Sólido PF = 205 °C | Aislado del hongo patógeno del maíz Phomopsis leptostromiformis[10] | Micotoxina del maíz |
| Quetoglobosina O |  |
C32H38N2O5 | 52645-09-7 | 530.663 | Líquido oleoso | Aislado del hongo Cylindrocladium floridanum[11] | [α]D = -168 (CHCl3) |
| Quetoglobosina P | 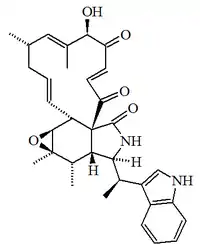 |
C33H38N2O5 | 191403-93-7 | 542.674 | Goma color amarillo pálido | Aislado del hongo Discosia sp. TCF 9535[12] | |
| Quetoglobosina Q |  |
C32H38N2O6 | 777939-29-4 | 546.662 | Sólido pálido amarillo | Aislado del hongo Chaetomium globosum[13] | [α]20D = -100 (c, 0.1 en MeOH) UV: [neutral] λmax217 (log ε4.81) ;289 (log ε4.05) (MeOH) |
| Quetoglobosina R |  |
C32H38N2O6 | 777939-30-7 | 546.662 | Sólido amarillo pálido | Aislado del hongo Chaetomium globosum junto con la quetoglobosina Q. | UV: [neutral] λmax220 (log ε4.46) ;282 (log ε3.73) (MeOH) |
| Quetoglobosina T | 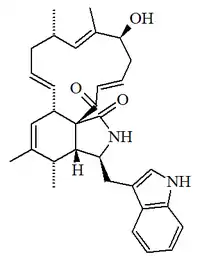 |
C32H38N2O3 | 777939-31-8 | 498.664 | Sólido | Aislado del hongo Chaetomium globosum | [α]20D = -80 (c, 0.1 en MeOH) UV: [neutral] λmax220 (log ε4.39) ;283 (log ε3.58) ;290 (log ε3.54) (MeOH) |
| Quetoglobosina U | 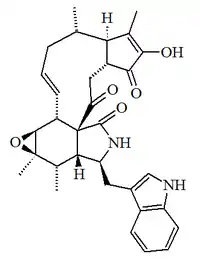 |
C32H36N2O5 | 882516-41-8 | 528.647 | Polvo amarillo pálido 168 °C | Aislado del hongo Chaetomium globosum IFB-E019[14] | [α]20D = -17 ( c, 0.18 in CHCl3); UV: [neutral] λmax222 (log ε0.48) ;281 (log ε0.09) ( CHCl3) |
| Quetoglobosina V | 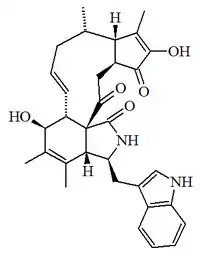 |
C32H36N2O5 | No reportado | 528.647 | Polvo amorfo | Aislado del hongo Chaetomium globosum IFB-E041[15] | [α]20D = -181 (c, 0.15 en MeOH) UV: [neutral]λmax206 (log ε4.54) ;221 (log ε4.61) ;269 (log ε4.09) (MeOH) |
| Quetoglobosina W | 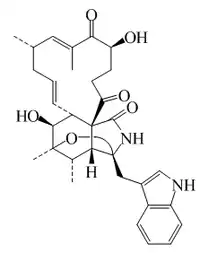 |
C32H38N2O6 | 1346835-16-2 | 546.662 | Polvo amorfo | Aislado del hongo Chaetomium globosum IFB-E041, junto con la quetoglobosina V. | [α]20D = -32 (c, 0.2 en MeOH) UV: [neutral]λmax205 (log ε4.53) ;220 (log ε4.61) ;281 (log ε3.87) ;289 (log ε3.8) (MeOH) |
| Quetoglobosina 510 | 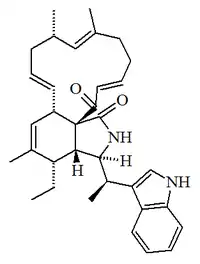 |
C34H42N2O2 | 871982-61-5 | 510.718 | Polvo amorfo | Aislado del hongo Phomopsis asparagi junto con las quetoglobosinas 540 y 542[16] | [α]25D = -100 (c, 0.02 en MeOH); UV: [neutral] λmax222 (log ε4.37) ;281 (log ε3.57) ;290 (log ε3.5) (MeOH) |
| Quetoglobosina 540 | 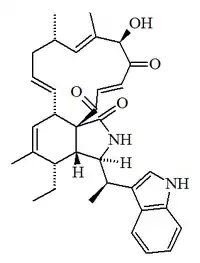 |
C34H40N2O4 | 871982-62-6 | 540.701 | Polvo amarillo pálido | Aislado del hongo Phomopsis asparagi junto con las quetoglobosinas 510 y 542 | α]25D -118 (c,0.009 en MeOH); UV: [neutral]λmax221 (log ε4.43) ;289 (log ε3.36) (MeOH). |
| Quetoglobosina 542 |  |
C34H42N2O4 | 871982-63-7 | 542.717 | Polvo amorfo | Aislado del hongo Phomopsis asparagi junto con las quetoglobosinas 510 y 540. | [α]25D = -44 (c, 0.01 en MeOH); UV: [neutral]λmax222 (log ε4.21) ;281 (log ε3.43) ;290 (log ε3.35) (MeOH) |
| Proquetoglobosina I |  |
C32H38N2O2 | 133613-77-1 | 482.664 | Cristales (MeOH) PF = 215 °C | Aislado del hongo Chaetomium subaffine | [α]D = -101.3 (c, 0.3 en MeOH). UV: [neutral]λmax223 (log ε4.45) ;291 (log ε3.5) (MeOH). |
| Proquetoglobosina II | 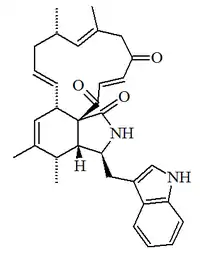 |
C32H36N2O3 C32H36N2O3 | 133625-26-0 | 496.648 | Cristales amarillo pálido (MeOH) PF = 188 °C | Aislado del hongo Chaetomium subaffine | [α]D = -204.2 (c, 0.4 en MeOH) UV: [neutral] λmax221 (log ε4.45) ;273 (log ε3.59) (MeOH) |
| Proquetoglobosina III |  |
C32H36N2O4 | 133613-78-2 | 512.647 | Cristales amarillo pálido (MeOH ac.) PF = 138 °C | Aislado del hongo Chaetomium elata[17] | [α]D = -210.4 (c,0.2 en MeOH); UV: [neutral]λmax221 (log ε4.7) ;280 (log ε3.87) ;290 (log ε3.79) (MeOH) |
| 20-Dihidroprotoquetoglobosina III | 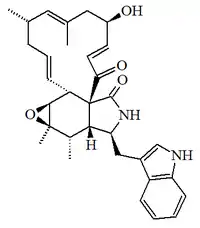 |
C32H38N2O4 | 149439-84-9 | 514.663 | Líquido oleoso | Aislado del hongo Chaetomium subaffine junto con la proquetoglobosina IV. | [α]D = -60 (c, 0.06 en MeOH); UV: [neutral]λmax222 (log ε4.63) ;291 (log ε3.72) ( MeOH) |
| Proquetoglobosina IIIed | 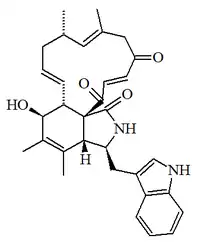 |
C32H36N2O4 | 146426-37-1 | 512.647 | Cristales amarillo pálido (CHCl3) PF = 154 °C | Aislado del hongo Chaetomium elatum[18] | [α]D = -15.3 ( c, 0.06 in CHCl3) UV: [neutral] λmax222 (log ε4.43) ;282 (log ε3.66) ;291 (log ε3.6) (MeOH) |
| Proquetoglobosina IV | 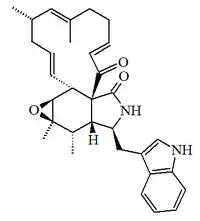 |
C32H38N2O3 | 137604-97-8 | 498.664 | Cristales (CHCl3>/sub>) PF = 257 °C | Aislado del hongo Chaetomium subaffine[19] | [α]D = -54.5 (c,0.02 en MeOH); UV: [neutral]λmax222 (log ε4.45) ;291 (log ε3.67) (MeOH) |
| Penocalasina A | 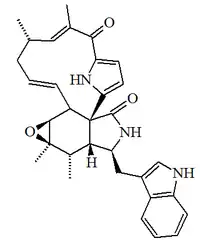 |
C32H35N3O3 | Aislado de un Penicillium endófito del alga Enteromorpha intestinalis[20] | Actividad citotóxica potente contra cultivos de linfocitos de leucemia P388. | |||
| Penocalasina B |  |
C32H35N3O3 | Aislado de un Penicillium endófito del alga Enteromorpha intestinalis junto con las penocalasinas A y C. | Actividad citotóxica potente contra cultivos de linfocitos de leucemia P388. | |||
| Penocalasina C | 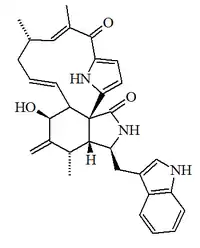 |
C32H35N3O3 | Aislado de un Penicillium endófito del alga Enteromorpha intestinalis junto con las penocalasinas A y B. | Actividad citotóxica potente contra cultivos de linfocitos de leucemia P388. | |||
| Penocalasina E | 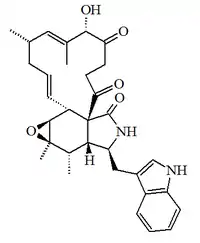 |
C32H38N2O5 | 345642-81-1 | 530.663 | Líquido oleoso | Aislado de un Penicillium marino sin identificar. | Citotóxico; [α]D = +73 (c,0.14 en CHClsub>3) UV: [neutral]λmax221 (log ε4.43) ;241 (log ε3.97) ;280 (log ε3.84) ;291 (log ε3.77) (EtOH) |
| Penocalasina F |  |
C32H38N2O5 | 345642-82-2 | 530.663 | Líquido oleoso | Aislado del hongo marino Penicillium[21] | [α]D = -80 (c,0.13 en CHCl3), UV: [neutral]λmax220 (log ε4.68) ;240 (log ε4.28) ;280 (log ε4.17) ;291 (log ε4.1) (EtOH) |
| Penocalasina G |  |
C32H38N2O4 | No reportado | 514.663 | Polvo PF = 125 °C | Aislado de un hongo marino del género Penicillium[21] | Citotóxico. [α]D = -143.6 (c, 0.19 en CHCl3) UV: [neutral] λmax220 (log ε4.42) ;240 (log ε3.82) ;280 (log ε3.8) (EtOH). |
| Penocalasina H | 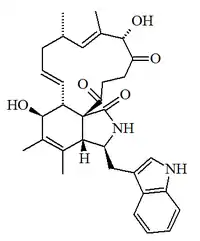 |
C32H38N2O5 | 345642-84-4 | 530.663 | Polvo PF = 182 °C | Aislado una especie marina de Penicillium no identificada.[22] | [α]D = -72.7 (c, 0.18 en CHCl3) UV: [neutral] λmax220 (log ε4.16) ;243 (log ε3.97) ;281 (log ε3.52) ;290 (log ε3.5) (EtOH) |
| Citoglobosina A | 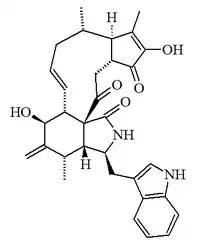 |
C32H36N2O5 | 1221163-90-1 | 528.647 | Polvo amorfo (DMSO) | Aislado del hongo Chaetomium globosum QEN-14[23] | [α]25D = +5 (c, 0.08 en MeOH); UV: [neutral]λmax203 (log ε3.56) ;207 (log ε3.58) ;221 (log ε3.75) ;239 (log ε3.23) ;268 (log ε3.23) (MeOH) |
| Citoglobosina B |  |
C32H38N2O5 | 1221163-92-3 | 530.663 | Polvo amorfo (DMSO) | Aislado del hongo Chaetomium globosum QEN-14[23] | [α]25D = +11 (c, 0.06 en MeOH); UV: [neutral] λmax203 (log ε4.05) ;222 (log ε4.13) ;281 (log ε3.3) ;290 (log ε3.23) (MeOH) |
| Citoglobosina C |  |
C32H38N2O5 | 1221163-94-5 | 530.663 | Polvo amorfo (DMSO) | Aislado del hongo Chaetomium globosum QEN-14[24] | Citotóxico. [α]25D = +36 (c, 0.02 en MeOH). UV: [neutral]λmax206 (log ε3.86) ;223 (log ε4.18) ;254 (log ε3.46) ;261 (log ε3.45) ;289 (log ε4.29) (MeOH) |
| Citoglobosina D | 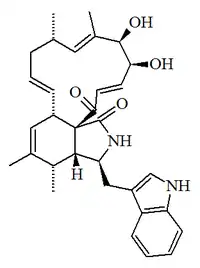 |
C32H38N2O4 | 1221163-96-7 | 514.663 | Polvo amorfo (DMSO) | Aislado del hongo Chaetomium globosum QEN-14[24] | Citotóxico. [α]25D = -34 (c, 0.04 en MeOH) UV: [neutral] λmax203 (log ε4.08) ;222 (log ε4.17) ;279 (log ε3.39) ;290 (log ε3.3) (MeOH) |
| Citoglobosina F |  |
C32H38N2O5 | 1221164-00-6 | 530.663 | Polvo amorfo (DMSO) | Aislado del hongo Chaetomium globosum QEN-14 junto con las quetoglobosinas B y G. | [α]25D = -73 (c, 0.15 en MeOH) |
| Citoglobosina G | 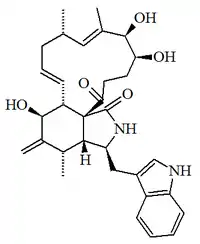 |
C32H40N2O5 | 1221164-02-8 | 532.678 | Polvo amorfo (DMSO) | Aislado del hongo Chaetomium globosum QEN-14 junto con las quetoglobosinas B y F. | [α]25D = +4 (c, 0.1 en MeOH) UV: [neutral] λmax204 (log ε4.14) ;221 (log ε4.17) ;274 (log ε3.44) ;290 (log ε3.39) (MeOH). |
| Isoquetoglobosina D |  |
C32H36N2O5 | 83530-07-8 | 528.647 | Sólido 265 °C | Aislado del hongo Chaetomium globosum KMITL-N0802 y Chaetomium globosum QEN-14.[25] | [α]D = +41 (c, 0.1 en MeOH); UV: [neutral] λmax222 (log ε4.53) ;275 (log ε3.82) ;281 (log ε3.82) ;291 (log ε3.76) (EtOH). |
| Isoquetoglobosina J |  |
C32H36N2O4 | 146426-38-2 | 512.647 | Cristales amarillo pálido . (CHCl3) PF = 118 °C | Aislado del hongo Chaetomium subaffine | [α]D = -20 (c, 0.07 en MeOH); UV: [neutral] λmax221 (log ε4.59) ;291 (log ε3.74) (MeOH) |
| Antibiótico TAN 1142 (20S-Dihidroquetoglobosina A) | 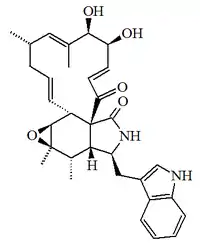 |
C32H38N2O5 | 149560-98-5 | 530.663 | Sólido PF = 146 °C | Aislado de los hongos Chaetomium globosum y Chaetomium subaffine.[26] | [α]D = -82.8 (MeOH); UV: [neutral]λmax212 (log ε4.71) ;221 (log ε4.8) ;266 (log ε3.93) ;272 (log ε3.92) ;291 (log ε3.82)(MeOH) |
Actividad biológica
Las quetoglobosinas A y C han mostrado actividad inhibitoria marcada contra Mucor miehei. Muchos de estos compuestos también son tóxicos al ganado. La quetoglobosina A es citotóxica a las células HeLa cells; promuebe lña fibrinólisis, son fitotóxicos, inducen la producción de uroquinasa y es inhibidora del ensamblaje de las proteínas de los microtúbulos. Es teratogénica.
Biosíntesis
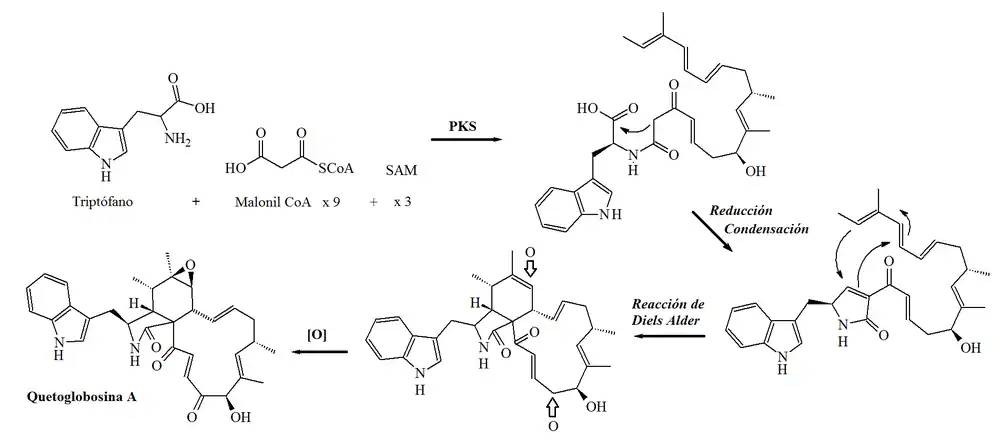
La biosíntesis de la quetoglobosina A ha sido estudiada por Oikawa y colaboradores. La quetoglobosina A es un alcaloide mixto que proviene de una amida entre el triptófano y un nonacétido trimetilado. Esta amida condensa intramolecularmente en el carbono donde se encontraba el carboxilo del triptófano para formar un anillo de 1,5-dihidro-2H-pirrol-2-ona. En el extremo terminal del policétido se encuentra un dieno, el cual reacciona en una cicloadición tipo Diels-Alder con la α,β insaturación de la pirrolona. El aducto formado puede oxidarse en dos pasos adicionales, formando así la quetoglobosina A.[27]
El clóster génico de la quetoglobosina de Pencillium expansum fue identificado, incluyendo CheA, un híbrido fungal iterativo tipo I PKS-NRPS. CheA tiene similitud con las megasintasas requeridas para la biosíntesis de aductos Diels Alder, tales como la lovastatina y equisetina (LovB y EqiS, respectivamente), y es requerida para la producción de las micotoxinas fusarina y tenelina.[28][29][30] La enoil reductasa de la quetoglobosina, CheB, actúa en trans con CheA para generar un nonacétido como intermediario. Los productos correspondientes a este clóster se espera que codifiquen a dos citocromos P450 (CheD and CheG) y una monooxigenasa FAD-dependiente(CheA), estas tres implicadas en las modificaciones posteriores al policétido precursor.[31]
Se cree que el módulo de polipéptido sintasa no ribosomal (NRPS) del CheA activa al triptófano y genera una unión amida con el nonacétido de modo análogo para el módulo EqiS NRPS de la equisetina.[32] Se cree que el intermediario policétido-aminoácido se reduce en la posición correspondiente al carboxilo del triptófano para producir el aldehído correspondiente.[33] El anillo de isoindolona se produce en un proceso de 2 pasos: una condensación de Knoevenagel para generar la pirrolinona y posteriormente la cicloadición Diels Alder.[34]
Referencias
- Bioactive metabolites from Stenocarpella maydis, a stalk and ear rot pathogen of maize. Wicklow DT, Rogers KD, Dowd PF, Gloer JB. Fungal Biol. (2011) 115(2):133-42.
- Umeda, M. et al., Experientia, 1975, 31, 435- 438
- Probst, A. et al., Helv. Chim. Acta, 1981, 64, 2056- 2064; 2065- 2077
- Probst, A. et al., Helv. Chim. Acta (1981) 64, 2056- 2064
- Umeda, M. et al., Experientia, 1975, 31, 435- 438
- Sekita, S. et al., Chem. Pharm. Bull., 1982, 30, 1609- 1617; 1618- 1628; 1982, 30, 1629- 1638; 1983, 31, 490- 498
- Oikawa, H. et al., Biosci., Biotechnol., Biochem., 1993, 57, 628- 631
- Sekita, S. et al., Chem. Pharm. Bull., 1982, 30, 1609- 1617
- Wicklow, D.T., Rogers, K.D., Dowd, P.F., Gloer, J.B. Fungal Biology (2011) 115 (2) , pp. 133-142
- Cherton, J.C. et al., Analusis, 1994, 22, 210- 216; 217- 221
- Ichihara, A. et al., Biosci., Biotechnol., Biochem., 1996, 60, 360- 361
- Donoso, R. et al., Nat. Prod. Lett., 1997, 10, 49- 54
- Jiao, W. et al., J. Nat. Prod., 2004, 67, 1722- 1725
- Ding, G. et al., J. Nat. Prod., 2006, 69, 302- 304
- Zhang, J. et al., Planta Med., 2010, 76, 1910- 1914
- Christian, O.E. et al., J. Nat. Prod., 2005, 68, 1592- 1597
- Oikawa, H. et al., JCS Perkin 1, 1992, 2949- 2953
- Oikawa, H. et al., JCS Perkin 1, 1992, 2949- 2953; , 2955- 2959
- Oikawa, H. et al., JCS Perkin 1, 1992, 2955- 2959
- Numata et al. J. Chem. Soc. Perkin Trans. 1 (1996) 239-245
- Iwamoto, C. et al., Tetrahedron, 2001, 57, 2997- 3004
- Iwamoto, C. et al., Tetrahedron, 2001, 57, 2997- 3004
- Cui, C.-M. et al., J. Nat. Prod., 2010, 73, 729- 733
- Cui, C.-M. et al., J. Nat. Prod., 2010, 73, 729- 733
- Kanokmedhakul, S. et al., Planta Med., 2002, 68, 834- 836
- Oikawa, H. et al., Biosci., Biotechnol., Biochem., 1993, 57, 628- 631
- Biosynthetic study of chaetoglobosin A: origins of the oxygen and hydrogen atoms, and indirect evidence for biological Diels–Alder reaction. Hideaki Oikawa , Yasunobu Murakami, Akitami Ichihara. J. Chem. Soc., Perkin Trans. 1 (1992) pp.2955-2959
- J. Kennedy, K. Auclair, S. G. Kendrew, C. Park, J. C. Vederas and C. R. Hutchinson, Science (1999) 284:1368–1372.
- J. W. Sims, J. P. Fillmore, D. D. Warner and E. W. Schmidt. Chem. Commun. (2005) pp. 186–188
- K. L. Eley, L. M. Halo, Z. Song, H. Powles, R. J. Cox, A. M. Bailey,C. M. Lazarus and T. J. Simpson, ChemBioChem (2007) 8, 289–297.
- Z. Song, R. J. Cox, C.M. Lazarus and T. J. Simpson, ChemBioBhem (2004) 5:1196–1203
- J. Schümann, C. Hertweck, J. Am. Chem. Soc. (2007) 129, 9564–9565.
- H. Oikawa, Y. Suzuki, A.Naya, K.Katayama and A. Ichihara, J. Am.Chem. Soc. (1994) 116:3605–3606.
- K. Katayama, T. Kobayashi, H. Oikawa,M. Honma and A. Ichihara. Biochim. Biophys. Acta (1998) 1384:387–395.
Véase también
- Citocalasinas