Reacción de Reed
La reacción de Reed es una reacción química que utiliza la luz para oxidar los hidrocarburos a los cloruros de sulfonilo empleando para este fin dióxido de azufre y cloro diatómico.[1] La reacción lleva a cabo a través de un mecanismo de radicales libres. En primer lugar, la luz promueve la disociación homolítica de una molécula de cloro; a continuación, el radical de cloro producido ataca la cadena de hidrocarburo para formar un cloruro de hidrógeno, lo que provoca la formación de radicales libres alquilo. A continuación, la molécula de dióxido de azufre dona un electrón para formar un enlace y un radical sulfonilo. Por último, este radical ataca al otro radical cloro para formar así el cloruro de sulfonilo deseado.[2]
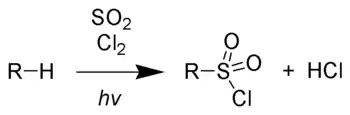
Mecanismo
Iniciación:
Propagación:
Terminación:
Los cloruros de sulfonilo resultantes son ampliamente utilizados en la industria de detergentes como materia prima. En determinadas circunstancias (40-80 °C) sólo se lleva a cabo la cloración de alcanos.
Referencias
- Asinger, F. et al. Ber. 1942, 75, 34.
- Helberger, J. H.; Manecka, G.; Fischer, H. M. Ann. 1949, 562, 23.