Tienamicina
La tienamicina, también conocida como tienpenem, es uno de los más potentes antibióticos producidos naturalmente hasta ahora, fue descubierto en Streptomyces cattleya en 1976. La tienamicina tiene una excelente actividad contra bacterias Gram-positivas y Gram-negativas y es resistente a la enzima β-lactamasa bacteriana. Es un zwitterion a pH 7.[2]
| Tienamicina | ||
|---|---|---|
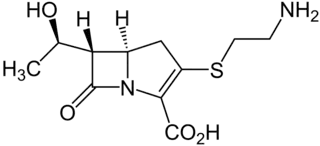 | ||
| Nombre IUPAC | ||
|
(5R,6S)-3-[(2-Aminoetil)tio]-6-[(1R)-1- hidroxietil]-7-oxo-1-azabiciclo[3.2.0]hept- 2-ene-2-ácido carboxílico | ||
| General | ||
| Fórmula estructural |
 | |
| Fórmula molecular | C11H16N2O4 | |
| Identificadores | ||
| Número CAS | 59995-64-1[1] | |
| ChEBI | 9542 | |
| ChEMBL | 278773 | |
| ChemSpider | 389922 | |
| PubChem | 441128 | |
| UNII | WMW5I5964P | |
| KEGG | C06664 | |
|
O=C(O)/C1=C(\SCCN)C[C@H]2N1C(=O)[C@@H]2[C@H](O)C
| ||
| Propiedades físicas | ||
| Masa molar | 272,083078 g/mol | |
Mecanismo de acción
In vitro, la tienamicina emplea un modo de acción similar a las penicilinas a través de la interrupción de la síntesis de la pared celular (biosíntesis de peptidoglicanos) de varias bacterias Gram-positivas y Gram-negativas (Staphylococcus aureus, Staphylococcus epidermidis, Pseudomonas aeruginosa por nombrar algunas). Aunque la tienamicina se une a todas las proteínas de unión a penicilina (PBP) en Escherichia coli, se une preferentemente a PBP-1 y PBP-2, ambas asociadas con el alargamiento de la pared celular. A diferencia de las penicilinas, que se vuelven ineficaces a través de la rápida hidrólisis por la enzima β-lactamasa presente en algunas cepas de bacterias, la tienamicina permanece antimicrobialmente activa. La tienamicina mostró una alta actividad contra las bacterias que eran resistentes a otros compuestos estables a las β-lactamasas (cefalosporinas), destacando la superioridad de la tienamicina como un antibiótico entre las Beta-lactámicas.
Referencias
- Número CAS
- Nicolaou, K.C.; Sorensen, Erik (1996). VCH Publishers, ed. Classics in Total Synthesis. pp. 255, 260. ISBN 3-527-29231-4.