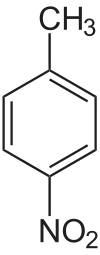
4-Nitrotoluène
Le 4-nitrotoluène est un dérivé du toluène possédant un groupe nitro. La formule brute de ce composé est C7H7NO2. C'est l'un des trois isomères du nitrotoluène, l'isomère para, les deux autres étant les isomères méta (3-nitrotoluène) et ortho (2-nitrotoluène).
| 4-Nitrotoluène | |||
| |||
| Identification | |||
|---|---|---|---|
| Synonymes |
p-nitrotoluène |
||
| No CAS | |||
| No ECHA | 100.002.553 | ||
| No CE | 202-808-0 | ||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule | C7H7NO2 [Isomères] |
||
| Masse molaire[1] | 137,136 ± 0,006 9 g/mol C 61,31 %, H 5,14 %, N 10,21 %, O 23,33 %, |
||
| Moment dipolaire | 4,68 D | ||
| Propriétés physiques | |||
| T° fusion | 51,6 °C | ||
| T° ébullition | 238,3 °C | ||
| Thermochimie | |||
| Cp | |||
| Précautions | |||
| Transport | |||
|
|||
| Écotoxicologie | |||
| LogP | 2,37 | ||
| Seuil de l’odorat | bas : 0,000 72 ppm[3] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
Propriétés et risques
Le 4-nitrotoluène se décompose en chauffant fortement, produisant des fumées toxiques d'oxydes d'azote. Il réagit violemment avec les oxydants forts et l'acide sulfurique ainsi qu'avec le feu - et présente des risques d'explosion. Le 4-nitrotoluène attaque certaines matières plastiques, le caoutchouc et certains revêtements.
Il est irritant pour les yeux et la peau. Il peut avoir des effets sur le sang, entraînant la formation de méthémoglobine, les effets pouvant être retardés.
Une exposition prolongée peut avoir un impact sur le sang, le foie ou les testicules.
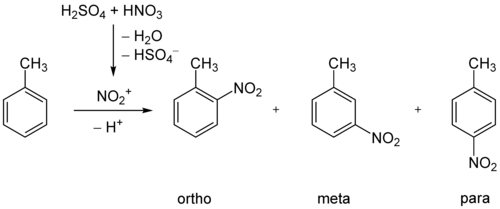
Synthèse
La nitration aromatique du toluène par l'acide nitrique en présence d'acide sulfurique produit un mélange des trois isomères. Le groupe méthyle étant orienteur ortho-para et de faible encombrement stérique, on obtient majoritairement l'isomère ortho (~60 %), puis l'isomère para (~37 %) et très peu de l'isomère méta (~2 %).
Les isomères peuvent ensuite être séparés par cristallisation, les points de fusions des trois isomères étant assez éloignés (respectivement −10 °C, 15,5 °C et 51,6 °C). Une autre méthode de séparation est l'adsorption sélective des isomères par un zéolithe adéquat. Dans ces conditions réactionnelles, le risque est peu élevé d'effectuer une double nitration et de synthétiser le 2,4-dinitrotoluène. Pour cela, il est nécessaire d'utiliser de l'acide sulfurique fumant (concentré).
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-858-6)
- « p-Nitrotoluene », sur hazmap.nlm.nih.gov (consulté le )
- Portail de la chimie