Acide isobutyrique
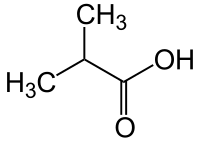
L'acide isobutyrique ou acide 2-méthylpropanoïque ou acide isobutanoïque est l'acide carboxylique de formule semi-développée (CH3)2-CH-COOH. C'est un liquide incolore d'odeur désagréable et un isomère de l'acide butanoïque.
| Acide isobutyrique | |
| |
| Identification | |
|---|---|
| Nom UICPA | acide 2-méthylpropanoïque |
| Synonymes |
acide isobutyrique, acide diméthylacétique, acide isobutanoïque |
| No CAS | |
| No ECHA | 100.001.087 |
| No CE | 201-195-7 |
| No RTECS | NQ4375000 |
| PubChem | 6590 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore |
| Propriétés chimiques | |
| Formule | C4H8O2 [Isomères] |
| Masse molaire[1] | 88,105 1 ± 0,004 4 g/mol C 54,53 %, H 9,15 %, O 36,32 %, |
| pKa | 4,86[2] |
| Propriétés physiques | |
| T° fusion | −46 °C[3] |
| T° ébullition | 155 °C[3] |
| Solubilité | 210 g·l-1 à 20 °C[3] |
| Paramètre de solubilité δ | 21,1 MPa1/2 (25 °C)[4] |
| Masse volumique | 0,95 g·cm-3[3] |
| T° d'auto-inflammation | 500 °C[3] |
| Point d’éclair | 57,5 °C[3] 55 °C[5] |
| Pression de vapeur saturante | 1,81 mbar à 20 °C 3,61 mbar à 30 °C 6,86 mbar à 40 °C 12,5 mbar à 50 °C[3] |
| Propriétés optiques | |
| Indice de réfraction | = 1.393 [5] |
| Précautions | |
| SGH[3] | |
 |
|
| Transport[3] | |
| Écotoxicologie | |
| LogP | 0,94 [3] |
| Unités du SI et CNTP, sauf indication contraire. | |
Il est trouvé à l'état naturel dans le caroubier (Ceratonia siliqua), dans les racines d'Arnica dulcis et sous forme d'ester éthylique dans l'huile de croton. Il est produit par la paire de glandes périanales du binturong (Viverridae).
Cet acide peut être préparé synthétiquement par hydrolyse d'isobutyronitrile, (CH3)2CH-CN, avec une base, par oxydation d'isobutanol avec du dichromate de potassium dans l'acide sulfurique[6] ou par action de l'amalgame de sodium sur l'acide méthacrylique.
Chauffé dans une solution d'acide chromique à 140 °C, l'acide isobutyrique se décompose en dioxyde de carbone, CO2 et en acétone, (CH3)2CO. Une solution alcaline de permanganate de potassium l'oxyde en l'acide α-hydroxyisobutyrique (acide 2-méthyl-2-hydroxypropanoïque).
Ses sels (isobutyrate) sont généralement plus solubles dans l'eau que ceux de l'acide butanoïque (butanoate).
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Isobutyric acid » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Bjerrum, J., et al. Stability Constants, Chemical Society, London, 1958.
- Entrée « Isobutyric acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 19 avril 2011 (JavaScript nécessaire)
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 0387690026, lire en ligne), p. 294
- Isobutyric acid chez Sigma-Aldrich.
- (en) I. Pierre and E. Puchot, « New Studies on Valerianic Acid and its Preparation on a Large Scale », Ann. de chim. et de phys., vol. 28, , p. 366

