Azoture de tosyle
L'azoture de tosyle est un réactif utilisé en synthèse organique[1].
| Azoture de tosyle | |||
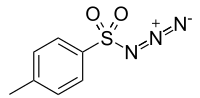
| |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | azoture de 4-méthylbenzènesulfonyle | ||
| Synonymes |
azoture de p-toluènesulfonyle, azoture de p-tosyle |
||
| No CAS | |||
| No ECHA | 100.012.164 | ||
| No CE | 213-381-5 | ||
| PubChem | 13661 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide huileux incolore[1] | ||
| Propriétés chimiques | |||
| Formule | C7H7N3O2S [Isomères] |
||
| Masse molaire[2] | 197,214 ± 0,012 g/mol C 42,63 %, H 3,58 %, N 21,31 %, O 16,23 %, S 16,26 %, |
||
| Propriétés physiques | |||
| T° fusion | 21 à 22 °C[1] | ||
| T° ébullition | 110 à 115 °C (0,001 mmHg[1] | ||
| Masse volumique | 1,286 g·cm-3[1] | ||
| Point d’éclair | 4 °C[3] | ||
| Propriétés optiques | |||
| Indice de réfraction | 1,502[3] | ||
| Précautions | |||
| SGH[3] | |||
  Danger |
|||
| NFPA 704[3] | |||
| Transport[3] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
Synthèse
L'azoture de tosyle peut être préparé par réaction entre le chlorure de tosyle et l'azoture de sodium en solution aqueuse d'acétone[4].
Utilisation
L'azoture de tosyle est utilisé pour introduire les groupes fonctionnels azoture et diazo[1]. Il est aussi utilisé comme source en nitrène et comme substrat pour les cycloadditions [3+2][1].
Sécurité
L'azoture de tosyle est l'un des azotures les plus stables, mais il est toujours considéré comme un explosif potentiel et doit donc être conservé avec précautions.
Notes et références
- "p-Toluenesulfonyl Azide". Heydt, Heinrich; Regitz, Manfred. Encyclopedia of Reagents for Organic Synthesis (2001)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé p-Toluenesulfonyl azide solution, consultée le 21 décembre 2012.
- (en) Curphey, Thomas J., « Preparation of p-toluenesulfonyl azide. A cautionary note », Organic Preparations and Procedures International (, vol. 13, no 2, , p. 112–115
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Tosyl azide » (voir la liste des auteurs).
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.

