Dichlorométhane
Le dichlorométhane (DCM) ou chlorure de méthylène (dénommé R30 dans la liste des réfrigérants), est un composé organique se présentant à température ambiante comme un liquide incolore et volatil émettant une odeur douceâtre relativement forte pouvant mettre certaines personnes mal à l'aise. Son odeur est perceptible dès 200–300 ppm (dès 25 ppm ou seulement vers 600 ppm selon d'autres sources[13]).
| Dichlorométhane | |
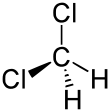 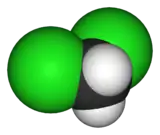 Structure du dichlorométhane |
|
| Identification | |
|---|---|
| Nom UICPA | dichlorométhane |
| Synonymes |
chlorure de méthylène |
| No CAS | |
| No ECHA | 100.000.763 |
| No CE | 200-838-9 |
| No RTECS | PA8050000 |
| PubChem | 6344 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore, d'odeur caractéristique[1]. |
| Propriétés chimiques | |
| Formule | CH2Cl2 [Isomères] |
| Masse molaire[2] | 84,933 ± 0,005 g/mol C 14,14 %, H 2,37 %, Cl 83,48 %, |
| Moment dipolaire | 1,14 D[3] |
| Diamètre moléculaire | 0,460 nm[3] |
| Propriétés physiques | |
| T° fusion | −95,1 °C[1] |
| T° ébullition | 40 °C[1] |
| Paramètre de solubilité δ | 20,2 J1/2 cm−3/2 (25 °C)[3] |
| Miscibilité | Non miscible avec l'eau
miscible dans l'acétone, l'éther et autres solvants. |
| Masse volumique | 1,33 g cm−3[1] |
| T° d'auto-inflammation | 556 °C[1] |
| Limites d’explosivité dans l’air | 12–25 %vol[1] |
| Pression de vapeur saturante | à 20 °C : 47,4 kPa[1] |
| Viscosité dynamique | 0,44 cP à 20 °C[réf. souhaitée] |
| Point critique | 63,0 bar, 236,85 °C[4] |
| Thermochimie | |
| S0liquide, 1 bar | 174,5 J/(mol·K)[5] |
| ΔfH0liquide | −124,3 kJ/mol[5] |
| Cp | |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 11,32 ± 0,01 eV (gaz)[7] |
| Propriétés optiques | |
| Indice de réfraction | 1,421[3] |
| Précautions | |
| SGH[8] | |
 Attention |
|
| SIMDUT[9] | |
 D1B, D2A, D2B, |
|
| NFPA 704 | |
| Transport | |
| Classification du CIRC | |
| Groupe 2B : Peut-être cancérogène pour l'Homme[10] | |
| Écotoxicologie | |
| LogP | 1,25[1] |
| DJA | 0,05 mg/kg p.c./j[11] |
| Seuil de l’odorat | bas : 1,2 ppm haut : 440 ppm[12] |
| Composés apparentés | |
| Autres composés |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Il est surtout utilisé comme solvant de composés organiques.
Histoire
Le dichlorométhane a été isolé pour la première fois en 1840 par le chimiste français Henri Victor Regnault, qui l'a isolé d'un mélange de chlorométhane et de chlore précédemment exposé à la lumière.
Production industrielle
Le dichlorométhane est produit par réaction du chlorométhane ou du méthane avec le chlore gazeux entre 400 °C et 500 °C.
À ces températures, le méthane, comme le chlorométhane subissent une série de réactions qui forment progressivement des produits de plus en plus chlorés :
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCl4 + HCl
Le résultat de cette série de réactions est un mélange de chlorométhane, dichlorométhane, chloroforme et tétrachlorométhane. Ces composés sont ensuite séparés par distillation.
Le dichlorométhane est instable ; il se décompose à 120 °C et notamment au contact de surfaces chaudes ou en présence d'une flamme (en produisant des composés dangereux chlorure d'hydrogène, phosgène, monoxyde et dioxyde de carbone. Il s’oxyde et se dégrade lentement dans l'air sec, et plus vite en présence d'eau et/ou de lumière. Dans l'eau froide, il s'hydrolyse en produisant de l'acide chlorhydrique, ce phénomène n'est toutefois pas significatif[14]. À partir de 180 °C, toujours dans l'eau, il forme également de l'acide formique, du chlorométhane, du méthanol et un peu de monoxyde de carbone.
Les industriels de la chimie le stabilisent souvent en lui ajoutant une faible quantité d'additifs (moins de 1 %) qui sont généralement des composés phénoliques, des amines, amylène, cyclohexane, époxydes, etc.).
Caractéristiques chimiques
- Peu soluble dans l’eau (13 à 20 g/L à 20 °C).
- Miscible avec la plupart des solvants organiques.
- Solvant efficace sur de nombreux produits organiques (graisses, huiles, résines, etc.).
- Réagit violemment (explosion possible en présence de certains catalyseurs courants ou d'autres solvants chlorés) avec des poudres métalliques (aluminium, magnésium), et réagit spontanément et fortement avec les métaux alcalins, les bases fortes et les oxydants puissants.
Usages


Son caractère volatil et sa capacité à dissoudre de nombreux composés organiques font du dichlorométhane un solvant idéal pour de nombreux procédés chimiques.
Il a principalement été utilisé ou l'est encore comme :
- intermédiaire de synthèse, par l'industrie chimique ;
- constituant de décapants pour peinture et vernis ;
- dégraissant industriel ou domestique (pour le bricolage) ;
- solvant extracteur de molécules organiques utilisé par l'industrie pharmaceutique, agroalimentaire et des cosmétiques (il est fréquemment utilisé pour la décaféination du café vert ainsi que pour l'extraction de la caféine ou pour préparer divers arômes (dont le houblon), mais peut être parfois remplacé par l'extraction au CO2 supercritique, moins toxique) ;
- solvant de polymérisation (dont pour la production de polycarbonates) ;
- gaz utilisé par l'industrie de l'imprimerie sur vêtements pour l'enlèvement des transferts à chaud ;
- gaz propulseur pour certains sprays ;
- agent moussant, par exemple pour obtenir la mousse de polyuréthane ;
- pesticide gazeux (pour traiter les stocks de fraises et les céréales) ;
- colles : il « fond » (se combine avec) de nombreux plastiques, aussi est-il utilisé pour la « soudure chimique » de certains plastiques (par exemple pour sceller le boitier de compteurs électriques). C'est l'un des composants principaux des adhésifs vendus pour le collage par soudure de plastique. Dans la fabrication de maquettes, par exemple, il est utilisé pour fixer ensemble les composants en plastique (Les maquettistes l'appellent parfois « Di-clo ») ;
- sa volatilité est exploitée pour animer certains articles de fantaisie (oiseau buveur, lampes décoratives de type Bubble light et affichages de jukebox…) ;
- il sert aussi dans le domaine d'essais techniques de matériaux de génie civil (matériaux bitumineux) comme solvant permettant de séparer le liant de l'ensemble d'une bitume (ou macadam) pour permettra de tester ces matériaux[15] ;
- en impression 3D, il est utilisé pour lisser les modèles en PETG ;
- parmi ses autres usages, il sert à produire des fibres cellulosiques, entre dans la composition de peintures,
est utilisé par l'industrie pétrolière, l'industrie du cuir, dans certains détachants textiles, comme solvant par les laboratoires d’analyses chimiques, etc.
En raison de la toxicité relative, on a toutefois cherché des alternatives à la plupart de ces applications.
Risques et dangers
Toxicité : le dichlorométhane est réputé être le moins toxique des chlorohydrocarbones simples, mais il est néanmoins toxique.
- Son caractère très volatil explique un risque d'intoxication aigüe ou chronique par inhalation[16].
- Le dichlorométhane est métabolisé en monoxyde de carbone par l'organisme qui peut alors subir une intoxication au monoxyde de carbone[17].
- Selon la littérature médicale, une exposition aigüe par inhalation peut mener à une neuropathie optique sévère[18] et à une attaque du foie (hépatite)[19].
- Le contact prolongé avec la peau peut provoquer des irritations ou des brûlures chimiques par dissolution des tissus adipeux[20].
- C'est une substance classée par le Centre international de recherche sur le cancer (CIRC) comme Cancérigène classe 2B, c'est-à-dire « l’agent est peut-être cancérigène pour l’homme ». En effet, il est bien cancérigène chez la souris, mais en raison d'un mécanisme spécifique à la souris, impliquant une protéine absente chez l'homme[21]. À ce jour, aucune étude n'a pu montrer ni contredire avec certitude un caractère cancérigène effectif chez l'Homme. Par contre, chez l'animal de laboratoire, il a été associé à des cancers du poumon, cancer du foie et cancer du pancréas[22].
- Le dichlorométhane traverse la barrière placentaire, mais sa toxicité éventuelle pour le fœtus chez les femmes qui y sont exposés pendant la grossesse n'a pas été prouvée[23]. Cependant, l'expérimentation animale le montre fœtotoxique aux doses qui sont toxiques pour la mère.
Aucun effet tératogène n'a été détecté à ce jour[22].
Précaution, information
Dans beaucoup de pays, les produits contenant du dichlorométhane doivent porter des étiquettes avertissant de ses dangers pour la santé. Toutefois, on le confond souvent avec l'essence de térébenthine ou le white spirit, qui présente moins de risques notamment pour la peau.
Dans l'Union européenne, l'usage de dichlorométhane dans les décapants a été interdit pour les consommateurs, et pour de nombreux professionnels[24].
Couche d'ozone
Du fait de sa courte vie, le dichlorométhane n'a pas été pris en compte dans le protocole de Montréal. Cependant sa concentration a doublé entre 2004 et 2014 et le niveau atteint est mis en cause dans un nouveau risque d'agrandissement du trou dans la couche d'ozone[25],[26].
Notes et références
- DICHLOROMETHANE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1, EAN 978-0-471-98369-9, LCCN 98018212)
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- Modèle:Nist
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, 2 et 3, Huston, Texas, Gulf Pub., (ISBN 0-88415-857-8, 0-88415-858-6 et 0-88415-859-4).
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205.
- Fiche de sécurité fournie par Sigma-Aldrich, consultée le 28/09/2019
- « Chlorure de méthylène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2B : Peut-être cancérogènes pour l'homme », sur monographs.iarc.fr, CIRC, (consulté le )
- Concentrations/doses journalières admissibles et concentrations/doses tumorigènes des substances d'intérêt prioritaire calculées en fonction de critères sanitaires, publié par Santé Canada
- « Methylene chloride », sur hazmap.nlm.nih.gov (consulté le )
- Fiche toxicologique, INRS.
- « Dichlorométhane (fiche technique) » [PDF], p. 5
- The Shell Bitumen Handbook, Shell Bitumen.
- Rioux J.P. et Myers R.A., Methylene chloride poisoning: a paradigmatic review ; J. Emerg. Med. ; vol. 6, chap. 3, p. 227-238 ; 1988 ; , DOI:10.1016/0736-4679(88)90330-7.
- Fagin J., Bradley J. et Williams D. ; Carbon monoxide poisoning secondary to inhaling methylene chloride ; Br. Med. J., vol. 281, n° 6253 ; p. 1461 ; 1980 ; , DOI:10.1136/bmj.281.6253.1461.
- Kobayashi A., Ando A., Tagami N., Kitagawa M., Kawai E., Akioka M., Arai E., Nakatani T., Nakano S., Matsui Y. et Matsumura M., Severe optic neuropathy caused by dichloromethane inhalation, J. Ocul. Pharmacol. and Ther. ; vol. 24 ; chap. 6, p. 607–612, 2008 ; ; DOI:10.1089/jop.2007.0100.
- Cordes D.H., Brown W.D. et Quinn K.M., Chemically induced hepatitis after inhaling organic solvents ; West. J. Med. ; vol. 148, chap. 4 ; p. 458–460 ; 1988 ; .
- Wells G. et Waldron H., Methylene chloride burns, Br. J. Ind. Med., vol. 41, chap. 3, p. 420, 1984, .
- Pharmaceutical Technology Europe, 1996, 8 (10), 30-31.
- USDHHS, accessdate=2006-09-10 Toxicological Profile for Methylene Chloride [PDF].
- Bell B., Franks P., Hildreth N. et Melius J., Methylene chloride exposure and birthweight in Monroe County, New York, Journal Environ. Res., vol. 55, chap. 1, p. 31–9, 1991, , DOI:10.1016/S0013-9351(05)80138-0.
- http://www.europarl.europa.eu/news/expert/infopress_page/064-46096-012-01-03-911-20090113IPR46095-12-01-2009-2009-false/default_en.htm Dichloromethane to be banned in paint-strippers ; 2009-01-14, consulté 2009-01-15.
- Science et Vie, no 1200, septembre 2017.
- « Une autre menace sur la couche d'ozone », Pour la science, no 479, , p. 12
Voir aussi
Articles connexes
Liens externes
- Fiche toxicologique, INRS
- Fiche Internationale de Sécurité
- (en) Usages durables et recommandations de l'Industrie
- Portail de la chimie

