DIPSO
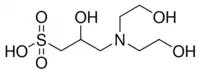
DIPSO est le nom courant de l'acide 3-(N,N-bis[2-hydroxyéthyl]amino)-2-hydroxypropanesulfonique, un acide sulfonique couramment utilisé comme tampon. C'est un composé faisant partie des tampons de Good[4], décrit et nommé en 1980. Son pKa de 7,6 à 25 °C[1] présente un certain intérêt pour des applications en biochimie, c'est d'ailleurs avec cet usage en tête qu'il a été synthétisé.
| DIPSO | |
| |
| Identification | |
|---|---|
| Nom UICPA | acide 3-(N,N-bis[2-hydroxyéthyl]amino)-2-hydroxypropanesulfonique |
| No CAS | |
| No ECHA | 100.063.610 |
| No CE | 269-992-2 |
| PubChem | 100210 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche[1] |
| Propriétés chimiques | |
| Formule | C7H17NO6S [Isomères] |
| Masse molaire[2] | 243,278 ± 0,014 g/mol C 34,56 %, H 7,04 %, N 5,76 %, O 39,46 %, S 13,18 %, |
| pKa | 7,6 à 25 °C[1] |
| Propriétés physiques | |
| T° fusion | 189 à 192 °C[1] |
| Précautions | |
| SGH[3] | |
 |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Applications
Le DIPSO est utilisé comme tampon en biologie et biochimie. Le pH d'une solution préparée avec du DIPSO dépend de la concentration et de la température[5], un effet que l'on peut prédire et calculer[6].
Faisant partie des tampons de Good, il répond à plusieurs des caractéristiques que celui-ci recherchait : il est assez soluble (environ 58,4 g/L dans l'eau à 0 °C[4]), son pKa le rend adapté à un usage en biologie, il est chimiquement stable et peu sujet à des réactions enzymatiques, présente une absorption négligeable dans le visible et le proche UV, et sa synthèse est relativement aisée.
Stéréochimie
L'atome de carbone C2, au centre de la partie propane du DIPSO et qui porte une fonction hydroxyle, est chiral. Le DIPSO se présente donc sous la forme d'une paire d'énantiomères dont le racémique porte le numéro CAS .
Références
- Fiche Sigma-Aldrich du composé DIPSO, consultée le 18 septembre 2018. + (pdf) fiche SDS.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- PubChem, CID 100210
- (en) Wilfred J. Ferguson, K.I. Braunschweiger, W.R. Braunschweiger et James R. Smith, « Hydrogen ion buffers for biological research », Analytical Biochemistry, vol. 104, no 2, , p. 300–310 (DOI 10.1016/0003-2697(80)90079-2, lire en ligne, consulté le )
- Lakshmi N. Roy, Rabindra N. Roy, Sean R. LeNoue et Cole E. Denton, « Buffer Standards for the Physiological pH of the Zwitterionic Compound, DIPSO from 5 to 55°C », Journal of Solution Chemistry, vol. 38, no 4, , p. 459–469 (ISSN 0095-9782, PMID 20160870, PMCID PMC2771870, DOI 10.1007/s10953-009-9379-2, lire en ligne, consulté le )
- « Biological buffers », REACH Devices
- Portail de la chimie