Bromodichlorométhane
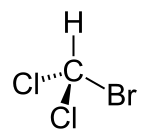
Le bromodichlorométhane est un trihalogénométhane de formule CHBrCl2. C'est un liquide incolore, lourd et non combustible formé par action du chlore sur des matières organiques.
| Bromodichlorométhane | |
| |
| Identification | |
|---|---|
| Nom UICPA | Bromodichlorométhane |
| Synonymes |
dichlorobromométhane |
| No CAS | |
| No ECHA | 100.000.779 |
| No CE | 200-856-7 |
| No RTECS | PA5310000 |
| PubChem | 6359 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore[1] |
| Propriétés chimiques | |
| Formule | CHBrCl2 [Isomères] |
| Masse molaire[2] | 163,829 ± 0,006 g/mol C 7,33 %, H 0,62 %, Br 48,77 %, Cl 43,28 %, |
| Propriétés physiques | |
| T° fusion | −57 °C[1] |
| T° ébullition | 90 °C[1] |
| Solubilité | 4,5 g l−1 (eau, 20 °C)[1] |
| Masse volumique | 1,980 g cm−3[1] |
| Point d’éclair | imcombustible[1] |
| Pression de vapeur saturante | 67 mbar (20 °C)[1] |
| Propriétés optiques | |
| Indice de réfraction | 1,497[3] |
| Précautions | |
| SGH[3] | |
   |
|
| NFPA 704[3] | |
| Transport[1] | |
| Écotoxicologie | |
| DL50 | 450 mg/kg (souris, oral)[4] 430 mg/kg (rat, oral)[5] |
| LogP | 2[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
Occurrence et production
Le bromodichlorométhane est principalement un produit secondaire de la chloration de l'eau. Il est parfois présent dans l'eau du robinet à l'état de trace (taux inférieur à 1 µg/l) par le traitement de l'eau potable[6], à un seuil jugé inoffensif pour l'organisme.
De petites quantités sont produites dans les usines chimiques pour être utilisées en laboratoire ou pour créer d'autres substances chimiques. Une très petite quantité (moins de 1 % de la quantité produite par les activités humaines) est produite par les algues dans les océans.
Le bromodichlorométhane s'évapore très facilement, la plus grande partie du bromodichlorométhane présent dans l’atmosphère y est entré par évaporation depuis les usines chimiques et les centres de traitement des eaux. Le bromodichlorométhane se dégrade lentement (environ 90 % en un an) par des réactions chimiques dans l’air. Le bromodichlorométhane qui reste présent dans l'eau ou le sol est dégradé lentement par des bactéries.
Utilisations
Il a été utilisé comme retardateur de flamme, solvant pour graisses et cires et, à cause de sa grande densité, comme séparateur de minéraux. Il est maintenant utilisé comme réactif et apparaît comme intermédiaire en chimie organique.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Bromodichloromethane » (voir la liste des auteurs).
- (es) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en espagnol intitulé « Bromodiclorometano » (voir la liste des auteurs).
- Entrée « Bromodichloromethane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 7 août 2012 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Bromodichloromethane, consultée le 7 août 2012.
- Toxicology and Applied Pharmacology, vol. 44, p. 213, 1978 (Pubmed.
- Science Reports of the Research Institutes, Tohoku University, Series C: Medicine, vol. 36(1-4), p. 10, 1989.
- A titre indicatif, le taux maximal de dichloromonobromométhane autorisé par le ministère français de la Santé est de 100 µg/l d'eau,
Voir aussi
- BROMODICHLOROMETHANE, Fiches internationales de sécurité chimique
- (en) Bromodichloromethane at The Carcinogenic Potency Database
- (en) Toxicological Profile at ATSDR
- (en) Bromodichloromethane MSDS
- Portail de la chimie

