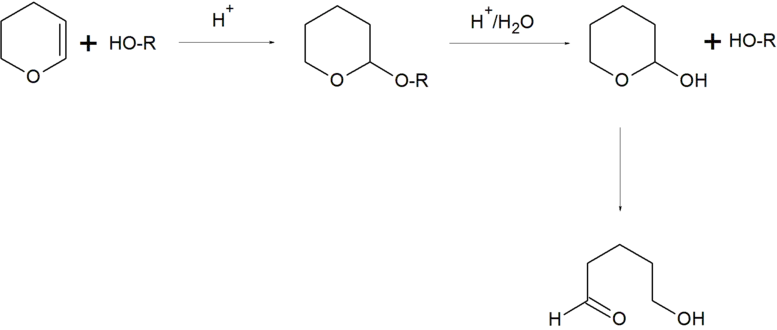Dihydropyrane
Le dihydropyrane est un composé organique hétérocyclique insaturé de formule brute C5H8O. Le cycle est formé de cinq atomes de carbone et d'un hétéroatome d'oxygène. Il contient une double liaison, dont l'emplacement sur le cycle détermine deux isomères :
 3,4-Dihydro-2H-pyrane.
3,4-Dihydro-2H-pyrane. 3,6-Dihydro-2H-pyrane.
3,6-Dihydro-2H-pyrane.
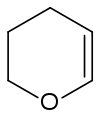
| 3,4-Dihydro-2H-pyrane | |
| |
| Structure du 3,4-dihydro-2H-pyrane | |
| Identification | |
|---|---|
| Nom UICPA | 3,4-dihydro-2H-pyrane |
| No CAS | |
| No ECHA | 100.003.465 |
| No CE | 203-810-4 |
| PubChem | 8080 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H8O [Isomères] |
| Masse molaire[1] | 84,116 4 ± 0,004 9 g/mol C 71,39 %, H 9,59 %, O 19,02 %, |
| Propriétés physiques | |
| T° fusion | −70 °C[2] |
| T° ébullition | 89 °C[2] |
| Solubilité | 20 g·L-1[2] à 20 °C |
| Masse volumique | 0,927 g·cm-3[2] à 20 °C |
| T° d'auto-inflammation | 243 °C[2] |
| Point d’éclair | −9 °C[2] |
| Pression de vapeur saturante | 12 kPa[2] à 20 °C |
| Précautions | |
| SGH[2] | |
  Danger |
|
| Transport[2] | |
| Composés apparentés | |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
La double liaison est en position 5 dans le 3,4-dihydro-2H-pyrane et en position 4 dans le 3,6-dihydro-2H-pyrane. Ainsi le 3,4-dihydro-2H-pyrane peut être vu comme un éther d'énol, contrairement au 3,6-dihydro-2H-pyrane.
Préparation
Le 3,4-dihydro-2H-pyrane est préparé par déshydratation de l'alcool tétrahydrofurfurylique (THFA) sur l'alumine de 300 à 400 °C[3] :
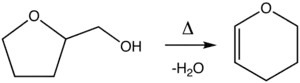
Utilisation
Le dihydropyrane est utilisé comme groupe protecteur de groupes alcool en synthèse organique[4],[5]. La réaction d'un alcool avec le dihydropyrane forme un éther de tétrahydropyranyle, qui protège le groupe alcool d'un grand nombre de réactions :
L'alcool peut être rétabli ultérieurement par hydrolyse acide avec formation de 5-hydroxypentanal.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Dihydro-3,4-2H pyranne » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 8 juillet 2016 (JavaScript nécessaire)
- (en) R.L. Sawyer, D.W. Andrus, Nathan L. Drake et Charles M. Eaker, « 2,3-Dihydropyran », Organic Syntheses, vol. 23, , p. 25 (DOI 10.15227/orgsyn.023.0025, lire en ligne)
- (en) R.A. Earl, L.B. Townsend, G. Saucy et G. Weber, « Methyl 4-hydroxy-2-butynoate », Organic Syntheses, vol. 60, , p. 81 (DOI 10.15227/orgsyn.060.0081, lire en ligne)
- (en) Arthur F. Kluge, A. Pilli, Kenneth S. Kirshenbaum, Clayton H. Heathcock et K. Barry Sharpless, « Diethyl[(2-tetrahydropyranyloxy)methyl]phosphonate », Organic Syntheses, vol. 64, , p. 80 (DOI 10.15227/orgsyn.064.0080, lire en ligne)
- Portail de la chimie