Oxyde d'iridium(IV)
L'oxyde d'iridium(IV) ou dioxyde d'iridium[1] est le composé chimique de formule IrO2. Il cristallise dans la structure du rutile, avec six atomes d'oxygène coordonnés et trois d'iridium coordonnés[7]
Pour les articles homonymes, voir Oxyde d'iridium.
| Oxyde d'iridium(IV) | |
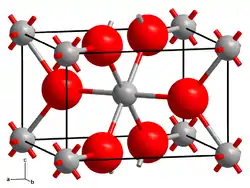
| |
| __ Ir4+ __ O2− | |
| Identification | |
|---|---|
| Nom UICPA | dioxoiridium[1] |
| No CAS | (dihydrate) |
| No ECHA | 100.031.572 |
| PubChem | 82821 |
| SMILES | |
| InChI | |
| Apparence | poudre noire inodore[2] poudre bleue/noire (dihydrate)[3] |
| Propriétés chimiques | |
| Formule | IrO2 [Isomères] |
| Masse molaire[4] | 224,216 ± 0,004 g/mol Ir 85,73 %, O 14,27 %, |
| Propriétés physiques | |
| T° fusion | se transforme au-dessus de 1 200 °C en trioxyde d'iridium[3] |
| Solubilité | eau : insol.[5] |
| Masse volumique | 11,7 g·cm-3[2] |
| Cristallographie | |
| Système cristallin | tétragonal |
| Classe cristalline ou groupe d’espace | P42/mnm[6] (no 136) |
| Paramètres de maille | a = 449,83 pm, c = 354,4 pm, Z = 2 |
| Précautions | |
| SGH[2] | |
 |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Il est utilisé avec d'autres oxydes rares dans le revêtement d'anodes pour l'électrolyse industrielle et dans des microélectrodes (en) utilisées pour la recherche en électrophysiologie[8].
Il peut être obtenu par oxydation de noir d'iridium, une poudre très fine d'iridium métallique
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Iridium(IV) oxide » (voir la liste des auteurs).
- (en) 82821 sur PubChem.
- Fiche Iridium(IV)-oxide chez AlfaAesar.
- A. F. Holleman, E. Wiberg, N. Wiberg, Lehrbuch der Anorganischen Chemie,102e Ed., de Gruyter, Berlin, 2007, p.1702. (ISBN 978-3-11-017770-1).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Iridium(IV)-oxide chez Acros.
- (de) Jean d' Ans et Ellen Lax, Taschenbuch für Chemiker und Physiker, , 1463 p. (ISBN 978-3-540-60035-0, lire en ligne), p. 496.
- (en) Norman N. Greenwood et Alan Earnshaw, Chemistry of the Elements, Butterworth-Heinemann, (ISBN 0080379419).
- (en) Stuart F. Cogan, « Neural Stimulation and Recording Electrodes », Annual Review of Biomedical Engineering, vol. 10, no 1, , p. 275–309 (DOI 10.1146/annurev.bioeng.10.061807.160518).
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.