Fisétine
La fisétine ou fisétol est un composé organique de la famille des flavonols, une sous-famille des flavonoïdes.
| Fisétine | |
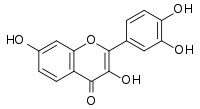
| |
| Identification | |
|---|---|
| Nom UICPA | 3,3',4',7-tétrahydroxy-2-phénylchromèn-4-one |
| Synonymes |
Fustel |
| No CAS | |
| No ECHA | 100.007.669 |
| PubChem | 5281614 |
| Apparence | aiguilles jaunes[1] |
| Propriétés chimiques | |
| Formule | C15H10O6 [Isomères] |
| Masse molaire[2] | 286,236 3 ± 0,014 5 g/mol C 62,94 %, H 3,52 %, O 33,54 %, |
| Propriétés physiques | |
| T° fusion | 330 °C[3] |
| Solubilité | insoluble dans l'eau, soluble dans l'éthanol |
| Précautions | |
| Directive 67/548/EEC | |
| Écotoxicologie | |
| DL50 | 180 mg·kg-1 (souris, i.v.)[4] |
| LogP | 1,180[3] |
| Unités du SI et CNTP, sauf indication contraire. | |
Ce composé est utilisé comme teinture jaune/brune. Sa structure a été découverte par le chimiste autrichien Josef Herzig (1853–1924) qui l'a identifiée dans le fustet ou arbre à perruques (Cotinus coggygria, Fisetholz en allemand d'où son nom). Elle est aussi naturellement présente dans certains arbres du genre Acacia, Acacia greggii[5], Acacia berlandieri[5], dans le Butea monosperma (palash, flamme de la forêt), dans le Quebracho colorado, dans les plantes du genre Rhus[6] et dans le cyprès de Nootka (Xanthocyparis nootkatensis). Elle serait aussi présente dans les mangues et dans les fraises.
Propriétés
Diluée dans une solution d'éthanolate de sodium, la fisétine présente une fluorescence vert foncé.
Effets biologiques
La fisétine est légèrement toxique, et potentiellement mutagène. Elle réduit cependant la toxicité des aflatoxines
Applications médicales
La fisétine est un puissant activateur de sirtuine[7]. C'est par conséquent un puissant mimétique de la restriction calorique, agissant ainsi contre les effets du vieillissement.
Une étude de P. Maher et al. montre que la fisétine aurait aussi une action bénéfique sur la mémoire à long terme[8].
Une nouvelle étude de P. Maher et al. sur des souris Akita (génétiquement prédisposées au diabète) montre qu'un régime riche en fraises (un fruit riche en fisétine) réduit les symptômes de diabète et de l'activité inflammatoire liée au cancer[9].
Notes et références
- J. Falbe, M. Regitz (Hrsg.): Römpp Lexikon Chemie. 10. Auflage. Thieme, Stuttgart u. New York 1996–1999, S. 1347.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Fisétine », sur ChemIDplus
- U.S. Army Armament Research & Development Command, Chemical Systems Laboratory, NIOSH Exchange Chemicals. Vol. NX#01998
- Chemistry of Acacia's from South Texas
- Antibacterial Effect of Fisetin and Fisetinidin, M. Gabor & E. EperJessy, 1966
- (en) David A. Sinclair et al. « Discover Three Classes of Molecules that Activate Sirtuins (Including Resveratrol »)
- (en) P. Maher et al. « Flavonoid fisetin promotes ERK-dependent long-term potentiation and enhances memory » Proceedings of the National Academy of Sciences of the United States of America 103(44) (2006), pp. 16568-16573.
- (en) « Fisetin Lowers Methylglyoxal Dependent Protein Glycation and Limits the Complications of Diabetes », P. Maher et al., 2011
- Portail de la chimie