gamma-Glutamylcystéine
La L-γ-glutamyl-L-cystéine, parfois abrégée en γ-Glu-Cys, est un dipeptide intermédiaire de la synthèse du glutathion résultant de la liaison entre un résidu glutamate et un résidu cystéine par la glutamate-cystéine ligase (EC ) ; elle est utilisée par la glutathion synthétase (EC ) pour former le glutathion. La liaison peptidique entre ces deux acides aminés est inhabituelle en ce qu'elle fait intervenir le carboxyle γ du glutamate, et non le carboxyle α, ce qui confère à cette molécule une meilleure stabilité par rapport au clivage par les peptidases.
| γ-Glutamylcystéine | |
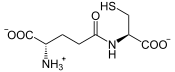 Structure de la L-γ-glutamyl-L-cystéine |
|
| Identification | |
|---|---|
| Synonymes |
γ-Glu-Cys |
| No CAS | |
| No ECHA | 100.164.128 |
| PubChem | 123938 |
| ChEBI | 17515 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C8H14N2O5S [Isomères] |
| Masse molaire[1] | 250,272 ± 0,014 g/mol C 38,39 %, H 5,64 %, N 11,19 %, O 31,96 %, S 12,81 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Le groupe sulfhydryle de la γ-Glu-Cys est moins sensible à l'oxydation spontanée que celui de la cystéine, mais plus sensible que celui du glutathion, lequel représente une meilleure forme de stockage de soufre réduit dans la cellule. Comme le glutathion, la γ-Glu-Cys peut dimériser en formant un pont disulfure et ainsi jouer le rôle d'antioxydant cellulaire. Des organismes tels que les halobactéries utilisent ainsi la γ-Glu-Cys à la place du glutathion, qu'ils ne synthétisent pas.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Human Metabolome Database « Showing metabocard for Gamma-Glutamylcysteine (HMDB01049) »
- Portail de la biochimie
- Portail de la chimie