Guanidine
La guanidine est un composé cristallin formé lors de l'oxydation de la guanine. Elle est utilisée dans la production de plastiques et d'explosifs. Elle se trouve également dans l'urine, étant un produit du métabolisme.
| Guanidine | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| No CAS | ||
| No ECHA | 100.003.656 | |
| Code ATC | A07 | |
| SMILES | ||
| InChI | ||
| Apparence | déliquescent | |
| Propriétés chimiques | ||
| Formule | CH5N3 [Isomères] |
|
| Masse molaire[1] | 59,070 5 ± 0,001 8 g/mol C 20,33 %, H 8,53 %, N 71,14 %, |
|
| Propriétés physiques | ||
| T° fusion | 50 °C | |
| T° ébullition | décomposition à 160 °C | |
| Solubilité | soluble dans l'eau, l'alcool | |
| Écotoxicologie | ||
| DL50 | souris : 350 mg·kg-1 | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Elle n'est pas commercialisée telle quelle, mais sous forme de sel (chlorhydrate, acétate, carbonate, etc.). Elle peut également céder un proton. Son pKa est de l'ordre de 20.
Utilisation
Les sels de guanidine comme le thiocyanate de guanidinium sont des agents chaotropiques qui déstabilisent les interactions faibles impliquées dans la structure spatiale des protéines. Pour cette raison, ils sont utilisés pour provoquer la dénaturation des protéines.
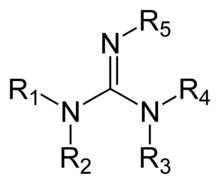 structure générale d'une guanidine |  Guanidine pour usage au laboratoire. |
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.