Hémagglutinine
L’hémagglutinine (HA) est une glycoprotéine antigénique présente à la surface du virus de la grippe, et est responsable de la fixation de la particule virale à un récepteur situé sur la cellule cible. Le nom hémagglutinine provient de la faculté de la protéine à agglomérer les érythrocytes hématiques (Nelson 2005).
Le terme hémagglutinine est aussi employé pour une autre glycoprotéine agglutinant les érythrocytes via les résidus mannosyls (c'est une lectine), la concanavaline A, qui est le terme plus approprié (abréviation: ConA).
Sous-types
Il y a 18 types différents d'antigènes HA. Ces sous-types sont numérotés de H1 à H18. H16 a été découverte en 2005 sur les virus de grippe A, isolés sur des goélands à tête noire de Suède et de Norvège (Fouchier, 2005). H17 & H18 ont été quant à eux découverts respectivement en 2012 & 2013 sur des chauves-souris d'Amérique centrale[1],[2].
On trouve les trois premières hémagglutinines H1, H2 et H3 sur les souches virales pathogènes de grippe humaine.
Fonctions et mécanismes d’action
L’HA a deux fonctions principales :
- la reconnaissance des cellules vertébrées cibles, accomplie lors de la fixation aux récepteurs de ces cellules contenant de l’acide sialique (cellules de l'épithélium pulmonaire) ;
- la fusion des membranes endosomales hôtes et virales (White 1997), accomplie par le recrutement des molécules HA par le site hôte de fusion, où certaines de ces molécules entreprennent des altérations de conformation déstabilisant la double couche lipidique hôte, ce qui conduit à la formation conjointe d'un intermédiaire de fusion associant les deux doubles couches lipidiques.
Dès la fusion opérée, la membrane cellulaire conjointe se retend, la coque virale s'ouvre directement sur le cytoplasme hôte, et le matériel génétique viral est injecté dans la cellule hôte où il va pouvoir se reproduire.
Structure
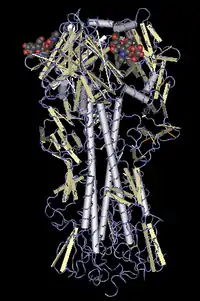
L’HA est une glycoprotéine homotrimérique intégrante de la membrane. De forme cylindrique, elle mesure environ 135 Å de long. Les trois monomères identiques qui constituent l’HA sont groupés en une spirale centrale alpha-hélicoïdale ; trois têtes sphériques contiennent les sites de fixation de l’acide sialique cible.
Les monomères HA sont d’abord synthétisés comme précurseurs, puis sont alors glycosylatés et découpés en deux polypeptides plus petits : les sous-unités HA1 et HA2. Chacun des trois monomères HA consiste en une longue chaine hélicoïdale, ancrée à la membrane par HA2 et surmontée par un large globule HA1.
Références
- Université de Strasbourg
- (en) Fouchier R.A.M., Munster V., Wallensten A. et al., 2005. Characterization of a novel influenza A virus hemagglutinin subtype (H16) obtained from black-headed gulls'. Paru dans J. Virology. vol. 79, no 5, p. 2814-22.
- (en) Nelson D.L. et Cox M.M., 2005. Lehninger’s Principles of Biochemistry, 4e édition, WH Freeman, New York, NY, États-Unis
- (en) Weis W.I., Brünger A.T., Skehel J.J. et al., 1990. Refinement of the influenza virus hemagglutinin by simulated annealing. Paru dans J. Molecular Biology vol. 212, p. 737-761.
- (en) White J.M., Hoffman L.R., Arevalo J.H. et al., 1997. Attachment and entry of influenza virus into host cells. Pivotal roles of hemagglutinin. Paru dans Structural Biology of Viruses, Chiu W., Burnett R.M. et Garcea R.L., éditeurs. Oxford University Press, NY, États-Unis p. 80-104.
Voir aussi
Articles connexes
Références
- Tong S, Li Y, Rivailler P, Conrardy C, Castillo DA, Chen LM, Recuenco S, Ellison JA, Davis CT, York IA, Turmelle AS, Moran D, Rogers S, Shi M, Tao Y, Weil MR, Tang K, Rowe LA, Sammons S, Xu X, Frace M, Lindblade KA, Cox NJ, Anderson LJ, Rupprecht CE, Donis RO, « A distinct lineage of influenza A virus from bats », Proceedings of the National Academy of Sciences of the United States of America, vol. 109, no 11, , p. 4269–74 (PMID 22371588, PMCID 3306675, DOI 10.1073/pnas.1116200109, Bibcode 2012PNAS..109.4269T)
- Tong S, Zhu X, Li Y, Shi M, Zhang J, Bourgeois M, Yang H, Chen X, Recuenco S, Gomez J, Chen LM, Johnson A, Tao Y, Dreyfus C, Yu W, McBride R, Carney PJ, Gilbert AT, Chang J, Guo Z, Davis CT, Paulson JC, Stevens J, Rupprecht CE, Holmes EC, Wilson IA, Donis RO, « New world bats harbor diverse influenza A viruses », PLoS Pathogens, vol. 9, no 10, , e1003657 (PMID 24130481, PMCID 3794996, DOI 10.1371/journal.ppat.1003657)
- Portail de la médecine
- Portail de la virologie