Méthacrylate d'éthyle
Le méthacrylate d'éthyle est un composé chimique de formule CH2=CH(CH3)COOCH2CH3. C'est l'ester d'acide méthacrylique CH2=CH(CH3)COOH et d'éthanol CH3CH2OH. Il se présente sous la forme d'un liquide hautement inflammable, volatil et incolore, à l'odeur caractéristique. Son enthalpie de polymérisation est de −59,5 kJ/mol ou −521 kJ/kg[4]. Il est donc susceptible de polymériser de manière explosive, et est sensible à la lumière et à l'air. Il est par conséquent distribué avec des stabilisants.
| Méthacrylate d'éthyle | |
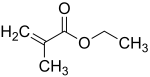
| |
| Structure du méthalylate d'éthyle | |
| Identification | |
|---|---|
| Nom UICPA | 2-méthylprop-2-énoate d'éthyle |
| No CAS | |
| No ECHA | 100.002.362 |
| No CE | 202-597-5 |
| No RTECS | OZ4550000 |
| PubChem | 7343 |
| SMILES | |
| InChI | |
| Apparence | liquide volatil incolore et inflammable formant des mélanges explosifs avec l'air[1] |
| Propriétés chimiques | |
| Formule | CH2=C(CH3)COOC2H5 |
| Masse molaire[2] | 114,142 4 ± 0,006 1 g/mol C 63,14 %, H 8,83 %, O 28,03 %, |
| Propriétés physiques | |
| T° fusion | −61 à −59 °C[1] |
| T° ébullition | 117 °C[1] |
| Solubilité | 5,1 g/L[1] à 20 °C |
| Masse volumique | 0,91 g/cm3[1] à 20 °C |
| T° d'auto-inflammation | 385 °C[1] |
| Point d’éclair | 19 °C[1] |
| Limites d’explosivité dans l’air | à partir de 1,37 % en volume (65 g/m3)[1] |
| Pression de vapeur saturante | 21,3 hPa[1] à 20 °C |
| Viscosité dynamique | 0,62 mPa s[1] à 20 °C |
| Précautions | |
| SGH[1] | |
  Danger |
|
| NFPA 704[3] | |
| Transport[1] | |
| Écotoxicologie | |
| DL50 | 14 800 mg/kg[1] (souris, oral) |
| Unités du SI et CNTP, sauf indication contraire. | |
Le méthacrylate d'éthyle est utilisé comme monomère pour produire des polymères acryliques[5], généralement par polymérisation radicalaire[6].
Notes et références
- Entrée « Ethyl methacrylate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 12 avril 2022 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fiche du composé Ethyl methacrylate, 98+%, stab. with 10-120ppm, 4-methoxyphenol », sur Alfa Aesar (consulté le ).
- (en) J. Brandrup, E. H. Immergut, E. A. Grulke, A. Abe et D. R. Bloch, Polymer Handbook, 4e éd., Wiley, 2003, p. II/369. (ISBN 978-0-471-47936-9)
- (en) William Bauer Jr., « Methacrylic Acid and Derivatives », Ullmann's Encyclopedia of Industrial Chemistry, (DOI 10.1002/14356007.a16_441.pub2, lire en ligne)
- (en) C. Granel, Ph. Dubois, R. Jérôme et Ph. Teyssié, « Controlled Radical Polymerization of Methacrylic Monomers in the Presence of a Bis(ortho-chelated) Arylnickel(II) Complex and Different Activated Alkyl Halides », Macromolecules, vol. 29, no 27, , p. 8576-8582 (DOI 10.1021/ma9608380, Bibcode 1996MaMol..29.8576G, lire en ligne)
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.

