n-Butylamine
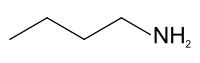
La n-butylamine est une amine de formule CH3-CH2-CH2-CH2-NH2. Ce composé fait partie des quatre isomères aminés dérivés du butane. Ces dérivés se nomment de manière générale des butylamines.
| n-Butylamine | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | butan-1-amine | |
| Synonymes |
1-aminobutane |
|
| No CAS | ||
| No ECHA | 100.003.364 | |
| PubChem | 8007 | |
| ChEBI | 43799 | |
| SMILES | ||
| InChI | ||
| Apparence | liquide incolore | |
| Propriétés chimiques | ||
| Formule | C4H11N [Isomères] |
|
| Masse molaire[1] | 73,136 8 ± 0,004 2 g/mol C 65,69 %, H 15,16 %, N 19,15 %, |
|
| Propriétés physiques | ||
| T° fusion | −49,15 °C[réf. souhaitée] | |
| T° ébullition | 76,9 à 78,9 °C[réf. souhaitée] | |
| Masse volumique | 0,74 g/cm3[réf. souhaitée] | |
| Viscosité dynamique | 500 µPa s à 20 °C[réf. souhaitée] | |
| Écotoxicologie | ||
| DL50 | 366 mg/kg (rats, oral) | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Propriétés
Ce liquide incolore a l'odeur typique des amines, celle de poisson pourri, ressemblant un peu à l'ammoniac. Il est soluble dans tous les solvants organiques.
Utilisation
Ce composé est utilisé comme ingrédient dans la fabrication de pesticides, de produits pharmaceutiques et d'émulsifiants.
Toxicologie
La dose létale médiane par exposition orale pour des rats est de 366 mg/kg. [réf. souhaitée]
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « N-Butylamine » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.