Nitrate de calcium
Le nitrate de calcium ou nitrate de calcium(II) ou dinitrate de calcium, aussi appelé Norgessalpeter (littéralement, salpêtre norvégien) ou Kalksalpeter, est un sel hygroscopique soluble de couleur blanche de formule chimique Ca(NO3)2 et de masse molaire 164,1 g/mol[3]. On le trouve souvent à l'état monohydraté, Ca(NO3)2 · H2O, avec une masse molaire de 182,11 g/mol[4]. Il est couramment utilisé comme réactif, fertilisant ou produit pyrotechnique.
| Nitrate de calcium | |||
Ca2+ 2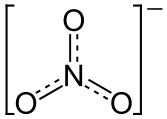 |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | Nitrate de calcium | ||
| Synonymes |
Dinitrate de calcium |
||
| No CAS | |||
| No ECHA | 100.030.289 | ||
| No CE | 233-332-1 | ||
| Apparence | cristaux incolores a blancs,hygroscopiques[1]. | ||
| Propriétés chimiques | |||
| Formule | Ca(NO3)2 | ||
| Masse molaire[2] | 164,088 ± 0,006 g/mol Ca 24,42 %, N 17,07 %, O 58,5 %, |
||
| Propriétés physiques | |||
| T° fusion | 560 °C[1] | ||
| Solubilité | dans l'eau : 1 212 g·l-1[1] | ||
| Masse volumique | 2,50 g·cm-3[1] | ||
| Précautions | |||
| Transport | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
Les engrais vendus sous le nom de nitrate de chaux sont composés de 70 à 100 % de nitrate de calcium tétrahydraté (n° CAS:13477-34-4) et de 7 à 10 % de nitrate d’ammonium (n° CAS:6484-52-2 [5].

2_dans_l'eau.png.webp)
Le nitrate de calcium hydraté existe à l'état naturel, sous le nom de nitrocalcite. Ce minéral apparaît sous forme d'efflorescences quand le jus (liviat) de fumier ou lisier, riche en nitrates, entre en contact avec du béton ou du calcaire dans un environnement sec, comme c'est le cas dans les écuries ou les grottes. On le récoltait autrefois pour les besoins militaires des poudreries.
C'est un sel qui facilite la pénétration de l'eau et de minéraux dans la plante. Très soluble dans l'eau, c'est aussi un puisant eutrophisant.
Le Norgessalpeter a été le premier engrais azoté à être industrialisé.
Production
Elle a débuté à Notodden, en Norvège, en 1905.
De nos jours, la majorité de la production mondiale de nitrate de calcium se fait à Porsgrunn[6]. Le nitrocalcite est une forme de nitrate de calcium que l'on retrouve à l'état naturel.
Voir aussi
Articles connexes
Bibliographie
- {...}
Liens externes
- {...}
Notes et références
- NITRATE DE CALCIUM, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Nitrate de calcium (II) »
- (en) « Calcium Nitrate - a Hydroculture Salt »
- Duclos international, Fiche de données de sécurité Nitrate de chaux (Conforme à la Directive 91/155/CEE de l'UE, telle qu'amendée par la Directive 2001/58/CE)
- « Nitrate de calcium, Porsgrunn »
- Portail de la chimie