Oxydation de Jones
L'oxydation de Jones est une réaction chimique décrite comme étant l'oxydation par l'acide chromique des alcools primaires en acides carboxyliques et des alcools secondaires en cétones[1],[2],[3],[4],[5].
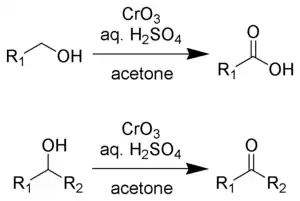
L'oxydation de Jones.
Le réactif de Jones, une solution de trioxyde de chrome dans de l'acide sulfurique concentré, est employé comme agent oxydant.
- L'acétone affecte sensiblement les propriétés de l'acide chromique.
- L'oxydation est très rapide, relativement exothermique, et les rendements sont généralement élevés.
- Le réactif oxyde rarement les liaisons insaturées.
- Les résidus chromés sont très toxiques, si bien que la prudence doit être de rigueur lors de l'utilisation de cette réaction.
La première demi-équation chimique de la réaction est : 2 CrO3 + 3 H2SO4 + 6 H+ + 6 e- → Cr2(SO4)3 + 6 H2O
La deuxième demi-équation chimique de la réaction est : 3 R2HC-OH → 3 R2C=O + 6 H+ + 6 e-
Références
- Bowden, K.; Heilbron, I. M.; Jones, E. R. H. J. Chem. Soc. 1946, 39.
- Heilbron, I.M.; Jones, E.R.H.; Sondheimer, F. J. Chem. Soc. 1949, 604.
- Bladon, P. et al. J. Chem. Soc. 1951, 2402.
- Jones, E. R. H. et al. J. Chem. Soc. 1953, 457 & 2548 & 3019.
- Djerassi, C. et al. J. Org. Chem. 1956, 21, 1547.
Voir aussi
- Chlorochromate de pyridinium
- Réactif de Collins
- Oxydation de Swern
- Oxydation de Sarett
- Oxydoréduction en chimie organique
- Oxydation d'un alcool
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.