Oxyde de triphénylphosphine
L'oxyde de triphénylphosphine (TPPO) est un composé chimique de formule OP(C6H5)3, ce qu'on abrège souvent en écrivant Ph3PO, « Ph » représentant un groupe phényle –C6H5. Il se présente sous la forme d'un solide cristallisé combustible incolore faiblement volatil à l'odeur désagréable et faiblement soluble dans l'eau. C'est un sous-produit fréquent dans les réactions impliquant la triphénylphosphine. Il est couramment utilisé pour induire la cristallisation de composés chimiques.
| Oxyde de triphénylphosphine | |
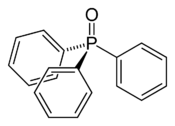 Structure de l'oxyde de triphénylphosphine |
|
| Identification | |
|---|---|
| Nom UICPA | triphényl-λ5-phosphanone, oxyde de triphénylphosphane |
| Synonymes |
diphénylphosphorylbenzène |
| No CAS | |
| No ECHA | 100.011.217 |
| No CE | 212-338-8 |
| No RTECS | SZ1676000 |
| PubChem | 13097 |
| ChEBI | 36601 |
| SMILES | |
| InChI | |
| Apparence | solide cristallisé blanc jaunâtre à l'odeur déplaisante |
| Propriétés chimiques | |
| Formule | C18H15OP |
| Masse molaire[1] | 278,284 9 ± 0,015 8 g/mol C 77,69 %, H 5,43 %, O 5,75 %, P 11,13 %, |
| Propriétés physiques | |
| T° fusion | 155 à 158 °C[2] |
| T° ébullition | > 360 °C[2] décomposition au-delà de 375 °C[2] |
| Solubilité | faiblement soluble à 20 °C[2] |
| Masse volumique | 1,2 g·cm-3[2] à 20 °C |
| T° d'auto-inflammation | 590 °C[2] |
| Point d’éclair | 180 °C[2] |
| Précautions | |
| SGH[2] | |
 Attention |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Structure et propriétés
La molécule présente une géométrie moléculaire tétraédrique semblable à celle du trichlorure de phosphoryle POCl3[3]. L'atome d'oxygène est relativement basique et l'ossature de la molécule est assez rigide, de sorte que l'oxyde de triphénylphosphine est un réactif commode pour cristalliser des composés qui seraient autrement plus difficiles à cristalliser, ce qui est notamment le cas des molécules possédant des atomes d'hydrogène acides, tels que les phénols[4].
Synthèse comme sous-produit de réaction
L'oxyde de triphénylphosphine est un sous-produit apparaissant au cours de nombreuses réactions utiles en synthèse organique, notamment les réactions de Wittig, de Staudinger et de Mitsunobu. Il se forme également lors de la conversion des alcools en chloroalcanes sous l'effet du PPh3Cl2 :
La triphénylphosphine PPh3 peut être régénérée à partir de l'oxyde de triphénylphosphine sous l'action du trichlorosilane SiHCl3 :
Il peut être difficile d'extraire l'oxyde de triphénylphosphine d'un mélange réactionnel par chromatographie ; il est cependant un peu soluble dans l'hexane et l'éther diéthylique froid, de sorte que la trituration ou la chromatographie de ces produits dans ces solvants permet généralement une bonne séparation du Ph3PO.
L'oxyde de triphénylphosphine est une impureté qu'on trouve fréquemment dans les échantillons de triphénylphosphine. L'oxydation de cette dernière par l'oxygène de l'air est catalysée par de nombreux ions métalliques :
Complexométrie
Ph3PO est un très bon ligand pour les centres métalliques « durs » au sens HSAB. Un exemple typique de tels édifices est le complexe tétraédrique dichloro-bis(oxyde de triphénylphosphine)-nickel(II) Cl2Ni(OPPh3)2[5].
nickel(II)-from-xtal-3D-balls.png.webp)
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Triphenylphosphine oxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 20 octobre 2013 (JavaScript nécessaire)
- (en) D. E. C. Corbridge, « Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology », Elsevier 5e édition, Amsterdam. (ISBN 0-444-89307-5).
- (en) Margaret C. Etter et Paul W. Baures, « Journal of the American Chemical Society », Triphenylphosphine oxide as a crystallization aid, vol. 110, no 2, , p. 639-640 (lire en ligne) DOI:10.1021/ja00210a076
- (en) D. M. L. Goodgame et M. Goodgame, « Near-Infrared Spectra of Some Pseudotetrahedral Complexes of Cobalt (II) and Nickel(II) », Inorganic Chemistry, vol. 4, no 2, , p. 139-143 (lire en ligne) DOI:10.1021/ic50024a002
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Triphenylphosphine oxide » (voir la liste des auteurs).
- Portail de la chimie