Peptidomimétique
Les peptidomimétiques sont des molécules organiques souvent utilisées en pharmacologie comme substitut de peptides actifs. Plusieurs stratégies peuvent être utilisées afin de concevoir un peptidomimétique: l'utilisation des acides aminés D au lieu de L afin de diminuer la vitesse de dégradation dans le corps, la synthèse de peptoïdes ou l'utilisation de β-peptides.
D-peptides
Les D-peptides sont non naturels dans le corps. Les enzymes chargés d'hydrolyser les peptides n'auront pas une affinité élevée envers les D-peptides vu la stéréochimie inversée des peptides anormalement rencontrés dans le corps. Ils ont aussi une réponse immunitaire faible, diminuant l'inflammation[1].
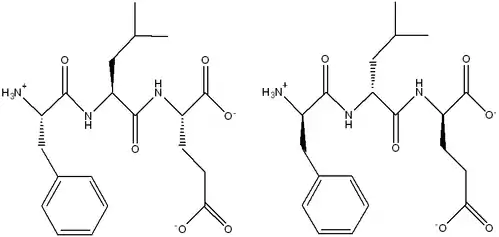
β-peptides
Les β-peptides sont des peptides ayant deux carbones entre le carbonyle de l'amide et l'azote de l'amide précédent. La structure en hélice serait plus stable que dans les peptides normaux[2].
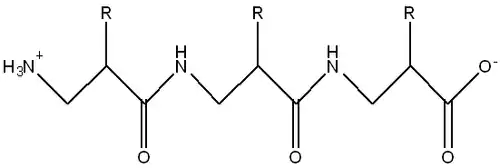
Peptoïdes
En général, les peptidomimétiques sont faits pour mimer certains peptides actifs tout en ayant une demi-vie plus longue dans l'organisme ou une affinité plus grande.
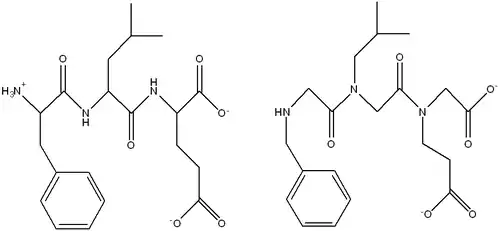
Synthèse
La synthèse d'un monomère de peptoïde passe par deux étapes subséquentes que l'on fait en série pour ajouter des unités. Cette approche de synthèse permet notamment d'exploiter avec facilité la chimie combinatoire, permettant une grande quantité de produits différents, utiles dans le criblage moléculaire.
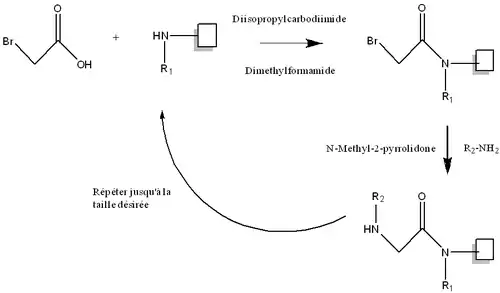
Notes et références
- (en) Brett D. Welch, Andrew P. VanDemark, Annie Heroux et Christopher P. Hill, « Potent D-peptide inhibitors of HIV-1 entry », Proceedings of the National Academy of Sciences, vol. 104, no 43, , p. 16828–16833 (ISSN 0027-8424 et 1091-6490, PMID 17942675, DOI 10.1073/pnas.0708109104, lire en ligne, consulté le )
- (en) K. Gademann, T. Hintermann et J. V. Schreiber, « Beta-peptides: twisting and turning », Current Medicinal Chemistry, vol. 6, no 10, , p. 905–925 (ISSN 0929-8673, PMID 10519905, lire en ligne, consulté le )
- Portail de la biochimie