Permanganate d'argent
Le permanganate d'argent (AgMnO4) peut être synthétisé par réaction entre le permanganate de potassium et le nitrate d'argent. Ce composé est utilisé dans les masques à gaz, il est aussi utilisé pour la synthèse de hollandite à l'argent[2],[3].
| Permanganate d'argent | |
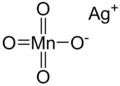
| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.029.127 |
| Apparence | cristaux violets monocliniques, décomposés par la lumière |
| Propriétés chimiques | |
| Formule | AgMnO4 [Isomères] |
| Masse molaire[1] | 226,803 8 ± 0,001 4 g/mol Ag 47,56 %, Mn 24,22 %, O 28,22 %, |
| Propriétés physiques | |
| Solubilité | 9,1 g·L-1 à 18 °C, plus soluble dans l'eau chaude, réagit avec l'éthanol |
| Masse volumique | 4,49 g·cm-3 |
| Unités du SI et CNTP, sauf indication contraire. | |
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- J. Chen, X. Tang, J. Liu, E. Zhan, J. Li, X. Huang, W. Shen, Chemistry of Materials 19 (2007) 4292-4299
- L. Li, D. King, Chemistry of Materials 17 (2005) 4335-4343
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.