Pustulose exanthématique aiguë généralisée
La pustulose exanthématique aigüe généralisée (PEAG) (également connue sous le nom d'éruption pustuleuse médicamenteuse ou de pustulodermie toxique) est une réaction cutanée rare qui, dans 90 % des cas, est liée à la prise de médicaments.
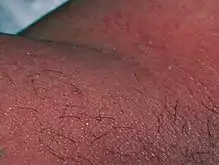
La PEAG se caractérise par des éruptions cutanées soudaines qui apparaissent en moyenne cinq jours après le début de la prise d'un médicament. Ces éruptions sont des pustules[1], c'est-à-dire de petites élévations rouges ou blanches de la peau qui contiennent une matière trouble ou purulente (pus)[2]. Les lésions cutanées disparaissent généralement dans les 1 à 3 jours suivant l'arrêt du médicament incriminé[3],[4]. Cependant, des cas plus graves sont associés à des troubles plus persistants pouvant se compliquer d'infections cutanées secondaires ou d'atteintes du foie, des poumons ou des reins[5].
Les troubles liés à une réaction cutanée indésirable grave (en) (SCAR) s'expliquent par une activation des lymphocytes T induite par un médicament qui déclenche ensuite des réponses immunitaires innées dirigées de manière inappropriée contre les tissus du soi. Des études sur le syndrome d'hypersensibilité médicamenteuse (DRESS), le syndrome de Stevens-Johnson (SJS), la nécrolyse épidermique toxique (TEN) et le chevauchement SJS/TEN indiquent que de nombreux individus sont prédisposés à développer ces réactions à un médicament particulier en fonction de leur expression génétique d'allèles d'antigènes de leucocytes humains (HLA) ou de récepteurs de cellules T particuliers et/ou de leur efficacité à adsorber, distribuer aux tissus, métaboliser et/ou éliminer un médicament particulier induisant des SCAR. Les preuves de ces prédispositions dans le cas de la PEAG n'ont pas été aussi bien établies[3],[6],[7] .
Notes et références
- (en) Khalel MH, Fattah Saleh SA, F El-Gamal AH, Najem N., « Acute generalized exanthematous pustulosis: an unusual side effect of meropenem », Indian J Dermatol., vol. 55, no 2, , p. 176-7. (PMID 20606889, PMCID PMC2887524, DOI 10.4103/0019-5154.62759, lire en ligne)
- James, William; Berger, Timothy; Elston, Dirk (2005). Andrews' Diseases of the Skin: Clinical Dermatology. (10th ed.). Saunders. (ISBN 0-7216-2921-0).:124
- Hoetzenecker W, Nägeli M, Mehra ET, Jensen AN, Saulite I, Schmid-Grendelmeier P, Guenova E, Cozzio A, French LE, « Adverse cutaneous drug eruptions: current understanding », Seminars in Immunopathology, vol. 38, no 1, , p. 75–86 (PMID 26553194, DOI 10.1007/s00281-015-0540-2, S2CID 333724)
- Feldmeyer L, Heidemeyer K, Yawalkar N, « Acute Generalized Exanthematous Pustulosis: Pathogenesis, Genetic Background, Clinical Variants and Therapy », International Journal of Molecular Sciences, vol. 17, no 8, , p. 1214 (PMID 27472323, PMCID 5000612, DOI 10.3390/ijms17081214)
- Alniemi DT, Wetter DA, Bridges AG, El-Azhary RA, Davis MD, Camilleri MJ, McEvoy MT, « Acute generalized exanthematous pustulosis: clinical characteristics, etiologic associations, treatments, and outcomes in a series of 28 patients at Mayo Clinic, 1996-2013 », International Journal of Dermatology, vol. 56, no 4, , p. 405–414 (PMID 28084022, DOI 10.1111/ijd.13434, S2CID 21325754)
- Halevy S, « Acute generalized exanthematous pustulosis », Curr Opin Allergy Clin Immunol, vol. 9, no 4, , p. 322–8 (PMID 19458527, DOI 10.1097/ACI.0b013e32832cf64e, S2CID 205434868)
- Garon SL, Pavlos RK, White KD, Brown NJ, Stone CA, Phillips EJ, « Pharmacogenomics of off-target adverse drug reactions », British Journal of Clinical Pharmacology, vol. 83, no 9, , p. 1896–1911 (PMID 28345177, PMCID 5555876, DOI 10.1111/bcp.13294)
Voir aussi
Article connexe
Liens externes
- Ressources relatives à la santé :
- Orphanet
- (en) Medical Subject Headings
- (en) NCI Thesaurus
- Portail de la médecine