Rifabutine
La rifabutine est une molécule antibiotique de la classe des rifamycines.
| Rifabutine | ||
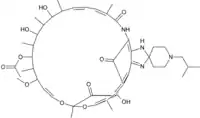
| ||
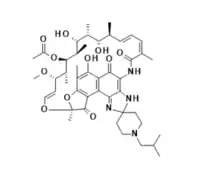 | ||
| Identification | ||
|---|---|---|
| No CAS | ||
| No ECHA | 100.133.627 | |
| Code ATC | J04 | |
| SMILES | ||
| InChI | ||
| Apparence | poudre violette | |
| Propriétés chimiques | ||
| Formule | C46H62N4O11 [Isomères] |
|
| Masse molaire[1] | 847,004 7 ± 0,045 2 g/mol C 65,23 %, H 7,38 %, N 6,61 %, O 20,78 %, |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
Elle fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[2].
Historique
La rifabutine a pour la première fois été synthétisée par Marsili et al. en 1981[3], par condensation de la 1-isobutyl-4-pipéridone avec la rifamycine S. Cette dernière est elle-même dérivée de la rifamycine B, un produit de fermentation (historiquement) issu d’Amycolatopsis mediterranei :[4] la rifabutine est donc une molécule hémisynthétique.
.png.webp)
Concernant sa commercialisation, la rifabutine a obtenu son autorisation de mise sur le marché (AMM) en 1993, sous le nom de princeps Ansatipine[5]. La rifabutine existe également sous le nom de spécialité Mycobutin.
Spectre d'action
La rifabutine possède un large spectre d'action[6]. Celle-ci est active contre des mycobactétries (Mycobacterium avium complex, Mycobacterium tuberculosis, Mycobacterium leprae). La rifabutine est également active contre un certain nombre de bactéries Gram positif telles que Staphylococcus aureus et Streptococcus pyogenes. Elle possède aussi une activité contre certaines bactéries Gram négatif comme Neisseria meningitidis, Helicobacter pylori, Chlamydia trachomatis et Pseudomonas aeruginosa.[7]Il est même rapporté une activité antiparasitaire, contre Toxoplasma gondii.
Données pharmacologiques
Pharmacodynamie
Comme les autres membres de la classe des rifamycines, le mécanisme d’action de la rifabutine passe par une inhibition de l’ARN polymérase ADN-dépendante de la bactérie. Cette inhibition est due à une gêne stérique occasionnée par l’agent thérapeutique lors de son interaction avec l’enzyme : la polymérisation des nucléosides triphosphate de l’amorce se trouve bloquée, empêchant ainsi la poursuite de la synthèse de l’ARN bactérien[8]. De par ce mécanisme, la rifabutine est bactéricide.
Absorption
La rifabutine présente un facteur de biodisponibilité d'environ 20 %. Cette faible valeur est sûrement due à une grande excrétion biliaire et un effet de premier passage hépatique[9].
Distribution
Du fait de son caractère lipophile, la rifabutine se distribue largement dans les tissus. La molécule possède ainsi un volume de distribution de 9,3 L/kg[10].
Métabolisation

Le temps de demi-vie de la rifabutine est de 45 heures en moyenne[11]. Elle est lentement mais fortement métabolisée, avec possiblement une vingtaine de métabolites formés. Deux d'entre eux ont été identifiés dans la plasma : la 25-O-désacetyl-rifabutine, correspondant à l'hydrolyse de la fonction ester en position 25 et la 31-hydroxy-rifabutine, obtenue par oxydation du groupement méthyle en position 31. Ces métabolites possèdent une activité antibiotique.
Utilisation pharmaceutique
Indications
La rifabutine est indiquée dans les cas suivants[12] :
- traitement préventif des infections à mycobactéries dues à Mycobacterium avium complex (MAC) chez les sujets infectés par le virus VIH et présentant un taux de CD4 inférieur à 100/mm3.
- traitement curatif des infections à mycobactéries dues à Mycobacterium avium complex (MAC) chez les sujets infectés par le virus VIH dans le cadre d'une polychimiothérapie.
- Traitement de la tuberculose multirésistante en particulier à la rifampicine.
Effets Indésirables
La rifabutine peut causer un certain nombre d'effets indésirables, tels qu'une neutropénie, des éruptions cutanées, des nausées et vomissements, etc.[13]
De plus, du fait de la forte coloration de la rifabutine et de ses métabolites, un autre effet indésirable rencontré est la coloration des sécrétions (urines, sueur, larmes, etc.) en orange. Ceci n'est toutefois pas dangereux.
Comme d'autres molécules de la classe des rifamycines, la rifabutine est un inducteur du cytochrome P450. Cet effet est toutefois moins marqué que pour la rifampicine par exemple[11].
Contre-indications
Les contre-indications de la rifabutine sont les suivantes[12] :
- Hypersensibilité aux rifamycines, de par une réaction allergique croisée entre les membres de cette famille chimique
- Insuffisance rénale, de par une grande proportion de la rifabutine excrétée dans les urines (sous forme de métabolites)
- Utilisation concomitante de saquinavir, un inhibiteur de la protéase utilisé dans le traitement contre le VIH. La rifabutine étant un inducteur enzymatique, le saquinavir peut voir son efficacité diminuée car plus fortement métabolisé par le cytochrome P450[14].
- Par mesure de précaution, la rifabutine ne doit pas être prescrite chez la femme enceinte et chez la femme allaitante. Il n'existe en effet pas d'études concernant le passage de l'antibiotique dans le liquide amniotique ou dans le lait maternel.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- WHO Model List of Essential Medicines, 18th list, avril 2013
- (en) L. Marsili, C. R. Pasqualucci, A. Vigevani et B. Gioia, « New rifamycins modified at positions 3 and 4. Synthesis, structure and biological evaluation. », The Journal of Antibiotics, vol. 34, no 8, , p. 1033–1038 (ISSN 0021-8820 et 1881-1469, DOI 10.7164/antibiotics.34.1033, lire en ligne, consulté le )
- P.S. Murali Krishna, G. Venkateswarlu et L. Venkateswar Rao, « [No title found] », World Journal of Microbiology and Biotechnology, vol. 15, no 6, , p. 741–743 (DOI 10.1023/A:1008906930394, lire en ligne, consulté le )
- « ANSATIPINE 150 mg gél », sur VIDAL (consulté le )
- (en) Calvin M. Kunin, « Antimicrobial Activity of Rifabutin », Clinical Infectious Diseases, vol. 22, no Supplement_1, , S3–S14 (ISSN 1537-6591 et 1058-4838, DOI 10.1093/clinids/22.Supplement_1.S3, lire en ligne, consulté le )
- « Rifabutin », sur go.drugbank.com (consulté le )
- W. Wehrli et M. Staehelin, « Actions of the rifamycins », Bacteriological Reviews, vol. 35, no 3, , p. 290–309 (ISSN 0005-3678, PMID 5001420, PMCID PMC378391, lire en ligne, consulté le )
- (en) Terrence F. Blaschke et Michael H. Skinner, « The Clinical Pharmacokinetics of Rifabutin », Clinical Infectious Diseases, vol. 22, no Supplement_1, , S15–S22 (ISSN 1537-6591 et 1058-4838, DOI 10.1093/clinids/22.Supplement_1.S15, lire en ligne, consulté le )
- (en) M H Skinner, M Hsieh, J Torseth et D Pauloin, « Pharmacokinetics of rifabutin. », Antimicrobial Agents and Chemotherapy, vol. 33, no 8, , p. 1237–1241 (ISSN 0066-4804 et 1098-6596, PMID 2552902, PMCID PMC172632, DOI 10.1128/AAC.33.8.1237, lire en ligne, consulté le )
- (en) Michael H. Skinner et Terrence F. Blaschke, « Clinical Pharmacokinetics of Rifabutin: », Clinical Pharmacokinetics, vol. 28, no 2, , p. 115–125 (ISSN 0312-5963, DOI 10.2165/00003088-199528020-00003, lire en ligne, consulté le )
- « Résumé des Caractéristiques du Produit », sur agence-prd.ansm.sante.fr (consulté le )
- « Notice patient - ANSATIPINE 150 mg, gélule - Base de données publique des médicaments », sur base-donnees-publique.medicaments.gouv.fr (consulté le )
- (en) G. J. Moyle, N. E. Buss, T. Goggin et P. Snell, « Interaction between saquinavir soft-gel and rifabutin in patients infected with HIV: Short report », British Journal of Clinical Pharmacology, vol. 54, no 2, , p. 178–182 (PMID 12207638, PMCID PMC1874397, DOI 10.1046/j.1365-2125.2002.01631.x, lire en ligne, consulté le )
- Portail de la pharmacie
- Portail de la chimie