Substance humique
Les substances humiques sont des composés organiques qui sont des composants importants de l'humus, la principale fraction organique du sol, de la tourbe et du charbon (et également un constituant de nombreux cours d'eau des hautes terres, des lacs dystrophiques et de l'eau de l'océan). Pendant une longue période aux XIXe et XXe siècles, les substances humiques ont souvent été considérées sous l'angle de la théorie acido-basique qui décrivait les acides humiques, comme des acides organiques, et leurs bases conjuguées, les humates, comme des composants importants de la matière organique. De ce point de vue, les acides humiques furent définis comme des substances organiques extraites du sol qui coagulent (forment de petits morceaux solides) lorsqu'un extrait à base forte est acidifié, tandis que les acides fulviques sont des acides organiques qui restent solubles (restent dissous) lorsqu'un extrait à base forte est acidifié.
La matière humique isolée est le résultat d'une extraction chimique à partir de la matière organique du sol (en) ou de la matière organique dissoute et représente les molécules humiques distribuées dans le sol ou l'eau[1],[2],[3]. Une nouvelle compréhension considère les substances humiques non pas comme des macropolymères à haut poids moléculaire, mais comme des composants moléculaires hétérogènes et relativement petits de la matière organique du sol auto-assemblés en associations supramoléculaires et composés d'une variété de composés d'origine biologique et synthétisés par des réactions abiotiques et biotiques dans le sol[4]. C'est la grande complexité moléculaire de l'huméome du sol [5] qui confère à la matière humique sa bio-activité dans le sol et son rôle de promoteur de croissance des plantes[6].
Vue traditionnelle de la formation et de la description
La formation de substances humiques dans la nature est l'un des aspects les moins compris de la chimie de l'humus et l'un des plus intrigants. Il existe trois théories principales pour l'expliquer: la théorie de la lignine de Waksman (1932), la théorie des polyphénols et la théorie de la condensation sucre-amine de Maillard (1911)[7],[8]. Ces théories sont insuffisantes pour rendre compte des observations en recherche pédologique[9]. Les substances humiques sont formées par la dégradation microbienne de matières végétales mortes (en), telles que la lignine et le charbon de bois [10] . Les substances humiques dans le laboratoire sont très résistantes à une biodégradation ultérieure. Les propriétés et la structure précises d'un échantillon donné dépendent de la source d'eau ou de sol et des conditions spécifiques d'extraction. Néanmoins, les propriétés moyennes des substances humiques produites en laboratoire à partir de différentes sources sont remarquablement similaires.
Les substances humiques présentes dans les sols et les sédiments peuvent être divisées en trois fractions principales: les acides humiques, les acides fulviques et l' humine. Leur présence et leur abondance relative sont déduites par extraction en laboratoire, un processus qui altère leur forme originale au-delà de toute reconnaissance. Les acides humique et fulvique sont extraits sous forme de sol colloïdal du sol et d'autres sources en phase solide dans une solution aqueuse fortement basique d'hydroxyde de sodium ou d'hydroxyde de potassium. Les acides humiques sont précipités à partir de cette solution en ajustant le pH à 1 avec de l'acide chlorhydrique, laissant les acides fulviques en solution. C'est la distinction opérationnelle entre les acides humique et fulvique. L'humin est insoluble dans un alcali dilué. La partie soluble dans l'alcool de la fraction humique est, en général, appelée acide ulmique. Les «acides humiques gris» (gray humic acids, GHA) sont solubles dans les milieux alcalins de faible force ionique; les «acides humiques bruns» (brown humic acids, BHA) sont solubles dans des conditions alcalines indépendantes de la force ionique; et les acides fulviques (FA) sont solubles indépendamment du pH et de la force ionique[11].
L'humus dans la nature est produit par biodégradation de tissus d'organismes morts et est donc à peu près synonyme de matière organique ; les distinctions entre les deux ne sont souvent pas établies de manière précise et cohérente.
L'acide humique tel qu'il est traditionnellement produit en laboratoire n'est pas un acide unique; il s'agit plutôt d'un mélange complexe de nombreux acides différents contenant des groupes carboxyle et phénolate de sorte que le mélange se comporte fonctionnellement comme un acide dibasique ou, occasionnellement, comme un acide tribasique. L'acide humique utilisé pour modifier le sol est fabriqué selon ces mêmes procédures bien établies. Les acides humiques peuvent former des complexes avec des ions que l'on trouve couramment dans l'environnement, créant des colloïdes humiques. Les acides humiques sont insolubles dans l'eau à pH acide, tandis que les acides fulviques sont également dérivés de substances humiques, mais sont solubles dans l'eau sur toute la plage de pH[12]. Les acides humiques et fulviques sont couramment utilisés comme complément du sol en agriculture, et moins fréquemment comme complément nutritionnel humain[13]. En tant que complément nutritionnel, l'acide fulvique peut être trouvé sous forme liquide en tant que composant de colloïdes minéraux. Les acides fulviques sont des polyélectrolytes et sont des colloïdes uniques qui se diffusent facilement à travers les membranes, contrairement à tous les autres colloïdes[14].
Un fractionnement chimique séquentiel appelé Humeomics peut être utilisé pour isoler des fractions humiques plus homogènes et déterminer leurs structures moléculaires par des méthodes spectroscopiques et chromatographiques avancées[15]. Les substances identifiées dans les extraits humiques et directement dans le sol comprennent les mono, di- et trihydroxy acides (en), les acides gras, les acides dicarboxyliques, les alcools linéaires, les acides phénoliques, les terpénoïdes, les glucides et les acides aminés[16].
Critique
Les produits de décomposition des matières végétales mortes forment des associations intimes avec les minéraux, ce qui rend difficile l'isolement et la caractérisation des constituants organiques du sol. Les chimistes du sol du XVIIIe siècle ont utilisé avec succès l'extraction alcaline pour isoler une partie des constituants organiques du sol. Cela a conduit à la théorie selon laquelle un processus « d'humification » créait des « substances humiques »; le plus souvent « acide humique », « acide fulvique » et « humin ». Cependant, ces substances humiques n'ont pas été observées dans le sol. Bien que la théorie de « l'humification » ne soit pas étayée par des preuves, la théorie sous-jacente persiste dans la littérature contemporaine, y compris les manuels actuels. Les tentatives de redéfinir les « substances humiques » en termes valables ont abouti à une prolifération de définitions incompatibles, avec des implications de grande portée au-delà de la capacité à communiquer des processus et des propriétés du sol scientifiquement précis[17].
Caractéristiques chimiques des substances humiques dans la nature
Depuis l'aube de la chimie moderne, les substances humiques sont parmi les plus étudiées parmi les matériaux naturels. Malgré de longues études, leur structure moléculaire et chimique reste insaisissable. L'opinion traditionnelle est que les substances humiques sont des hétéropolycondensats, en associations variées avec l'argile. Une opinion plus récente est que des molécules relativement petites jouent également un rôle[18]. Les substances humiques représentent 50 à 90% de la capacité d'échange cationique. Semblable à l'argile, le charbon et l'humus colloïdal contiennent des nutriments cationiques[19].
Caractéristiques chimiques des substances humiques traditionnellement produites
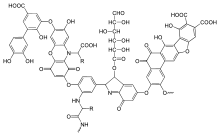
Une substance humique typique est un mélange de nombreuses molécules, dont certaines sont basées sur un motif de noyaux aromatiques avec des substituants phénoliques et carboxyliques, liés ensemble; l'illustration montre une structure typique. Les groupes fonctionnels qui contribuent le plus à la charge de surface et à la réactivité des substances humiques sont les groupes phénoliques et carboxyliques[20]. Les acides humiques se comportent comme des mélanges d'acides dibasiques, avec une valeur pK1 d'environ 4 pour la protonation des groupes carboxyle et d'environ 8 pour la protonation des groupes phénolate. Il existe une similitude globale considérable entre les différents acides humiques[21]. Pour cette raison, les valeurs pK mesurées pour un échantillon donné sont des valeurs moyennes relatives aux espèces constitutives. L'autre caractéristique importante est la densité de charge. Les molécules peuvent former une structure supramoléculaire maintenue ensemble par des forces non-covalente, telles que la force de van der Waals, les liaisons π-π et CH-π[18].
La présence de groupes carboxylate et phénolate donne aux acides humiques la capacité de former des complexes avec des ions tels que Mg 2+, Ca 2+, Fe 2+ et Fe 3+. De nombreux acides humiques ont au moins deux de ces groupes disposés de manière à permettre la formation de complexes chélates[22]. La formation de complexes (chélates) est un aspect important du rôle biologique des acides humiques dans la régulation de la biodisponibilité des ions métalliques[21].
Détermination des acides humiques dans les échantillons d'eau
La présence d'acide humique dans l'eau destinée à un usage d'eau potable ou industriel peut avoir un impact significatif sur la traitabilité de cette eau et le succès des procédés de désinfection chimique. Par exemple, les acides humiques et fulviques peuvent réagir avec les produits chimiques utilisés dans le processus de chloration pour former des sous-produits de désinfection tels que les dihaloacétonitriles, qui sont toxiques pour l'homme[23],[24] . Des méthodes précises d'établissement des concentrations d'acide humique sont donc essentielles pour maintenir l'approvisionnement en eau, en particulier à partir des bassins versants tourbeux des hautes terres dans les climats tempérés.
Comme de nombreuses molécules bio-organiques différentes dans des associations physiques très diverses sont mélangées dans des environnements naturels, il est difficile de mesurer leurs concentrations exactes dans la superstructure humique. Pour cette raison, les concentrations d'acide humique sont traditionnellement estimées à partir des concentrations de matière organique (généralement à partir des concentrations de carbone organique total (COT) ou de carbone organique dissous (COD).
Les procédures d'extraction sont vouées à modifier certaines des liaisons chimiques présentes dans les substances humiques du sol (principalement les liaisons ester dans les biopolyesters tels que les cutines et les subérines). Les extraits humiques sont composés d'un grand nombre de molécules bio-organiques différentes qui n'ont pas encore été totalement séparées et identifiées. Cependant, des classes uniques de biomolécules résiduelles ont été identifiées par des extractions sélectives et un fractionnement chimique, et sont représentées par les acides alcanoïques et hydroxyalcanoïques, les résines, les cires, les résidus de lignine, les sucres et les peptides.
Effets écologiques
Les agriculteurs savent que les amendements du sol en matière organique sont bénéfiques à la croissance des plantes depuis bien avant l'histoire enregistrée[25]. Cependant, la chimie et la fonction de la matière organique ont été un sujet de controverse depuis que les humains ont commencé à postuler à ce sujet au XVIIIe siècle. Jusqu'à l'époque de Liebig, on supposait que l'humus était utilisé directement par les plantes, mais, après que Liebig ait montré que la croissance des plantes dépend de composés inorganiques, de nombreux pédologues ont estimé que la matière organique n'était utile pour la fertilité que parcequ'elle était décomposée, avec la libération de ses éléments nutritifs constitutifs, sous des formes inorganiques. À l'heure actuelle, les pédologues ont une vision plus holistique et reconnaissent au moins que l'humus influence la fertilité du sol, par son effet sur la capacité de rétention d'eau du sol. De plus, comme il a été démontré que les plantes absorbent et transloquent les molécules organiques complexes des insecticides systémiques, ils ne peuvent plus discréditer l'idée que les plantes peuvent être capables d'absorber les formes solubles de l'humus [26]; cela peut en fait être un processus essentiel pour l'absorption d'oxydes de fer autrement insolubles.
Une étude sur les effets de l'acide humique sur la croissance des plantes a été menée à l'Ohio State University qui déclara qu'en partie les acides humiques augmentaient la croissance des plantes et qu'il y a des réponses relativement importantes à de faibles taux d'application[27].
Une étude réalisée en 1998 par des scientifiques du North Carolina State University College of Agriculture and Life Sciences a montré que l'ajout d'humate au sol augmentait considérablement la masse racinaire des gazon d'Agrostis stolonifera[28],[29].
Applications technologiques
Les capacités de liaison des métaux lourds des acides humiques ont été exploitées pour développer des technologies de remédiation pour éliminer les métaux lourds des eaux usées. À cette fin, Yurishcheva et al. revêtent des nanoparticules magnétiques enrobées d'acides humiques. Après avoir capturé les ions plomb, les nanoparticules peuvent ensuite être capturées à l'aide d'un aimant[30].
Maçonnerie ancienne
L'archéologie constate que l'Égypte ancienne utilisait des briques de boue renforcées avec de la paille et des acides humiques[31].
Géologie économique
Dans la géologie économique, le terme Humus fait référence à des matériaux géologiques, tels que lits de charbon décomposé (par altération), argilite (mudrock, roche argileuse meuble et peu stratifiée, provenant de la consolidation d'argiles par compaction) ou matériau de pores dans les grès, qui sont riches en acides humiques. De l'humate a été extrait de la Formation de Fruitland du Nouveau-Mexique pour être utilisé comme amendement du sol depuis les années 1970, avec près de 60 000 tonnes métriques produites en 2016[32]. Les gisements d'humates peuvent également jouer un rôle important dans la genèse des gisements d'uranium[33].
Références
- Piccolo A., « In memeoriam of Prof. F.J.Stevenson and the Question of humic substances », Chemical and Biological Technologies in Agriculture, vol. 3, (DOI 10.1186/s40538-016-0076-2)
- Drosos M., « A molecular zoom into soil Humeome by a direct sequential chemical fractionation of soi », The Science of the Total Environment, vol. 586, , p. 807–816 (PMID 28214121, DOI 10.1016/j.scitotenv.2017.02.059, Bibcode 2017ScTEn.586..807D)
- « Source Materials for International Humic Substances Society Samples » (consulté le )
- Piccolo A., The Molecular Composition of Humus Carbon: Recalcitrance and Reactivity in Soils. In: The Future of Soil Carbon, Wiley and Sons, , 87–124 p. (ISBN 9780128116876, DOI 10.1016/B978-0-12-811687-6.00004-3), « The Molecular Composition of Humus Carbon: Recalcitrance and Reactivity in Soils »
- Nebbioso A. and Piccolo A., « Basis of a Humeomics Science: Chemical Fractionation and Molecular Characterization of Humic Biosuprastructures », Biomacromolecules, vol. 12, no 4, , p. 1187–1199 (PMID 21361272, DOI 10.1021/bm101488e, lire en ligne)
- Canellas P.L and Olivares F.L., « TPhysiological responses to humic substances as plant growth promoter », Chemical and Biological Technologies in Agriculture, vol. 1, , p. 3 (DOI 10.1186/2196-5641-1-3)
- Stevenson, F.J. (1994). Humus Chemistry: Genesis, Composition, Reactions, Wiley & Sons, New York, 1994, pp. 188-210. (ISBN 0471594741).
- Tan, K. H. (2014). Humic matter in soil and the environment: principles and controversies. 2nd ed. Boca Ranton: CRC Press. (ISBN 1482234459).
- Lehmann et Kleber, « The contentious nature of soil organic matter », Nature, vol. 528, no 7580, , p. 60–8 (PMID 26595271, DOI 10.1038/nature16069, Bibcode 2015Natur.528...60L)
- Mao, Johnson, Lehmann et Olk, « Abundant and stable char residues in soils: implications for soil fertility and carbon sequestration », Environmental Science and Technology, vol. 46, no 17, , p. 9571–9576 (PMID 22834642, DOI 10.1021/es301107c, Bibcode 2012EnST...46.9571M, lire en ligne)
- Baigorri R, Fuentes M, González-Gaitano G et García-Mina JM, « Complementary Multianalytical Approach To Study the Distinctive Structural Features of the Main Humic Fractions in Solution: Gray Humic Acid, Brown Humic Acid, and Fulvic Acid », J Agric Food Chem, vol. 57, no 8, , p. 3266–72 (PMID 19281175, DOI 10.1021/jf8035353, lire en ligne)
- MacCarthy, « The Principles of Humic Substances », Soil Science, vol. 166, no 11, , p. 738–751 (DOI 10.1097/00010694-200111000-00003, Bibcode 2001SoilS.166..738M)
- « Effects of Humic Acid on Animals and Humans: An Overview of Literature and a Review of Current Research », vet servis
- Yamauchi, Katayama, Todoroki et Watanable, « Total synthesis of fulvic acid », Journal of the Chemical Society, Chemical Communications, no 23, , p. 1565–6 (DOI 10.1039/C39840001565) :
« Synthesis of fulvic acid (1a) was accomplished by a route involving selective ozonization of 9-propenylpyranobenzopyran (1c), obtained by a regioselective cyclization of the 2-methylsulphinylmethyl 1,3-dione(3c) »
- Nebbioso A. and Piccolo A., « Advances in humeomics: Enhanced structural identification of humic molecules after size fractionation of a soil humic acid », Analytica Chimica Acta, vol. 720, , p. 77–90 (PMID 22365124, DOI 10.1016/j.aca.2012.01.027)
- Drosos M. and Piccolo A., « The molecular dynamics of soil humus as a function of tillage », Land Degradation & Development, vol. 29, no 6, , p. 1792–1805 (DOI 10.1002/ldr.2989)
- Lehmann et Kleber, « The contentious nature of soil organic matter », Nature, vol. 528, no 7580, , p. 60–8 (PMID 26595271, DOI 10.1038/nature16069, Bibcode 2015Natur.528...60L) :
« The issue has also been approached by redefining ‘humic substances’ as the portion of soil organic matter that cannot be molecularly characterized or by calling all soil organic matter ‘humus’. We argue that this compromise - maintaining terminology but altering its meanings in varying ways — hampers scientific progress beyond the soil sciences.The [need for accurate models] of soil organic matter does not allow a confusing middle path; it requires leaving the traditional view behind to bring about lasting innovation and progress. This is critical as scientific fields outside the soil sciences base their research on the false premise of the existence of ‘humic substances’. Thus an issue of terminology becomes a problem of false inference, with far-reaching implications beyond our ability to communicate scientifically accurate soil processes and properties. »
- Piccolo, A., The Supramolecular structure of humic substances. A novel understanding of humus chemistry and implications in soil science, vol. 75, coll. « Advances in Agronomy », , 57–134 p. (ISBN 978-0-12-000793-6, DOI 10.1016/S0065-2113(02)75003-7)
- (en) Ray R. Weil et Nyle C. Brady, The Nature and Properties of Soils, Columbus, Pearson, (réimpr. April 11, 2016) (ISBN 9780133254488, OCLC 942464649, LCCN 2016008568), p. 554 :
« Humus accounts for 50 to 90% of cation exchange capacity. Like clays, humus colloids and high surface area char hold nutrient cations »
- Stevenson F.J., Humus Chemistry: Genesis, Composition, Reactions, New York, John Wiley & Sons,
- E.A. Ghabbour et Davies, G. (Editors), Humic Substances: Structures, Models and Functions, Cambridge, U.K., RSC publishing, (ISBN 978-0-85404-811-3)
- Tipping, « 'WHAM – a chemical equilibrium model and computer code for waters, sediments, and soils incorporating a discrete site/electrostatic model of ion-binding by humic substances », Computers and Geosciences, vol. 20, no 6, , p. 973–1023 (DOI 10.1016/0098-3004(94)90038-8, Bibcode 1994CG.....20..973T)
- Oliver, « Dihaloacetonitriles in drinking water: Algae and fulvic acid as precursors », Environmental Science & Technology, vol. 17, no 2, , p. 80–83 (PMID 22295957, DOI 10.1021/es00108a003, Bibcode 1983EnST...17...80O)
- Peters, De Leer et De Galan, « Dihaloacetonitriles in Dutch drinking waters », Water Research, vol. 24, no 6, , p. 797 (DOI 10.1016/0043-1354(90)90038-8)
- McGraw-Hill encyclopedia of science and technology: an international reference work, Volume 12, McGraw-Hill, (ISBN 978-0070452657, lire en ligne), p. 428 :
« The value of adding organic matter to the soil in the form of animal manures, green manures, and crop residues for producing favorable soil tilth has been known since ancient times »
- Pan American Union. Dept. of Cultural Affairs. División de Fomento Científico, Pan American Union. Dept. of Scientific Affairs, Organization of American States. Dept. of Scientific Affairs, Ciencia interamericana: Volumes 24–27, (lire en ligne) :
« And since plants have shown their ability to absorb and translocate the complex molecules of systemic insecticides, they can no longer discredit the idea that plants are able to absorb the soluble humic nutrients, containing by far ... »
- Arancon, Edwards, Lee et Byrne, « Effects of humic acids from vermicomposts on plant growth », European Journal of Soil Biology, vol. 42, , S65–S69 (DOI 10.1016/j.ejsobi.2006.06.004)
- Cooper, Liu et Fisher, « Influence of Humic Substances on Rooting and Nutrient Content of Creeping Bentgrass », Crop Science, vol. 38, no 6, , p. 1639 (DOI 10.2135/cropsci1998.0011183X003800060037x)
- Liu, Chunhua et Cooper, R. J., « Humic Substances Their Influence on Creeping Bentgrass Growth and Stress Tolerance », TurfGrass Trends, , p. 6 (lire en ligne)
- Yurishcheva, Kydralieva, Zaripova et Dzhardimalieva, « Sorption of Pb2+ by magnetite coated with humic acids », J. Biol. Phys. Chem., vol. 13, no 2, , p. 61–68 (DOI 10.4024/36FR12A.jbpc.13.02)
- Lucas, A. et Harris, J.R., Ancient Egyptian Materials and Industries, New York, Dover Publications, (ISBN 978-0-486-40446-2, lire en ligne), p. 62
- Newcomer, Nybo et Newcomer, « Humate in the upper Cretaceous Fruitland Formation in northwestern New Mexico », New Mexico Geological Society Special Publication, vol. 14, , p. 41-46 (lire en ligne, consulté le )
- McLemore, « Uranium deposits in the Poison Canyon trend, Ambrosia Lake Subdistrict, Grants Uranium District, McKinley and Cibola Counties, New Mexico », New Mexico Geological Society Special Publication, vol. 14, , p. 53-63 (lire en ligne, consulté le )
Liens externes
- Supramolecular Humic Systems in the Environment (In English, original is Italian)
Lectures complémentaires
- D.O. Hessen et Tranvik, L.J. (Editors), Aquatic humic substances: ecology and biogeochemistry, Berlin, Springer, (ISBN 978-3-540-63910-7)
- Sillanpää, M. (Ed.) Matière organique naturelle dans l'eau, méthodes de caractérisation et de traitement (ISBN 9780128015032)
- Portail de la chimie
- Portail de la biochimie