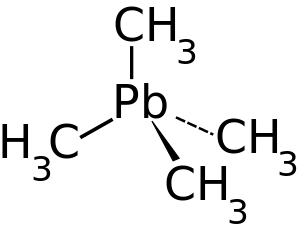
Tétraméthylplomb
Le tétraméthylplomb est un composé organoplombé. Il est notamment utilisé comme additif anti-cliquetis (en) pour l'essence[4]. Son utilisation est progressivement supprimée pour des raisons environnementales[5].
| Tétraméthylplomb | |
  |
|
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.000.816 |
| PubChem | 6394 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore[1] |
| Propriétés chimiques | |
| Formule | C4H12Pb |
| Masse molaire[2] | 267,3 ± 0,1 g/mol C 17,97 %, H 4,52 %, Pb 77,52 %, |
| Propriétés physiques | |
| T° fusion | −28 °C[1] |
| T° ébullition | 110 °C[1] |
| Solubilité | 0,3 g L−1 (20 °C)[1] |
| Masse volumique | 2,00 g cm−3 (20 °C)[1] |
| Densité de vapeur | 9,20[1] |
| Densité du mélange air-vapeur | 1,26 (20 °C, pression normale)[1] |
| Point d’éclair | < 21 °C (coupelle fermée)[1] |
| Limites d’explosivité dans l’air | 1,8 vol.% - 200 g/m3 (limite basse)[1] |
| Pression de vapeur saturante | 32 hPa (20 °C)[1] 52 hPa (30 °C)[1] 128 hPa (50 °C)[1] |
| Précautions | |
| SGH[1] | |
   Danger |
|
| Transport[1] | |
| Écotoxicologie | |
| DL50 | 105 mg kg−1 (rat, oral)[3] |
| LogP | 2,97[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
L'Institut national pour la sécurité et la santé au travail (NIOSH) aux États-Unis a identifié le tétraméthylplomb comme un danger sur le lieu de travail. La limite d'exposition moyenne pondérée dans le temps recommandée est de 0,075 mg/m3 pendant une journée de travail de dix heures ; la limite d'exposition admissible OSHA est la même valeur en supposant une journée de travail de huit heures.
L'exposition au tétraméthylplomb peut affecter le système nerveux central, les reins et le système cardiovasculaire. Le tétraméthylplomb peut être absorbé par inhalation, par contact avec les yeux, par absorption cutanée et par ingestion. Les symptômes de l'exposition comprennent l'insomnie, le coma, les convulsions, la manie, le délire, la perte d'appétit, les nausées, l'hypotension, l'anxiété, l'agitation et les cauchemars. Les premiers soins en cas d'exposition comprennent la respiration artificielle, l'irrigation immédiate des yeux et le lavage immédiat à l'eau. Une attention médicale immédiate doit être recherchée en cas d'ingestion de tétraméthylplomb[6].
Voir également
Références
- Entrée « Tetramethyllead » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 2021-02-17 (JavaScript nécessaire).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- MELAAD Medicina del Lavoro. Industrial Medicine. (Via S. Barnaba, 8, 20122 Milan, Italy)Vol. 54, Pg. 486,1963. (RTECS).
- « Tetramethyllead », sur pubchem.ncbi.nlm.nih.gov.
- Montserrat Filella et Josep Bonet, Lead: Its Effects on Environment and Health, vol. 17, de Gruyter, coll. « Metal Ions in Life Sciences » (réimpr. 2017), 471–490 p. (DOI 10.1515/9783110434330-014), « Chapter 14. Environmental Impact of Alkyl Lead(IV) Derivatives: Perspective after Their Phase-out ».
- « CDC - NIOSH Pocket Guide to Chemical Hazards - Tetramethyl lead (as Pb) », sur cdc.gov (consulté le ).
- Portail de la chimie

