Triméthylamine
La triméthylamine a pour formule C3H9N. Elle est dérivée de l'ammoniac dans lequel trois groupes –CH3 ont remplacé ses trois atomes d'hydrogène.
| Triméthylamine | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | N,N-diméthylméthanamine | |
| Synonymes |
triméthylamine |
|
| No CAS | ||
| No ECHA | 100.000.796 | |
| No CE | 200-875-0 | |
| FEMA | 3241 | |
| Apparence | gaz comprimé liquéfié incolore, d'odeur caractéristique. Ou solution incolore dans l'eau, d'odeur âcre (solution aqueuse à 40 %)[1] |
|
| Propriétés chimiques | ||
| Formule | C3H9N [Isomères] |
|
| Masse molaire[2] | 59,110 3 ± 0,003 2 g/mol C 60,96 %, H 15,35 %, N 23,7 %, |
|
| pKa | 9,87 | |
| Moment dipolaire | 0,612 ± 0,003 D [3] | |
| Propriétés physiques | ||
| T° fusion | −117 °C (pur)[1], −3 °C (solution à 40 %)[1] |
|
| T° ébullition | 3 °C (pur)[1], 30 °C (solution à 40 %)[1] |
|
| Solubilité | dans l'eau : très bonne | |
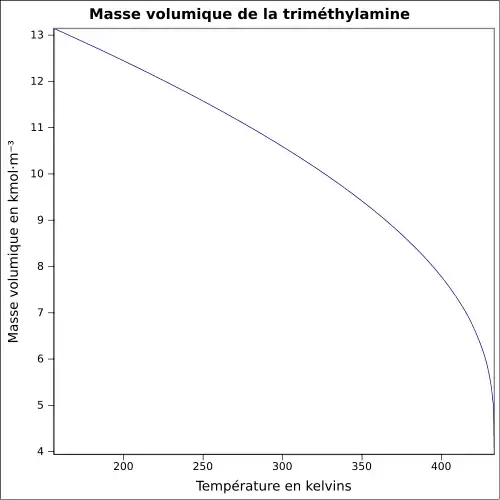
| Masse volumique | 0,6 g·cm-3 (liquide pur)[1], 0,9 g·cm-3 (solution à 40 %)[1] |
|
| T° d'auto-inflammation | 190 °C[1] | |
| Point d’éclair | −7 °C[1] | |
| Limites d’explosivité dans l’air | 2,0–11,6 %vol (pur)[1],2–16,6 %vol (solution à 40 %)[1] |
|
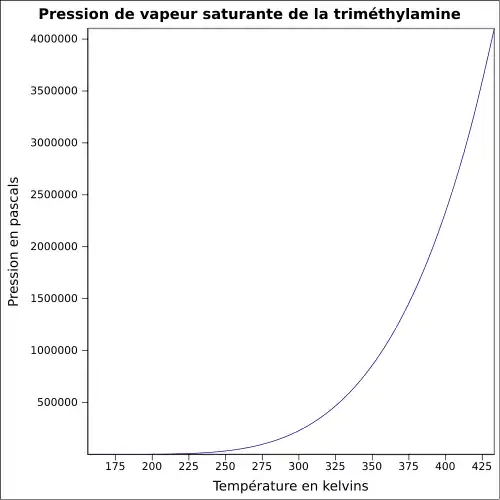
| Pression de vapeur saturante | 187 kPa (pur, 20 °C)[1], 67 kPa (solution à 40 %, 20 °C)[1] |
|
| Point critique | 40,9 bar, 160,15 °C [5] | |
| Thermochimie | ||
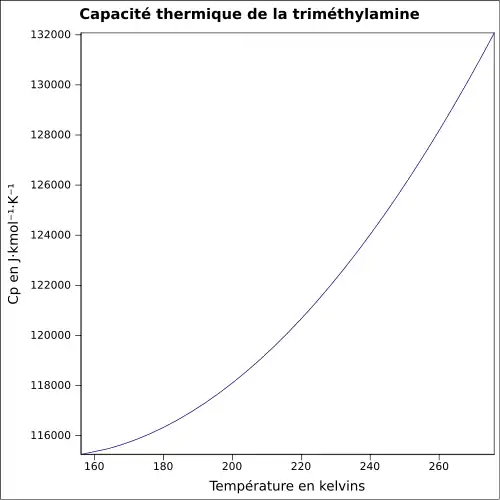
| Cp | ||
| PCS | 2 443,1 kJ·mol-1 (25 °C, gaz)[7] | |
| Propriétés électroniques | ||
| 1re énergie d'ionisation | 7,82 ± 0,06 eV (gaz)[8] | |
| Précautions | ||
| SGH[9],[10] | ||
    Danger    Danger |
||
| SIMDUT[11] | ||
   A, B1, E, |
||
| NFPA 704 | ||
| Transport | ||
| Inhalation | Sensation de brûlure. Toux. Maux de tête. Mal de gorge. Respiration difficile. Essoufflement. Symptômes d'effets retardés. | |
| Peau | Lors du contact avec le liquide : gelure. | |
| Yeux | Rougeur. Douleur. Troubles de la vue. | |
| Écotoxicologie | ||
| LogP | 0,2 (pur)[1], -0.3 (solution à 40 %)[1] |
|
| Seuil de l’odorat | bas : 0,000 11 ppm haut : 0,87 ppm[12] |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
La triméthylamine est un gaz qui se liquéfie à 2 °C.
Elle dégage une odeur de poisson pourri sous l’action des enzymes et microbes sur les protéines de poisson. Elle est responsable de l’odeur des harengs marinés.[réf. nécessaire]
Utilisation
La triméthylamine est utilisée comme réactif intermédiaire dans la synthèse de nombreux produits organiques (produits pharmaceutiques, agriculture, colorants, caoutchoucs et produits explosifs ou propulseurs)[13].
En médecine
La triméthylaminurie est une maladie génétique, consistant en une concentration trop élevée en cette molécule dans les fluides corporels, secondaire à une mutation sur le gène codant une enzyme, la flavine-monooxygénase 3 (FMO3), permettant la dégradation de la molécule en un composé non odorant. La caractéristique principale de la maladie est l'odeur corporelle de poisson.
Voir aussi
Notes et références
- TRIMETHYLAMINE et TRIMETHYLAMINE (solution aqueuse à 40 %), Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 9-50
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 978-0-07-049841-9, LCCN 96051648), p. 2-50
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 1, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 978-0-88415-857-8, LCCN 96036328)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Triméthylamine » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Trimethylamine », sur hazmap.nlm.nih.gov (consulté le )
- lire en ligne
- Portail de la chimie
- Portail des odeurs, des senteurs et du parfum