Wohlfahrtiose
La wohlfahrtiose est une parasitose provoquée par les diptères du genre Wohlfahrtia, de la famille des Sarcophagidae. De nombreuses espèces produisent des myiases, spécifiques ou non, aux animaux et aux hommes.


Contexte historique et géographique
Cette parasitose est mise en évidence à la fin du XIXe siècle, lorsque Wohlfahrtia magnifica (Schiner), un parasite particulièrement dangereux, provoque d’importants dommages dans l’économie de plusieurs pays européens en créant une déstabilisation de certains écosystèmes agricoles. De nombreuses races ovines à laine fine et demi-fine, originaires d’Australie et de Nouvelle-Zélande (Corriedale (en), Polwarth (en), Romney Marsh (en)) ont été massivement introduites dans ces pays, ce qui a bouleversé l’équilibre de la faune parasitaire, notamment celle des diptères myiasigènes dont les populations ont explosé de façon imprévisible, notamment Wohlfahrtia magnifica (Schiner). Dans tous les élevages ovins des pays de l’Europe centrale, l’infestation a commencé au début du mois de mai et, après la tonte des brebis, les myiases sont devenues visibles et ont évolué jusqu’à des formes graves, voire très graves. Lehrer (1983) a identifié pour la première fois en Roumanie et dans les pays limitrophes que Wohlfahrtia magnifica est l’agent myiasigène obligatoire et létal de ces ovines et a introduit les premiers traitements originaux pour combattre toutes les formes de myiases (Lehrer & Lehrer, 1986).
Les premiers animaux atteints gravement dans la région génitale, ont été les moutons importés à queue « miroir », chez qui la caudotomie pratiquée dans le pays d’origine a laissé la vulve entièrement découverte. Leurs descendants ont ensuite été attaqués, même si chez ceux-ci la caudotomie avait été effectuée à un niveau plus distal, de façon que la vulve soit protégée jusqu’à 1 cm sous la commissure ventrale. Rapidement, d’autre types de myiases sont alors apparues.
Certaines espèces de ces parasites se développent dans les substances organiques animales ou végétales en décomposition. Les facteurs qui provoquent et stimulent l’oviposition ou de larviposition sont les odeurs fétides que dégagent les tissus ou les organes malades ou nécrosés. Ainsi, Wohlfahrtia nuba (Wiedemann) est un myiasigène facultatif, qui produit des plaies bénignes aux mammifères et aux hommes.
En Roumanie, Lehrer et al. décrivent, en 1988[1], les formes suivantes d’affections : myiase vulvaire, myiase du prépuce, podomyiase, ophthalmomyiase, myiase traumatique et myiase cutanée des ovins nouveau-nés. Lehrer a observé également l’apparition plus ou moins occasionnelle de myiase cutanée sur des chiens et des porcs (dans le județ de Dâmbovița), de myiase génitale sur des chevaux (județ de Vaslui), de myiase traumatique (județ de Iași) et de myiase vulvaire sur les bovins (județ de Dâmbovița et de Neamț, etc.). Depuis, il a rencontré nombre de myiases similaires sur les bovins et sur porcs dans le delta du Danube, sur les bovins et sur les buffles dans le județ de Sălaj. À Tatamir, outre la myiase vulvaire, il a observé des myiases péri-anales sur vaches et sur porcs, ou la myiase du prépuce chez un taurillon.
Avant l’apparition de cette parasitose, W. magnifica n'était pas très répandue en Roumanie. Le premier cas d’otomyiase est décrit par R. Blanchard en 1881, chez une jeune fille de la localité Cîmpulung. Puis, N. Leon mentionne un cas de myiase de la muqueuse gingivale (abcès dentaire) chez une femme de 40 ans en 1903, et deux cas d’otomyiase chez deux enfants en 1908. Néanmoins, aucune invasion de W. magnifica n'a été observé sur plusieurs animaux dans une même région.
Il faut souligner que la « wohlfahrtiose » s'est largement développée en Europe centrale car ces pays constituent de vrais foyers de développement et de dispersion de la parasitose, du fait de l’élevage de ces races ovines dans des conditions bio-géographiques particulièrement similaires.
La myiase vulvaire

La plus répandue et la plus grave de toutes les formes de myiases connues, touche les brebis des troupeaux des associations d’éleveurs, des fermes, des coopératives et autres entreprises agricoles (fig. 2) dans une proportion de 90-95 %, pratiquement toute l’année (du début du mois de mai jusqu’au mois d’octobre). Les actions de ces larves sont désastreuses sur l’organisme animal. Dès que les conditions météorologiques s’améliorent, les dépôts de larves deviennent de plus en plus fréquents sur la muqueuse de la vulve et le développement larvaire ne demande plus que 5-7 jours. Ainsi on peut observer plusieurs générations de larves qui vivent dans la même plaie, ce qui a des conséquences particulièrement impressionnantes. La vitesse de reproduction de ce diptère myiasigène est devenue alarmante, et des myiases vulvaires graves a très graves sont rapidement apparues.
Le plus souvent, à la suite de la croissance rapide des larves, la vulve se tuméfie et les plaies s'approfondissent rapidement, on y observe de vrais tunnels voire des anfractuosités dans les parois, ce qui peut provoquer des déformations anatomiques défavorables à l'accouplement. Quand l'extirpation des larves et le traitement médical des plaies est retarde d'une semaine ou plus, les plaies alors isolées, confluent et transforment la vulve en une plaie unique d'un diamètre de 10 à 12 cm, enflée prenant l'aspect d'un tube envahi par des centaines de larves de toutes dimensions (fig. 1, A). À ce stade, les brebis souffrent énormément et ne mangent plus, luttant en permanence contre la douleur et le prurit vulvaire provoqués par les crochets mandibulaires et la spinulation récurrente, grâce auxquels les larves assurent leur fixation dans la musculature des organes génitaux. Plusieurs fois on constate aussi de nombreuses larves matures à l'intérieur du vagin. Les animaux essaient de se gratter soit avec les dents, soit en frottant leur train postérieur sur le sol. C'est la raison pour laquelle les plaies s'infectent souvent, suppurent, saignent, attirent les Muscides qui se nourrissent de ces liquides organiques ou les Calliphorides qui peuvent y déposer leur propres œufs.
Cette myiase affecte tant les brebis adultes, que les agnelles chez qui elle peut être fatale. Cet état de maladie quasi permanente, son contrôle à des intervalles aussi brefs et les traitements sanitaires appropriés provoquent un grand stress chez ces animaux. lIs ne se nourrissent pas normalement, maigrissent et tombent en prostration.
La myiase du prépuce
Avec la même célérité, Wohlfahrtia magnifica dépose ses paquets de larves au niveau de l'orifice du prépuce des béliers. Elles s'enfoncent immédiatement dans la cavité prépuciale et se développent dans les parois du tégument interne.
Cette myiase des béliers ne se découvre habituellement que quand le pénis est déjà très tuméfié ou quand l'animal se traîne le ventre au sol, à cause du prurit penial, alors que toute la cavite du prépuce est déjà envahie de nombreuses larves matures (fig. 1, B). D'un seul petit bélier, on peut extraire plus de 850 larves de divers stades.
Si on ne fait pas un contrôle permanent, les larves peuvent même détruire le gland de la verge compromettant irrémédiablement ainsi les meilleurs reproducteurs. Dans les fermes et les associations intercoopératives d'élevage d'ovins, qui cherchent à augmenter leur cheptel en respectant les caractéristiques biophysiologiques des races australiennes, notamment par l'obtention de 3 agneaux en deux ans, cette parasitose devient économiquement catastrophique au point d'annihiler un des principaux buts pour lesquels elles avaient été importées.
Podomyiase
On rencontre aussi très fréquemment la myiase des tissus mous des onglons. Elle peut être déclenchée soit par un traumatisme dans la zone de la couronne abaxiaIe, soit par une pododermatite necrobacillaire. L'infection de l'autopode constitue le point d'attraction au dépôt des larves par W. magnifica. La pénétration de ces larves dans l'intérieur de la boite cornée est facilitée aussi par l'évolution de la pododermite infectieuse qui, atteignant le pododerme et les tissus voisins (membrane keratogène), la détache peu à peu jusqu'à son décollement complet. Ainsi, les larves envahiront tant la zone interdigitale que l'intérieur de la boite cornée, provoquant la destruction des tissus des phalanges et l'accélération de la chute de l'onglon. En d'autres termes, la podomyiase peut être interdigitale, intraongulaire et mixte.
Ophtalmyiase
S'observe parfois sur des agneaux et des moutons de diverses origines. Un traumatisme ou une lésion d'une zone à proximité des yeux au moment de la tonte peut constituer le point d'infestation pour les larves de W. magnifica et permettre ensuite leur pénétration dans les orbites. Sur les agneaux nouveau-nés, affectés par une keratoconjonctivite, les séromuqueuses et les sécrétions purulentes conjonctivales attirent beaucoup de mouches, parmi lesquelles ce parasite obligatoire. Les larves sont déposées au niveau de la muqueuse oculaire, d'où elles peuvent détruire le globe oculaire et passer par le canal lacrymo-nasal dans les sinus nasaux et maxillaires.
Myiase traumatique
Une myiase traumatique est en réalité une myiase des plaies, produites par différentes causes. La plus répandue est celle qui suit la tonte. Mais, dans cette catégorie de myiases, on trouve encore les traumatismes provoques par les coups de l'animal, les lésions du corps de la mamelle ou la caudotomie. On connaît aussi une myiase à la base des cornes des béliers, résultant de la dislocation ou de la fissure des cornes à l'époque des luttes entre mâles.
Myiase cutanée des nouveau-nés
Peut-être considérée comme une variante extérieure de la myiase génitale déclenchée à la suite de négligences dans les mesures zoohygiéniques à observer chez les agneaux, lors des agnelages d'été (juillet et août). Chez les races autochtones, l'enlèvement des mucosités et du liquide amniotique se fait plus ou moins superficiellement après la parturition, et vise notamment a nettoyer la bouche et les narines en vue de libérer les voies respiratoires obstruées. Sur les agneaux d'origine étrangère cette opération du nettoyage s'est révélée très importante. L'enlèvement incomplet des mucosités sur tout le corps amène inévitablement la création de points ou de zones d'attraction pour les diptères myiasigènes à cause des odeurs spécifiques et des décompositions bactériennes intenses. Le processus parasitaire s'installe plus vite quand les agnelages s'effectuent dans des box non-protégés, sous la chaleur ardente du soleil des régions de steppes et de sylvosteppes. Dans ces circonstances, W. magnifica dépose ses larves sur les mucosités génitales subsistant a la surface du corps. Les conséquences de cette myiase sont particulièrement néfastes, puisqu'elle provoque des pertes allant jusqu'à 20 % des effectifs des nouveau-nés et des destructions très étendues sur la partie dorsale des peaux (garrot, lombes et croupes).
Développement larvaire de Wohlfahrtia magnifica
La connaissance des divers aspects morphologiques des stades et des interstades de larves, pendant le développement du Wohlfahrtia magnifica, a une exceptionnelle valeur pratique pour permettre la découverte précoce de ce dangereux agent myiasigène qui a tendance à se disperser de plus en plus dans les zones de steppe et de sylvosteppe des pays d'Europe centrale où des races d'ovins de l'hémisphère austral ont été introduites. Les stades du développement de ce parasite ont été décrites, pour la première fois, par Lehrer et ses collaborateurs (1986, 1988, 1991).
Larve de stade I


La larve de stade I a une spinulation peu sclérifiée, possédant trois crochets buccaux très visibles et extériorisés partiellement à la partie postéro-ventrale du segment céphalique (A). Si on réalise la transparence de la larve par n'importe quel procédé histologique, on peut observer non seulement la position perpendiculaire de la mandibule par rapport à l'axe longitudinal du squelette céphalo-pharyngien, mais aussi une paire de bourgeons embryonnaires des futurs mandibules (m) de la larve de deuxième âge, situés devant et au-dessus des crochets mandibulaires (fig. 3, A, B, C).
En extrayant l'armature buccale (B), on constate que la mandibule est formée d'une lame médiane longue, en forme de faux et d’une pièce basale étroite, soudée en angle aigu. De cette dernière, s'articulent deux crochets latéraux, plus courbés et aussi aigus que la lame médiane. Le sclérite pharyngien a ses ailes dorsales et ventrales souples, non divisées et sans ouvertures ; à la partie antérieure, il est muni d'un processus antéro-dorsal légèrement cambré, faiblement sclérifié. Un sclérite hypostomal se préfigure entre la pièce basale de la mandibule et le sclérite pharyngien. Les bourgeons embryonnaires de la mandibule de 1a larve de stade I sont très peu sclérifiés et très peu pigmentés au point qu'ils ne peuvent être décelés sans préparation histologique.
Les stigmates respiratoires postérieurs sont représentes par deux papilles simples (D), situées dans la cavité du dernier segment somatique. En fin de croissance de la larve de stade I (fig.3-4), on peut observer (A, B) le développement, la sclérification et la pigmentation progressif des mandibules du stade II (m). Tous ces phénomènes apparaissent simultanément avec l'esquisse du reste du squelette céphalo-pharyngien et des stigmates postérieurs, ces derniers sont munis de deux fentes respiratoires (C, b). Sans préparation spéciale on peut observer beaucoup de petites larves a cinq crochets buccaux, qui appartiennent à une forme de passage vers le deuxième stade embryonnaire. À l'aide des moyens histologiques, on peut aussi mettre en évidence la future spinulation, qui se forme sous les téguments.
Il est intéressant de signaler que l'armature bucco-pharyngienne du stade suivant se manifeste avant tout par l'apparition des sommets de la mandibule, qui augmentent graduellement et se continuent avec le sclérite pharyngien, entourant l'ancienne armature. À la première mue, le squelette céphalo-pharyngien à trois crochets est éjecte de l'intérieur de celui qui est nouvellement forme. En même temps, on observe l'élimination des papilles respiratoires postérieures (C, a). La succession de toutes ces séquences morpho-histo-physiologiques qui conduisent à la formation de la larve de stade II, se déroulent très rapidement dans les néo-plaies de la muqueuse génitale des moutons. Cela peut se réaliser en deux à trois heures après l'arrivée de la toute jeune larve.
Larve de stade II

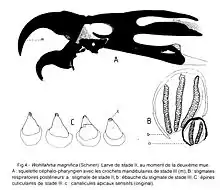
Le deuxième stade (fig. 5) est représenté par des larves à tégument d'un blanc plus clair, qui contraste fortement avec les rangées d'épines grandes, grosses et pigmentées en brun fonce. Les épines ont leurs bases sclérifiées assez larges (D) et leurs sommets plus ou moins arrondis. À l'extérieur de la région céphalique, on observe seulement deux crochets buccaux (A).
En étalant l'armature buccale, on voit les modifications caractéristiques de la nouvelle étape de croissance et on aperçoit aussi une autre paire de bourgeons embryonnaires mandibulaires (m), faiblement sclérifiés et pigmentés au début, qui deviendront les mandibules du dernier stade larvaire. À ce stade, les crochets buccaux sont bien développés et courbés et la pièce basale mandibulaire est et étroite et allongée postérieurement. II y a un sclérite dental et un subhypostomal. Le sclérite hypostomal est grand, allongé et il fait la liaison avec le pharyngien. Les ailes dorsales sont très incisées longitudinalement, tandis que les ailes ventrales sont entières à leur base (fig. 5, A) et ont des ouvertures tardives (fig. 6, A). Le sclérite parastomal est développé et l’arc dorsal du sclérite pharyngien s'allonge devenant de plus en plus gros.
Chaque stigmate respiratoire antérieur (B) a 4-5 papilles. Les postérieurs ont deux fentes (C). l'anneau péritrémal est mince et ouvert, avec une cicatrice à peine perceptible. Dans les étapes ultérieures du développement larvaire, les bourgeons mandibulaires vont croître progressivement (fig, 6, A, m) jusqu'au moment où ils définiront les pièces buccales de la larve de stade III, suivant le même processus que celui décrit pour le passage du stade I au stade II, processus du stade antérieur (décrit plus haut). Les phénomènes d'apparition des formations du dernier âge, à l'intérieur de la larve de stade II, se remarquent aussi dans les changements de la cavité stigmaticale postérieure (B). À l'arrière des stigmates respiratoires à deux fentes (a), les stigmates à trois fentes (b) de la larve adulte se précisent. Avant la deuxième mue, les larves avec deux paires de crochets buccaux se rencontrent très fréquemment. Une paire de crochets, tout l'appareil bucco-pharyngien et les stigmates respiratoires à deux fentes seront éliminés avec l'exuvie.
Larve de stade III
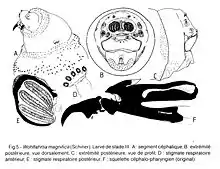
La larve de stade III a une couleur blanc-jaunâtre. Les segments du corps sont généralement entourés de larges ceintures d'épines plus aiguës à l'apex et d'un brun plus clair que les épines de la larve de stade II. Ces épines présentent aussi quelques canalicules microscopiques apicaux à rôle sensitif (fig 6, C, c).
Le segment céphalique (fig. 7, A) a des lobes antennaux, des palpes maxillaires et les sommets des crochets mandibulaires très forts. 11 est entouré d'une ceinture de petites épines, qui constitue la bande antérieure du premier segment thoracique. Celui-ci possède des stigmates antérieurs pourvus de 3-5 papilles respiratoires (D). Les ceintures d'épines sont formées de deux bandes (une antérieure et l'autre postérieure), plus c1aires sur la partie dorsale du corps. La spinulation postérieure est interrompue sur la partie dorsale du segment abdominal VI et manque sur les segments VII-VIII. Le dernier segment tronque au bout (C) présente une cavité ovale et profonde à la moitie supérieure (B). Sur les bords de cette cavité on trouve les tubercules: dorsal, subdorsal (presque indistinct), supéro-latéral, inféro-latéral, subventral, paraventral et ventral (presque indistinct). À l'intérieur de ce dernier segment abdominal on peut observer les deux stigmates respiratoires postérieurs. Sur la partie ventrale du segment terminal, on observe les petits tubercules anaux ainsi que les subanaux en forme de mamelons qui portent beaucoup d'épines notamment sur la bordure anale semi-circulaire antérieure. En général, les épines somatiques récurrentes sont plus développées sur ces sternites.
Chaque stigmate postérieur (E) a un anneau péritrémal ouvert et trois fentes internes allongées. Le bouton (ou la cicatrice) est peu sclérifié, presque indistinct.
Le squelette céphalo-pharyngien est très développé (F). Il présente une paire de mandibules fortes, à crochets buccaux allonges et pointus à l'apex, qui s'amincissent un peu jusqu'à la fin de ce stade. Sous la pièce basale mandibulaire, on trouve les sclérites : dental, labial et subhypostomal. Le sclérite hypostomal est robuste et bien fixe entre la partie antérieure du pharyngien et du parastomal. L'aile dorsale a une scissure longitudinale, caractéristique chez les Sarcophagidae. L'aile ventrale a une ouverture à son extrémité. W. magnifica (Schiner) possède spécifiquement un arc dorsal très fort, sépare partiellement de l'aile dorsale.
Bibliographie
- Blanchard R, « Un cas de myiase par la Sarcophaga magnifica en Roumanie » Bull. Soc. Zool. France 1891;16:25-26.
- (ro) Dinulescu G. & Niculescu A, Parazitologie clinicã veterinarã, Éd. Agro-Silvica, Bucuresti, 1960, 584 p.
- (de) Hennig W, Die Larvenformen der Dipteren. 3. Teil. Akad. Verlag, Berlin, 1952. 628 p.
- (en) James M-T, « The Flies that cause myiasis in man » U.S.Dept. Agric., Miscel. Public. Nr. 621, Washington, 1947, 1, 175 p.
- (en) James M.-T. & Gassner FX, « The immature stages of the fox maggot Wohlfahrtia opaca (CoQ.) » J Parasit. 1947;33(3):241-244.
- (en) Kokcam İ, Şaki CE, « A Case of Cutaneous Myiasis Caused by Wohlfahrtia magnifica » The J. of Dermatol. 2005;32(6):459-463.
- Lehrer AZ, Fromunda V, 1986, « Le développement larvaire du diptère myiasigène Wohlfahrtia magnifica (Schiner)(Diptera, Sarcophagidae) » Bull. Annls. Soc. r. belge Ent/, 122:129-136.
- Lehrer AZ & Lehrer M, 1986, « Soluţie pentru tratarea miazelor, la animale. Certificat de inventator nr. 90 806 », R.S.R., OSIM.
- Lehrer AZ & Lehrer M, 1986, « Unguent pentru tratarea miazelor la animale. Certificat de inventator nr. 90 807 », R.S.R., OSIM.
- Lehrer A, Lehrer M, Verstraeten C, « Les myiases causées aux moutons de Roumanie, par Wohlfahrtia magnifica (Schiner) (Diptera, Sarcophagidae) » Ann. Méd. Vét. 1988;132:475-481.
- LEHRER, A., VERSTRAETEN, C., Expansion parasitologique et géographique de Wohlfahrtyia magnifica (Schiner) (Diptera, Sarcophagidae) en Roumanie. ull. Rech. Agron. Gembloux, 1991, 26(4):563-567.
- LEON, N., Note de parasitologie roumaine. Arch. Parasitol., 1898, 3, 228-236.
- LEON, N., Contributions à l'étude des parasites animaux de Roumanie. Bull. Méd. Nat. Jasi, 1908, 9-10, 1-9.
- LUNGU, T. et col., Patologia si clinica bolilor parazitare (medical-veterinare). Éd. Didacticã si Pedagogicã, Bucuresti, 1982, 312 pp.
- PORTSCHINSKY, L.A., Wohlfahrtia magnifica SCHIN. Sa biologie et son rapport à l'homme et aux animaux domestiques. Bur. Ent. Sci. Com. Min. Agr. Mem., Petrograd, 1916, XI(9): 1-108 (en russe).
- SEGUY, E., Introduction à ]'étude biologique et morphologique des Insectes Diptères, Publ. avul. Mus. Nac., Rio de Janeiro, 1, 1955, 260 pp.
- ŞAKİ, C.E., ÖZER, E. Morphology and Development of Several External Myiasis larvae Recorded in Elazığ. Tr. J. Vet. Anim. Sci., 1999, 23 (4), 723-731.
- ŞAKİ, C.E., ÖZER, E. Morphology and Seasonal Distributions of External Myiasis Files Détermined in Elazığ Province. Tr. J. Vet. Anim. Sci., 1999, 23 (4), 733-746.
- ŞAKİ, C.E., Traumatic Myiasis of Dogs in Elazığ, Turkey. F.Ü. Sag. Bil. Derg., 2004, 18 (1), 29-33.
- ZUMPT, F., Myiasis in man and animals in the Old World. Butterworths, 1965, London, 265 p.
Références
- (en) Lehrer, Z., M. Lehrer, et C. Verstraeten, « Myiasis in sheep provoked by Wohlfahrtia magnifica (Schiner)(Diptera Sarcophagidae) », Annales de Medecine Veterinaire (Belgium), vol. 132, no 6, , p. 475-81.
- Portail des maladies infectieuses
- Portail de la parasitologie