الفيروسات المرتبطة بالغدية
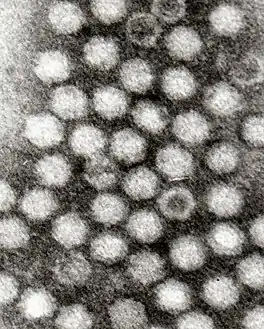
الفيروسات المرتبطة بالغدية (الاسم العلمي: Adeno-associated virus) اختصارًا AAV، هي فيروسات صغيرة تصيب البشر وبعض أنواع الرئيسيات الأخرى. تنتمي هذه الفيروسات إلى جنس ديبيندوبارفوفيروس، والذي ينتمي بدوره إلى عائلة الفيروسات الصغيرة. وهي فيروسات صغيرة (بعرض 20 نانومتر) معيبة النسخ وغير مغلفة وتمتلك جينوم دي إن إيه أحادي السلسلة (إس إس دي إن إيه) بطول 4.8 كيلو قاعدة (kb).[بحاجة لمصدر]
اضغط هنا للاطلاع على كيفية قراءة التصنيف الفيروسات المرتبطة بالغدية | |
|---|---|
 | |
| المرتبة التصنيفية | نوع |
| التصنيف العلمي | |
| فوق النطاق | حيويات |
| مملكة | فيروس |
| فصيلة | فيروسات صغيرة |
| فُصيلة | Parvovirinae |
| جنس | Dependovirus |
| الاسم العلمي | |
| Adeno-associated virus 2 | |
وفقًا للمعرفة الحالية، لا تسبب فيروسات إيه إيه في أي أمراض. تسبب هذه الفيروسات استجابة مناعية خفيفة للغاية. هناك العديد من الميزات الإضافية التي تجعل من إيه إيه في مرشحًا جذابًا لبناء ناقلات فيروسية للعلاج الجيني، ولإنشاء نماذج مرضية بشرية متماثلة النمط الجيني.[1] باستخدام إيه إيه، يمكن أن تصيب نواقل العلاج الجيني الخلايا المنقسمة والمستقرة وأن تستمر في حالة غير صبغية دون الاندماج في جينوم الخلية المضيفة، على الرغم من حدوث اندماج للجينات المنقولة في الجينوم المضيف في الفيروس الأصلي.[2] يمكن أن يكون الاندماج مهمًا في تطبيقات معينة، ولكن قد يكون له أيضًا عواقب غير مرغوب بها. أظهرت التجارب السريرية البشرية الحديثة باستخدام إيه إيه في نتائج واعدة للعلاج الجيني في شبكية العين.[3]
استخدمه في العلاج الجيني
المزايا والعيوب
اجتذب النوع البري لإيه إيه في اهتمام الكثير من الباحثين في العلاج الجيني بسبب عدد من الميزات الخاصة به. ومن أهم هذه الميزات هي عدم قدرة الفيروس على إحداث أمراض. يمكن أن يصيب أيضًا الخلايا غير المنقسمة ولديه القدرة على الاندماج بشكل مستقر في جينوم الخلية المضيفة في موقع معين (يُسمى إيه إيه في إس 1) في الكروموسوم البشري 19.[4][5] هذه الميزة تجعله أكثر قابلية للتنبؤ إلى حد ما من الفيروسات الراجعية، التي تشكل تهديدًا يتمثل في الإدخال العشوائي وتشكل طفرات، والتي يتبعها أحيانًا تطور خلايا سرطانية. يندمج جينوم إيه إيه في بشكل متكرر في الموقع المذكور، بينما يحدث الاندماج العشوائي في الجينوم بتردد ضئيل. مع ذلك، فإن تطوير إيه إيه في كنواقل للعلاج الجيني قد ألغى هذه القدرة الاندماجية عن طريق إزالة البروتينات القفيصة والنسخية من الحمض النووي للناقل. يُدخل الجين المطلوب جنبًا إلى جنب مع محفز نسخ الجين بين المكررات الطرفية المقلوبة (آي تي آر) التي تساعد في تكوين الحمض النووي المتسلسل في النواة بعد تحويل الحمض النووي الناقل أحادي السلسلة بواسطة مركبات بلمرة الحمض النووي للخلية المضيفة إلى حمض نووي ثنائي السلسلة. تشكل نواقل العلاج الجيني المستندة على إيه إيه في أحماض نووية متسلسلة إبيزومية في نواة الخلية المضيفة. في الخلايا غير المنقسمة، لا تتأثر هذه الأحماض النووية المتسلسلة طوال حياة الخلية المضيفة. في الخلايا المنقسمة، يُفقد حمض إيه إيه في النووي خلال الانقسام الخلوي، إذ لا يجري نسج الحمض النووي الإبيزومي مع الحمض النووي للخلية المضيفة.[6] يمكن كشف الاندماج العشوائي لحمض إيه إيه في النووي في الجينوم المضيف ولكنه يحدث بتردد منخفض جدًا.[6] تتميز إيه إيه في أيضًا بتوليد مناعة منخفض جدًا، ويبدو أنها مقيدة بتوليد الأجسام المضادة المعادلة، في حين أنها لا تحفز استجابة خلوية سامة مُحددة بوضوح.[7][8][9] توضح هذه الميزة، إلى جانب القدرة على إصابة الخلايا المستقرة، أفضلية فيروسات إي إي في على الفيروسات الغدانية كنواقل للعلاج الجيني البشري.
مراجع
- "Adeno-associated Virus as a Gene Therapy Vector: Vector Development, Production and Clinical Applications"، Adeno-associated virus as a gene therapy vector: vector development, production and clinical applications، Advances in Biochemical Engineering/Biotechnology، ج. 99، 2005، ص. 119–45، doi:10.1007/10_005، ISBN 978-3-540-28404-8، PMID 16568890.
- "Adeno-associated virus vector integration"، Current Opinion in Molecular Therapeutics، 11 (4): 442–7، أغسطس 2009، PMC 2929125، PMID 19649989.
- "Safety and efficacy of gene transfer for Leber's congenital amaurosis"، The New England Journal of Medicine، 358 (21): 2240–8، مايو 2008، doi:10.1056/NEJMoa0802315، PMC 2829748، PMID 18441370.
{{استشهاد بدورية محكمة}}: الوسيط|إظهار المؤلفين=6غير صالح (مساعدة) - "Site-specific integration by adeno-associated virus"، Proceedings of the National Academy of Sciences of the United States of America، 87 (6): 2211–5، مارس 1990، Bibcode:1990PNAS...87.2211K، doi:10.1073/pnas.87.6.2211، PMC 53656، PMID 2156265.
- "Adeno-associated virus Rep proteins target DNA sequences to a unique locus in the human genome"، Journal of Virology، 71 (10): 7951–9، أكتوبر 1997، doi:10.1128/JVI.71.10.7951-7959.1997، PMC 192153، PMID 9311886.
- "Gene therapy using adeno-associated virus vectors"، Clinical Microbiology Reviews، 21 (4): 583–93، أكتوبر 2008، doi:10.1128/CMR.00008-08، PMC 2570152، PMID 18854481.
- "Immune responses to adenovirus and adeno-associated virus in humans"، Gene Therapy، 6 (9): 1574–83، سبتمبر 1999، doi:10.1038/sj.gt.3300994، PMID 10490767.
- "Latent adeno-associated virus infection elicits humoral but not cell-mediated immune responses in a nonhuman primate model"، Journal of Virology، 73 (10): 8549–58، أكتوبر 1999، doi:10.1128/JVI.73.10.8549-8558.1999، PMC 112875، PMID 10482608.
- "Adeno-associated virus 2-mediated gene transfer in vivo: organ-tropism and expression of transduced sequences in mice"، Gene، 190 (1): 203–10، أبريل 1997، doi:10.1016/S0378-1119(96)00576-8، PMID 9185868.
- بوابة طب
- بوابة علم الأحياء الخلوي والجزيئي
- بوابة علم الفيروسات