نظام بلوري
النظام البلوري في علم البلورات، عبارة عن نظام يسهم في تصنيف المعادن والبلورات حسب التناظر الهندسي لها في فضاء ثلاثي الأبعاد.[1][2][3] يوجد 7 نظم بلورية تتبعها المعادن عند التبلور وهي:
- نظام بلوري مكعب
- نظام بلوري رباعي
- نظام بلوري سداسي
- نظام بلوري ثلاثي
- نظام بلوري معيني قائم
- نظام بلوري أحادي الميل
- نظام بلوري ثلاثي الميل
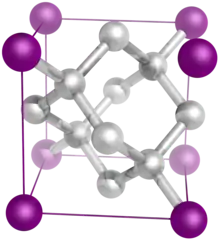

على سبيل المثال فإن كلوريد الصوديوم (ملح الطعام) يتبع النظام البلوري المكعب. يتكون المكعب من 6 أوجه و8 زوايا. فإذا نظرنا إلى وحدة الخلية وهي أصغر بلورة لملح الطعام، وجدنا أن 4 زوايا منها تشغل كل منها أيونا للكلور(-)، والأربعة زوايا الأخرى تشغل كل منها أيونا للصوديوم(+).
يلاحظ تناوب شغل الزوايا: أيون صوديوم (أحمر) يجاوره أيون كلور (أخضر) يجاوره أيون صوديوم يجاوره أيون كلور ... وهكذا، وذلك سواء نظرنا إلى البلورة من اليمين إلا اليسار، أو من أعلى إلى أسفل، أو من الأمام إلى الخلف. فالتبلور عملية منتظمة.
الأنظمة البلورية
التوزيع لل 32 مجموعة نقطية في السبعة أنظمة بلورية كما في الجدول التالي.
| عائلة البلورة | نظام البلورة | مجموعة النقط / فئة البلورة | تعداد سكوينفلايز [الإنجليزية] | تعداد هيرمان-ماوغوين [الإنجليزية] | مدار عديد التفرع [الإنجليزية] | تعداد كوكستير [الإنجليزية] | النوع | الترتيب التناظري [الإنجليزية] | التركيب |
|---|---|---|---|---|---|---|---|---|---|
| ثلاثي الميل | ثلاثي الميل-pedial | C1 | 1 | 11 | [ ]+ | قطبي بتقابل مرآتي | 1 | بديهي | |
| ثلاثي الميل-مسطح | Ci | 1 | 1x | [2,1+] | متناظرة مركزيا | 2 | دوري | ||
| أحادي الميل | أحادي الميل-وتدي | C2 | 2 | 22 | [2,2]+ | قطبي بتقابل مرآتي | 2 | دوري | |
| أحادي الميل-domatic | Cs | m | *11 | [ ] | قطبي | 2 | دوري | ||
| أحادي الميل-موشوري | C2h | 2/m | 2* | [2,2+] | متناظرة مركزيا | 4 | 2×دوري | ||
| معيني قائم | معيني قائم-وتدي | D2 | 222 | 222 | [2,2]+ | تقابل مرآتي | 4 | ثنائي السطح | |
| معيني قائم-هرمي | C2v | mm2 | *22 | [2] | قطبي | 4 | dihedral | ||
| معيني قائم-هرمين متقابلين | D2h | mmm | *222 | [2,2] | متناظرة مركزيا | 8 | 2×ثنائي السطح | ||
| رباعي | رباعي-هرمي | C4 | 4 | 44 | [4]+ | قطبي بتقابل مرآتي | 4 | دوري | |
| رباعي-وتدين متقابلين | S4 | 4 | 2x | [2+,2] | 4 | دوري | |||
| رباعي-هرمين متقابلين | C4h | 4/m | 4* | [2,4+] | متناظرة مركزيا | 8 | 2×دوري | ||
| رباعي-شبه منحرف | D4 | 422 | 422 | [2,4]+ | تقابل مرآتي | 8 | ثنائي السطح | ||
| رباعي-شبه منحرف | C4v | 4mm | *44 | [4] | قطبي | 8 | ثنائي السطح | ||
| رباعي-أطوال مختلفة | D2d | 42m or 4m2 | 2*2 | [2+,4] | 8 | ثنائي السطح | |||
| رباعي مزدوج-هرمين متقابلين | D4h | 4/mmm | *422 | [2,4] | متناظرة مركزيا | 16 | 2×ثنائي السطح | ||
| سداسي | ثلاثي | ثلاثي مزدوج-هرمي | C3 | 3 | 33 | [3]+ | قطبي بتقابل مرآتي | 3 | دوري |
| متوازي السطوح المعينة | S6 (C3i) | 3 | 3x | [2+,3+] | متناظرة مركزيا | 6 | دوري | ||
| ثلاثي-شبه منحرف | D3 | 32 or 321 or 312 | 322 | [3,2]+ | تقابل مرآتي | 6 | ثنائي السطح | ||
| ثلاثي مزدوج-هرمي | C3v | 3m or 3m1 or 31m | *33 | [3] | قطبي | 6 | ثنائي السطح | ||
| ثلاثي مزدوج-سطوح مختلفة | D3d | 3m or 3m1 or 31m | 2*3 | [2+,6] | متناظرة مركزيا | 12 | ثنائي السطح | ||
| سداسي | سداسي-هرمي | C6 | 6 | 66 | [6]+ | قطبي بتقابل مرآتي | 6 | دوري | |
| ثلاثي-هرمين متقابلين | C3h | 6 | 3* | [2,3+] | 6 | دوري | |||
| سداسي-هرمين متقابلين | C6h | 6/m | 6* | [2,6+] | متناظرة مركزيا | 12 | 2×دوري | ||
| سداسي-شبه منحرف | D6 | 622 | 622 | [2,6]+ | تقابل مرآتي | 12 | ثنائي السطح | ||
| سداسي مزدوج-هرمي | C6v | 6mm | *66 | [6] | قطبي | 12 | ثنائي السطح | ||
| ثلاثي مزدوج-هرمين متقابلين | D3h | 6m2 or 62m | *322 | [2,3] | 12 | ثنائي السطح | |||
| سداسي مزدوج-هرمين متقابلين | D6h | 6/mmm | *622 | [2,6] | متناظرة مركزيا | 24 | 2×ثنائي السطح | ||
| مكعب | رباعية الأوجه | T | 23 | 332 | [3,3]+ | تقابل مرآتي | 12 | متناوب | |
| رباعية الأوجه | Td | 43m | *332 | [3,3] | 24 | متماثل | |||
| متضاعف | Th | m3 | 3*2 | [3+,4] | متناظرة مركزيا | 24 | 2×متناوب | ||
| جيرسكوبية | O | 432 | 432 | [4,3]+ | تقابل مرآتي | 24 | متماثل | ||
| سداسي الثماني الأوجه | Oh | m3m | *432 | [4,3] | متناظرة مركزيا | 48 | 2×متماثل | ||
الأنظمة الشبكية
توزيع أنواع الشبكات البرافيه ال 14 في الأنظمة الشبكية السبعة كما في الجدول التالي:
| الأنظمة الشبكية السبعة | شبكات برافيه ال 14 | |||
| ثلاثي الميل (متوازي السطوح) | 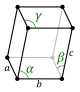 | |||
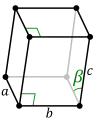
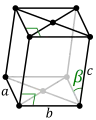
| أحادي الميل (المنشور الأيسر مع قاعدة متوازي أضلاع، ينظر إليها من فوق) |
بسيط | قاعدة-ممركزة | ||
 |
 | |||
| معيني قائم (متوازي مستطيلات) | بسيط | قاعدة-ممركزة | جسم-ممركز | وجه-ممركز |
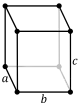 |
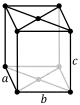 |
 |
 | |
| رباعي (مربع متوازي مستطيلات) | بسيط | جسم-ممركز | ||
 |
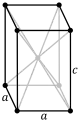 | |||
| ثلاثي (شبه منحرف ثلاثي) | 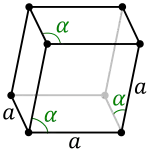 | |||
| سداسي (سداسي عادي متمركز) |  | |||
| مكعب (متساوي القياس؛ مكعب) | بسيط | جسم-ممركز | وجه-ممركز | |
 |
 |
 | ||
طرق تعيين البناء البلوري
الدراسات التي تقوم بتعيين البناء البلوري للأملاح والمعادن تعتمد على طرق القياس الآتية:
كما يمكن تعيين البناء البلوري المغناطيسي بواسطة حيود النيوترونات.
اقرأ أيضًا
مراجع
- Brown, H.؛ Bülow, R.؛ Neubüser, J.؛ Wondratschek, H.؛ Zassenhaus, H. (1978)، Crystallographic Groups of Four-Dimensional Space، New York: Wiley.
{{استشهاد بكتاب}}: تحقق من التاريخ في:|السنة=/|تاريخ=mismatch (مساعدة) - Whittaker, E. J. W. (1985)، An Atlas of Hyperstereograms of the Four-Dimensional Crystal Classes، Oxford & New York: Clarendon Press.
- Flack, Howard D. (2003)، "Chiral and Achiral Crystal Structures"، Helvetica Chimica Acta، 86 (4): 905–921، doi:10.1002/hlca.200390109.
- بوابة كيمياء فيزيائية
- بوابة الفيزياء
- بوابة الكيمياء
- بوابة علم الأحجار الكريمة والمجوهرات
- بوابة علم المواد
- بوابة علم طبقات الأرض