بورات
البورات هي مجموعة واسعة من الأنيونات الحاوية على عنصري البورون والأكسجين، وهي من حيث التركيب الكيميائي أملاح أو إسترات حمض البوريك. يمكن لمركبات البورات أن تكون بسيطة، أو أن تكون مركبة من عدد كبير من وحدات BO3 المستوية الثلاثية أو من وحدات BO4 رباعية السطوح، والتي تكون موصولة ببعضها البعض عبر تشاركها بذرات الأكسجين،[1] ويمكن أن تكون خطّية أو حلقية.
يوجد عنصر البورون في الطبيعة غالباً على شكل بورات، وتسمّى المعادن الحاوية على هذه الأملاح اسم معادن البورات.
الوفرة الطبيعية والتحضير
يوجد البورون على عدة أشكال من معادن البورات في الطبيعة مثل البورق والبوراسيت والموليمانيت والساسوليت والكيرنيت والأوليكسيت.
تحضر البورات بشكل تقليدي من تفاعل حمض البوريك مع قاعدة مثل محلول هيدروكسيد الصوديوم فينتج بورات الصوديوم
الخصائص

يمكن اعتبار أن البورات جميعها هي مشتقات من حمض البوريك B(OH)3، وهو حمض ضعيف (pKa = 8.98[2])، والذي تعود حموضته إلى تفاعل الحلمهة مع الماء ليعطي رباعي هيدروكسي البورات محرراً بروتون:[3]
إن أيون البورات 3−BO3، والتي تعرف باسم أورثو بورات، له بنية جزيئية مستوية ثلاثية وذلك حسب نظرية تنافر أزواج إلكترونات غلاف التكافؤ (VSEPR). من الأمثلة عليها أوروثو بورات الكالسيوم Ca3(BO3)2، والذي يوجد في الحالة الصلبة.[4] إن أنيون أورثو البورات له بنية مشابهة لبنية أنيون الكربونات 2−CO3 المتساوي إلكترونياً معه.
يوجد العديد من مركبات ميتا البورات، والتي هي مشتقة من حمض ميتا بوريك، والتي لها الصيغة العامة BO2)n-n) مثل ميتا بورات الكالسيوم Ca(BO2)2. إن مركبات ميتا البورات، يمكن أن تكون على شكل مفرد، أو تكون على شكل سلاسل بوليمرية.
يمكن أن يتفاعل حمض البوريك مع الكحولات المتعددة (مثل الغليسيرين أو المانيتول) ليعطي استرات بورات حلقية (معقدات متمخلبة).
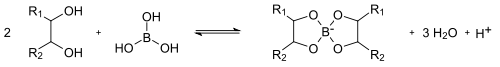
في حال وجود ذرتي أكسجين مرتبطتين بشكل مباشر في البورات نحصل على مركبات فوق البورات.
الكشف عن البورات

من أجل إجراء تحليل نوعي سريع للكشف عن البورات يمكن إضافة المادة المراد تحليلها إلى أنبوب أو وعاء اختبار، ثم يضاف الميثانول وبضع قطرات من حمض الكبريتيك، فيتشكل ثلاثي ميثيل البورات، والذي اختبار اللهب له يعطي لوناً أخضر مميز.[5]
من أجل إجراء تحليل كمّي يمكن استخدام طريقة الكركومين، وهي تتضمن التقاعل بين الكركومين وحمض البوريك، أو البورات، حيث يتشكل معقد أحمر اللون من مادة تدعى روزوسيانين، والتي يقاس تركيزها عن طريق قياس الألوان.
استرات البورات
إن استرات البورات هي مركبات عضوية لها الصيغة العامة B(OR)3، حيث R هو ألكيل أو أريل. يمكن تحضير هذه المركبات من تفاعل تكاثف بين حمض البوريك والكحول. يضاف عادة أثناء التحضير مركب ساحب للماء مثل حمض الكبريتيك.[6]
إن استرات البورات هي مركبات متطايرة ويمكن تنقيتها بالتقطير. تستخدم هذه العملية من أجل تحليل كميات نزيرة من البورات ومن أجل تحليل البورون في الفولاذ.[7]
الاستخدامات
تستخدم أنواع مختلفة من البورات في تركيب مواد حفظ الخشب، كما تدخل البورات في تركيب المحاليل المنظمة.
يستخدم ميتا بورات الليثيوم أو رباعي بورات الليثيوم، أو مزيح منهما، من أجل تحضير عينات التحليل من أجل فلورية الأشعة السينية ومطيافية الامتصاص الذري وتقنيات البلازما المقترنة بالتحريض.
المراجع
- Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN 0-12-352651-5
- N. Ingri, Acta Chem. Scand., 16, 439 (1962)
- Atkins؛ وآخرون (2010)، Inorganic Chemistry (ط. 5th)، Oxford University Press، ص. 334، ISBN 9780199236176.
{{استشهاد بكتاب}}: Explicit use of et al. in:|الأخير=(مساعدة) - Vegas, A. (1985)، "New description of the Ca3(BO3)2 structure"، Acta Crystallographica Section C Crystal Structure Communications، 41 (11): 1689–1690، doi:10.1107/S0108270185009052، ISSN 0108-2701.
- Vogel, Arthur I.; Svehla, G. (1979), Vogel's Textbook of Macro and Semimicro Qualitative Inorganic Analysis (5th ed.), London: Longman, ISBN 0-582-44367-9
- Brown, Herbert C.؛ Mead, Edward J.؛ Shoaf, Charles J. (1956)، "Convenient Procedures for the Preparation of Alkyl Borate Esters"، J. Am. Chem. Soc، 78 (15): 3613–3614، doi:10.1021/ja01596a015.
- Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K. (2000), Vogel's Quantitative Chemical Analysis (6th ed.), New York: Prentice Hall, p. 666, ISBN 0-582-22628-7
- بوابة الكيمياء
- بوابة علوم الأرض