تحليل كهربائي للماء
التحليلُ الكهربائيُّ للماء هو عملية إجراء تحليل كهربائي لجزيئات الماء H2O بفصله إلى مكوناته وهي الأكسجين O2 والهيدروجين وذلك عن طريق تمرير تيار كهربائي في الوسط المائي.
وتكون المعادلة كالتالي:
2H2O(l)⟶2H2(g)+O2g
المبدأ
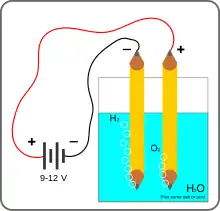
يوصل منبع تيار كهربائي إلى قطبين كهربائيين (مسرَيَيْن) موضوعين في الماء. عادةً ما تكون هذه الأقطاب الكهربائية مصنوعة من فلزات خاملة كيميائياً مثل البلاتين أو الإريديوم. يتشكل نتيجة هذه العملية غاز الهيدروجين على المهبط في حين يتشكل الأكسجين على المصعد.
في الشروط المثالية تكون كفاءة التحليل الكهربائي للماء (كفاءة فاراداي) تامة إذا كانت كمية الهيدروجين المولدة تساوي ضعف كمية الأكسجين من حيث عدد المولات، وتكون الكميات الناتجة متناسبة مع الشحنة الكهربائية المارة في المحلول.[1] عملياً، يختلف الأمر على أرض الواقع حيث أن هنالك العديد من التفاعلات الجانبية التي يمكن أن تحدث، وهي بذلك تعطي نواتج ثانوية مقلّلةً بذلك من الكفاءة المنشودة.
يتطلب إجراء عملية التحليل الكهربائي للماء استخدام طاقة (عملية ماصّة للحرارة) وذلك عن طريق تطبيق فرق جهد عالٍ للتغلب على الحاجز الطاقي للمكونات. بدون استخدام هذه الطاقة لا تحدث عملية تحليل كهربائي للماء، لأن الماء لا يتفكك إلى مكوناته من تلقاء ذاته، بسبب محدوديّة التأين الذاتي للماء.
الاستخدامات
استخدمت طريقة التحليل الكهربائي للماء في السابق لإنتاج الهيدروجين، إلا أن الهيدروجين حالياً ينتج بطريقة أكثر كفاءة من الوقود الأحفوري.[2]
طالع أيضاً
المراجع
- Carmo, M (2013)، "A comprehensive review on PEM water electrolysis"، Journal of Hydrogen Energy، doi:10.1016/j.ijhydene.2013.01.151، مؤرشف من الأصل في 14 ديسمبر 2019.
- Staff (2007)، "Hydrogen Basics — Production"، Florida Solar Energy Center، مؤرشف من الأصل في 22 أكتوبر 2018، اطلع عليه بتاريخ 05 فبراير 2008.
- بوابة الكيمياء
- بوابة طاقة
- بوابة كهرباء