درجة حرارة حرجة
درجة الحرارة الحرجة أو النقطة الحرجة في الكيمياء (بالإنجليزية: Critical point أو Critical Temperature) هي درجة الحرارة التي عندها تتساوى خواص السائل مع خواص بخاره حيث يضيع السطح الفاصل بينهما.[1][2][3] عند زيادة درجة حرارة سائل يحدث توازن لمعدل التبخر مع الضغط. فعندما نزيد درجة حرارة السائل يبدا الغليان عند درجة حرارة معينة (100 درجة مئوية للماء عند الضغط الجوي) فإذا أزدنا الضغط ارتفعت درجة الغليان أيضا ويكون لدينا خلال تلك العملية يكون لدينا طورين للمادة: الطور السائل، والطور الغازي. تتميز النقطة الحرجة بأنها درجة الحرارة (والضغط) الحرجين التي عندها يتلاشى الفرق بين الطورين، وتصبح المادة في حالة وسطية بين السائل وبخاره، يسمى السائل فوق تلك النقطة الحرجة «سائل فوق حرج» Supercritical fluid .
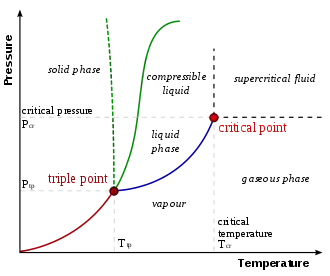
مخطط الطور
يبين الشكل رسما بيانيا للثلاتة أطوار للماء: الحالة السائلة (أعلى إلى اليمين)، والحالة الغازية (بخار) [أسفل]، والحالة الصلبة (ثلج) [أعلى إلى اليسار]. ويبين المخطط تحول تلك الحالات من واحدة إلى أخرى تحت تأثير درجة الحرارة (المحور السيني) والضغط (المحور الرأسي)، وذلك باعتبار أن الحجم ثابت لا يتغير.
يمثل الخط الأزرق غليان الماء وتحوله إلى بخار، حيث تكون الحالتان موجودتان كالمعتاد ومنفصلتان. بارتفاع الضغط ترتفع درجة حرارة الغليان وبالعكس عندما ينخفض الضغط تنخفض تبعا درجة الغليان. وطالما نتحرك على الخط الأزرق يكون لدينا حالتين (ماء وبخار) في حالة توازن، أي ماء يغلى وفوقه بخار ساخن يتبخر بمعدل معين. ومع استمرار رفع الضغط ترتفع بالتالي درجة الغليان حتي نصل إلى نقطة تسمى النقطة الحرجة (critical point)، وعندها نصل إلى حالة لا يكون فيها الماء سائلا ولا بخارا، بل هي حالة تجمع بين الاثنين في مخلوط مشبع من الماء والبخار عالي الضغط والحرارة. وتبلغ النقطة الحرجة للماء عند درجة حرارة 647 كلفن (374 درجة مئوية) وتتسم تلك النقطة أيضا بضغط حرج، وهي للماء عند 218 ضغط جوي.
في مخطط الطور (انظر الشكل) لا يمثل الخط الأخضر حالة الماء وإنما يمثل موادا أخرى غير الماء. ولكن الخط الأخضر المنقط يمثل حالات التوازن بين طور الماء السائل وطور الثلج عند درجات حراره وضغوط مختلفة.
الضغط الحرج critical pressure هو ضغط التبخر عند درجة الحرارة الحرجة. في الشكل الموضح هي النقطة الحمراء عند نهاية الخط الأزرق. تسمى الحالة فوق تلك النقطة «مائع فوق حرج» supercritical fluid .
الحجم الجزيئى الحرج هو حجم واحد مول من المادة عند درجة الحرارة الحرجة والضغط الحرج.
الخواص الحرجة تختلف من مادة لأخرى، كما في حالة نقطة التبخر ونقطة التجمد للماء. الخواص الحرجة للعديد من المواد النقية متوفرة في جداول خاصة. الحصول على الخواص الحرجة لمخاليط مختلفة هي من المسائل التي تحتاج إلى الاختبارات المعملية.
مراجع
- "معلومات عن درجة حرارة حرجة على موقع psh.techlib.cz"، psh.techlib.cz، مؤرشف من الأصل في 19 ديسمبر 2019.
- "معلومات عن درجة حرارة حرجة على موقع thes.bncf.firenze.sbn.it"، thes.bncf.firenze.sbn.it، مؤرشف من الأصل في 19 ديسمبر 2019.
- "معلومات عن درجة حرارة حرجة على موقع britannica.com"، britannica.com، مؤرشف من الأصل في 11 مارس 2016.
انظر أيضا
- بوابة الفيزياء
- بوابة كهرباء
- بوابة كهرومغناطيسية
- بوابة الكيمياء
- بوابة كيمياء فيزيائية