دورة كارنو
دورة كارنو في الفيزياء وفي الديناميكا الحرارية هي إحدى الدورات الديناميكية الانعكاسية المشهورة والتي سميت باسم المهندس الفرنسي سادي كارنو (1796 - 1832)م
| الديناميكا الحرارية |
| فروع الديناميكا الحرارية |
| ترموديناميكا الغلاف الجوي | ترموديناميكا بيولوجية | ترموديناميك الثقب الأسود | ترموديناميك كيميائي | ترموديناميك كلاسيكي | توازن ترموديناميكي | ترموديناميك اللاتوازن | ترموديناميك الظاهراتي | ديناميكا لونية كمية | ترموديناميكا إحصائية |
| قوانين الديناميكا الحرارية |
| القانون الصفري | القانون الأول | القانون الثاني | القانون الثالث |
| العمليات الديناميكية الحرارية |
| عملية متساوية الضغط | عملية متساوية الحرارة | عملية كظومة (أديباتية) | عملية متساوية الأنتالبية |
| مصطلحات |
| نظام دينامي حراري | حالة نظام ديناميكي | نظام مغلق | نظام مفتوح | نظام معزول | دورة حركة حرارية| دورة كارنو | دورة أوتو |دورة ديزل |دورة رانكن |تفاضل تام |
| خواص ترموديناميكية للسوائل |
|
وتمثل دورة كارنو دورة حرارية نظرية لها انعكاس كبير في الديناميكا الحرارية حيث أنها تعطي الحد الأقصى للحصول على الشغل من خلال دورة حرارية تعمل بين درجتين مختلفتين للحرارة.[1][2][3] وبواسطة دورة كارنو يمكن حساب الكفاءة الحرارية لآلة معينة. أي أنها تعطينا الجزء من الحرارية الكلية التي نضخها في الآلة لنحصل منها على شغل أو عمل.
ومثال على ذلك آلة الاحتراق الداخلي حيث يدخل مخلوط الوقود والهواء المكبس، ثم يحترق المخلوط بفعل الشرارة الكهربائية الصادرة من شمعة الاحتراق. فيندفع المكبس لتشغيل الآلة. وبتناوب عمل المكابس سواء كانوا أربعة مكابس أو أكثر تشتغل الآلة وتُنتج شغلا وهو حركة السيارة.
وتقاس كفاءة أي آلة مثل آلة الاحتراق الداخلي أو الآلة البخارية بمقارنتها بدورة كارنو.
وكان كارنو مهندسا في الجيش الفرنسي وكرس جهده في البحث العلمي وخاصة الظاهرة الحرارية ويعتبر مؤسس لعلم الديناميكا الحرارية.
وصف دورة كارنو
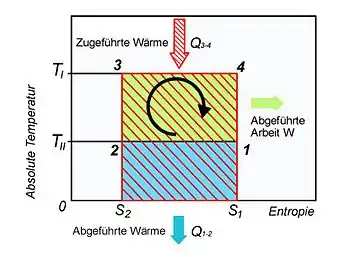
في هذا الشكل يعني اللون الأحمر الوسط الساخن (الاحتراق)، واللون الأزرق الوسط البارد (العادم). وتتكون دورة كارنو من عمليتين تكون فيهما درجة الحرارة ثابتة. وهاتان العمليتان ممثلتان بخطين أفقيين في الرسم، في أحدهما تسري العملية عند درجة حرارة عالية T1 وثابتة، والأخرى عند درجة حرارة منخفضة T2 وثابتة أيضا. بالإضافة إلى العمليتين السابقتين تتكون الدورة من عمليتان تتصفان بالعملية الكظومة يكون الغاز فيها معزولا حراريا. وهاتان عمليتان تتغير فيهما الحرارة إما صعودا من نقطة 2 إلى 3 في الدورة، أو هبوطا من 4 إلى 1. (تتصف العملية الكظومة بأنها حالة يكون النظام فيها معزولا حراريا عن الخارج ويمكن أن نصل لذلك إذا تمت المرحلة الكظومة بسرعة فيقل بذلك التبادل الحراري مع المحيط. بتعبير آخر يتسم التغير الكظومي بثبات الإنتروبية S) : وكما في الشكل تتكون دورة كارنو من أربعة مراحل، تعود فيها الدورة بعد اكتمالها إلى نقطة الابتداء.
إذا رمزنا هنا الإننتروبية بالحرف S واعتبرنا أن الدورة انعكاسية نحصل على العلاقة التالية لزيادة الإنتروبية حيث تعتمد على كمية الحرارة Q ودرجة الحرارة T:
ويمكننا كتابة المعادلة في الصورة التالية :
وتتكون دورة كارنو من الأربعة مراحل التالية:
1. تغير في الحالة من 1 إلى النقطة 2 : عملية ضغط الغاز مع ثبات الحرارة.
حيث تُفقد من الغاز كمية من الحرارة عند درجة حرارة ثابتة، مما يتسبب في تخفيض حجم الغاز من V1 إلى V2 .
وتُعطى كمية الحرارة المفقودة (العادم) من النظام بالعلاقة :
وطبقا لتلك المعادلة تكون كمية الحرارة المفقودة سالبة (مثال خروج العادم في درجة حرارة المحيط):
2. تغير في الحالة من 2 إلى النقطة 3 : عملية ضغط كظومية ( في انعزال حراري وبدون احتكاك).
خلال تلك المرحلة يُعزل الغاز كظوميا ويضغط بوساطة مكبس، فترتفع درجة حرارة الغاز إلى TI :
أي لا يحدث تغير في كمية حرارة الغاز خلال الحالة من 2 إلى 3.
3. تغير في الحالة من 3 إلى النقطة 4 : تمدد الغاز مع ثبات درجة الحرارة TI.
عند درجة الحرارة العالية يكتسب الغاز كمية حرارة كبيرة من المصدر ويتمدد عند درجة حرارة ثابتة TI.
وتبلغ كمية الحرارة المكتسبة من المصدر الحراري :
4. تغير في الحالة من النقطة 4 إلى النقطة 1 : تمدد كظومي بمعزل حراري وبدون احتكاك.
خلال تلك المرحلة يتمدد الغاز محركا لذراع ويؤدي شغل، ويعود إلى نقطة البداية ثانيا ً. أي يعود للحجم والضغط ودرجة الحرارة الابتدائية.
ويمكن تمثيل الدورة بآلة الاحتراق الداخلي حيث يسحب المكبس الوقود الغازي مختلطا بالهواء عند درجة حرارة الغرفة ثم يكبسه ويصغر حجم الغاز، ثم ينفجر الغاز بفعل شمعة الاحتراق، فيتمدد الغاز فوريا ويدفع ذراع تحريك الموتور، ويخرج العادم عند درجة الحرارة المنخفضة. وتبدأ الدورة من جديد.
كفاءة آلة كارنو

1.سحب رذاذ الجازولين
2. ضغط رذاذ الجازولين
3. الإشعال
4. خروج العادم
ينص القانون الأول للحرارة على :
حيث: U الحرارة الداخلية للغاز
W الشغل الناتج عن الآلة
Q كمية الحرارة.
بعد مرور دورة كارنو خلال الأربعة مراحل الموصوفة أعلاه تعود جميع متغيرات الدورة إلى نقطة البداية. أي أن الطاقة الداخلية للغاز تعود إلى أصلها ويصبح التغير فيها () يساوي صفرا.
أي أن الشغل المكتسب من الآلة :
وبذلك نحصل على :
وتقدر كفاءة الآلة طبقا لكارنو بالنسبة بين الشغل المكتسب من الآلة إلى كمية الحرارة المستهلكة، أي :
نلاحظ الآتي:
- أن كفاءة الآلة تتناسب تناسبا طرديا مع الفرق بين درجتي حرارة التشغيل (T1 - T2).
- أن أعلى كفاءة للآلة لا يمكن الحصول عليها إلا بأن تكون درجة حرارة العادم تساوي الصفر المطلق. ومن الواضح أن هذا لا يمكن الوصول إليه، فالعادم في حياتنا العملية تصل درجة حرارته إلى درجة الحرارة المحيطة(T2) وهي على احسن الفروض نحو 300 كلفن.
- أن الكفاءة تزيد بارتفاع درجة حرارة التشغيل (T1).
- يبدو مما سبق أن دورة كارنو هي دورة مثالية يتحقق فيها عزل النظام التام عن المحيط، بحيث لا يحدث فيها أي فقد للحرارة ولا فاقد بطريق الاحتكاك. وهذا لا يمكن تحقيقه عمليا. لذلك تمثل دورة كارنو الحد المثالي للكفاءة.
- تتفق تلك النتيجة مع القانون الثاني للحرارة الذي ينص على أنه ليس من الممكن تحويل الطاقة الحرارية كليا إلى طاقة حركة، وهذا قانون هام من قوانين الطبيعة.
تطبيق عملي
يضع القانون الثاني للحرارة حدا جذريا لكفاءة الآلة الحرارية. وحتي لو فرض أن الآلة مثالية ولا تفقد حرارة بالاحتكاك فهي لا تستطيع تحويل كمية الحرارة المعطاة لها إلى شغل. والحدود المتحكمة في ذلك هي درجة الحرارة الداخلة في الآلة (أو المتولدة فيها) T1، ودرجة حرارة الوسط المحيط لها والذي تخرج فيه الغاز العادم T2، ونعني هنا درجات الحرارة المطلقة أي المقاسة بالكلفن. وتعطينا معادلة كارنو العلاقة لآلة تعمل بين تلك الدرجتين كالآتي :
وهذا الحد يسمى كفاءة دورة كارنو وهي تعطي كفاءة آلة مثالية لا يحدث فيها أي فقد للحرارة أو احتكاك. ولا يمكن لأي آلة عملية تعدي ذلك الحد مهما كانت تركيبته.
ومثال على ذلك مثال بخار ساخن درجة حرارته T1، يدخل توربينا لتوليد الطاقة الكهربائية. أو الوقود الذي يحترق داخل محرك الاحتراق الداخلى. وتعني T2 درجة الحرارة المنخفضة وتكون عادة حرارة الطقس المعتادة أو درجة حرارة ماء النهر الذي يتلقى العادم من الآلة.
فمحرك السيارة يحرق البنزين عند درجة حرارة T1=1089 كلفن ودرجة حرارة الجو نحو T2=294 كلفن، وعلى ذلك يمكننا حساب الحد الأقصى لكفاءة المحرك، وهو يعطى بالعلاقة الآتية :
ونظرا لظروف تشغيل آلة حقيقية يحدث فيها احتكاك وفقد لا خلاص منه للحرارة تكون كفاءة الآلة بعيدة عن كفاءة دورة كارنو. وتصل كفاءة محرك الاحتراق الداخلى 25 % فقط. وتبلغ كفاءة محطات القوى التي تجمع بين إنتاج الطاقة الكهربائية والاستفادة من الماء الساخن الناتج في تدفئة البيوت وتشغيل بعض عمليات المصانع الكيماوية، تقترب كفاءتها من 46 %، وهي لا تزال تقل عن كفاءة دورة كارنو بمقدار 15 نقطة. وبينما تُطبق دورة كارنو على الآلات التي تعمل بالحرارة توجد أنواع من الأجهزة التي تحول طاقة الوقود مباشرة إلى شغل من دون اللجوء إلى احراقه، ومثال لذلك نجده في خلايا الوقود والتي قد تتعدي كفاءتها كفاءة كارنو.
وكما يتضح لنا أنه طالما كانت درجة الحرارة الباردة T1 محدودة بدرجة حرارة الجو، يلجأ مصممو الآلات إلى رفع درجة حرارة تشغيل الآلة من أجل رفع الكفاءة.
انظر أيضا
مراجع
- Ignacio A. Martínez؛ وآخرون (06 يناير 2016)، "Brownian Carnot engine"، Nature Physics، ص. 67–70، مؤرشف من الأصل في 14 أبريل 2020.
{{استشهاد بخبر}}: Explicit use of et al. in:|مؤلف=(مساعدة) - Nicholas Giordano (13 فبراير 2009)، College Physics: Reasoning and Relationships، Cengage Learning، ص. 510، ISBN 0-534-42471-6، مؤرشف من الأصل في 16 يوليو 2017.
- N. A. Sinitsyn (2011)، "Fluctuation Relation for Heat Engines"، J. Phys. A: Math. Theor.، 44: 405001، arXiv:1111.7014، Bibcode:2011JPhA...44N5001S، doi:10.1088/1751-8113/44/40/405001.
- بوابة طاقة
- بوابة الفيزياء