عبر الخلايا
يعد عبر الخلايا(المعروف أيضًا باسم cytopempsis) [1] نوعًا من النقل عبر الخلايا حيث يتم نقل الجزيئات الكبيرة المختلفة عبر الجزء الداخلي من الخلية. يتم التقاط الجزيئات الكبيرة في حويصلات على جانب واحد من الخلية، ويتم رسمها عبر الخلية، ويتم إخراجها على الجانب الآخر. تتضمن أمثلة الجزيئات الكبيرة المنقولة IgA ، [2] ترانسفيرين، [3] والأنسولين.[4] في حين أن كثرة الخلايا الظاهرة يلاحظ بشكل شائع في الخلايا الظهارية، فإن العملية موجودة أيضًا في مكان آخر. تُعد الشعيرات الدموية في الدم موقعًا معروفًا جيدًا لامتصاص الخلايا، [5] الرغم من أنها تحدث في خلايا أخرى، بما في ذلك الخلايا العصبية، [6] الخلايا العظمية [7] وخلايا الأمعاء.[8]
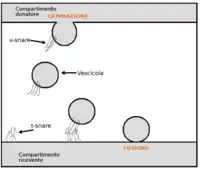
النظام
يختلف تنظيم عبر الخلايا بشكل كبير بسبب العديد من الأنسجة المختلفة التي لوحظت فيها هذه العملية. تم تحديد آليات مختلفة من الأنسجة الخلوية محددة الأنسجة. وقد ثبت أن بريفلدين أ، وهو مثبط شائع الاستخدام في نقل من الشبكة إندوبلازمية إلى - حهاز غولجي، الذي وضح أنه يثبط تخلخل الخلايا في خلايا الكلى للكلاب، والذي قدم الأدلة الأولى عن طبيعة تنظيم تحويل الخلايا.[9] وقد تم أيضًا تنظيم عملية تحويل الخلايا في خلايا الكلى للكلاب في الغشاء القمي تبواسطة راب17 ، [10] وكذلك راب11أ و رراب25.[11] أظهرت المزيد من الدراسة على خلايا الكلى في الكلاب أن سلسلة إشارات تتضمن فسفرة معدل الترشيح الكلوي المقدر عن طريق يس مما يؤدي إلى تنشيط راب 11 فيب 5 بواسطة مابك 1 ينظم عملية تحويل الخلايا.[12] وقد ثبت أن كثرة الكُرَيَّات مُثبَّتة بمزيج من البروجسترون والاستراديول متبوعًا بالتنشيط بوساطة البرولاكتين في غدة الأرنب عند الحمل.[13] في الغدة الدرقية، ينظم تحويل الخلايا الجريبية بشكل إيجابي بواسطة هرمون منبه الدرقية. ثبت أن فسفرة الكافولين 1 التي يسببها بيروكسيد الهيدروجين أمر بالغ الأهمية لتفعيل عبر الخلايا في الأنسجة الوعائية الرئوية.[14] لذلك يمكن الاستنتاج أن تنظيم عبر الخلايا هو عملية معقدة تختلف بين الأنسجة.
دورها في التسبب بالأمراض
بسبب وظيفة عبر الخلايا كعملية تنقل الجزيئات الضخمة عبر الخلايا، يمكن أن تكون آلية ملائمة يمكن من خلالها لمسببات الأمراض أن تغزو الأنسجة. ثبت أن عبر الخلايا أمر حاسم لدخول <i id="mwTg">كورونوباكتور ساكازاكي</i> عبر الظهارة المعوية وكذلك حاجز الدم والدماغ.[15] وقد ثبت أن الليستريا المستوحدة تدخل تجويف الأمعاء عن طريق عبر الخلايا عبر الخلايا الكأسية.[16] وقد ثبت أن توكسين شيغا الذي تفرزه <i id="mwWg">بكتيريا. كولي. أي</i> المعوية النزفية يتم نقله إلى تجويف الأمعاء.[17] استنتاجا من هذه الأمثلة، يمكن القول أن عبر الخلايا أمر حيوي لعملية التسبب في مجموعة متنوعة من العوامل المعدية.
التطبيقات السريرية
تستكشف شركات الأدوية، مثل لاندبيك، حاليًا استخدام عبر الخلايا كآلية لنقل الأدوية العلاجية عبر الحاجز الدموي الدماغي البشري. [بحاجة لمصدر] يمكن أن يساعد استغلال آلية النقل الخاصة بالجسم في التغلب على الانتقائية العالية لـ الحاجز الدموي الدماغي، والتي عادة ما تمنع امتصاص معظم الأجسام المضادة العلاجية في الدماغ والجهاز العصبي المركزي (CNS). واجهت شركة الأدوية جينينتيك، بعد تركيب جسم مضاد علاجي أعاق بشكل فعال وظيفة إنزيم باكي، مشاكل في نقل مستويات كافية وفعالة من الجسم المضاد داخل الدماغ. BACE1 هو الإنزيم الذي يعالج بروتينات السلائف النشواني إلى الببتيدات النشوانية، بما في ذلك الأنواع التي تتجمع لتشكيل لويحات النشواني المرتبطة بمرض الزهايمر. [بحاجة لمصدر] ويتم نقل الجزيئات عبر حاجز الظهارية أو البطانية من جانب واحد عن طريقين: 1) الطريق العابر من خلال حجرة داخل الخلايا للخلية، أو 2) الطريق مسار خارجي للخلايا من خلال الفضاء خارج الخلية بين الخلايا المجاورة.[18] يسمى المسارأيضا عبر الخلوي. يمكن أن يتم تخلُّل الخلايا المُحَوَّلة بالمستقبلات ويتكون من ثلاث خطوات: 1) كثرة الخلايا الخلوية بوساطة المستقبل على جانب واحد من الخلية، مثل الجانب اللمعي؛ 2) حركة الجزيء من خلال الحجرة داخل الخلايا عادة داخل نظام الإندوسومال؛ و 3) خلع الجزيء إلى الفضاء خارج الخلية على الجانب الآخر من الخلية، على سبيل المثال الجانب السطحي.
قد يكون عبر الخلايا إما أحادي الاتجاه أو ثنائي الاتجاه. قد يحدث انتحال الخلايا الأحادي الاتجاه بشكل انتقائي في الاتجاه من اللمعة إلى اللمعة، أو في الاتجاه العكسي، في الاتجاه اللامعي إلى اللمعي.
يعد عبر الخلايا بارزًا في الببتيد في الأوعية الدقيقة في الدماغ ونقل البروتين، [19] لأن بطانة الأوعية الدموية الدقيقة في الدماغ، والتي تشكل حاجز الدم في الدماغ (BBB) في الجسم الحي، تعبر عن تقاطعات ضيقة فريدة تشبه الظهارة.[20] تزيل الوصلات الضيقة البطانية في الدماغ المسار الخلوي للانتقال الذائب عبر جدار بطانة الأوعية الدموية الدقيقة في الدماغ. في المقابل، لا يعبر الحاجز البطاني في الأعضاء الطرفية عن تقاطعات ضيقة، والحركة الذائبة عبر المسار الخلوي بارزة في الحاجز البطاني في أعضاء أخرى غير الدماغ أو الحبل الشوكي.[21]
إن تحويل الخلايا المحول بوساطة المستقبل، أو أر ام تي، عبر الحاجز الدموي الدماغي هو مسار محتمل لإيصال الدواء إلى الدماغ، خاصة للعقاقير البيولوجية مثل البروتينات المؤتلفة.[22] يتم دمج الدواء غير القابل للنقل، أو البروتين العلاجي، وراثيًا مع بروتين ناقل. قد يكون بروتين الناقل عبارة عن ببتيد داخلي، أو الأجسام المضادة أحادية النسيلة الببتيدية، التي تخضع لـ أر أم تي عبر الحاجز الدموي الدماغي عن طريق النقل على مستقبلات البطانية في الدماغ مثل مستقبل الأنسولين أو مستقبل الترانسفيرين. يعمل بروتين الناقل كحصان طروادة الجزيئي لنقل الدماغ إلى البروتين العلاجي الذي يتم دمجه وراثيًا لبروتين حصان طروادة الخاص بالمستقبل.
أحصنة طروادة ضد الأجسام المضادة وحيدة النسيلة التي تستهدف أنسولين الحاجز الدموي الدماغي أو مستقبلات الترانسفيرين كانت في تطوير الأدوية لأكثر من 10 سنوات في شركة أرماجين. وهي شركة للتكنولوجيا الحيوية في لوس أنجلوس. قامت أرماجين بتطوير أجسام مضادة معدلة وراثيًا ضد كل من الأنسولين ومستقبلات الترانسفيرين، واندمجت مع هذه الأجسام المضادة بروتينات علاجية مختلفة، بما في ذلك الإنزيمات الليزوزومية، والأجسام المضادة العلاجية، ومستقبلات الطعم، والنباتات العصبية.[23] هذه البروتينات العلاجية وحدها لا تعبر الحاجز الدموي الدماغي، ولكن بعد الاندماج الجيني للجسم المضاد حصان طروادة، يخترق البروتين العلاجي الحاجز الدموي الدماغي بمعدل مماثل للجزيئات الصغيرة. سيكون أرماجين في عام 2015 أول من يدخل التجارب السريرية البشرية مع بروتينات دمج حصان طروادة الحاجزالدموي الدماغي التي تنقل عقاقير البروتين إلى الدماغ عبر مسار تحويل الخلايا. الأمراض البشرية التي تستهدفها أرماجين مبدئيًا هي أمراض تخزين الليزوزومات التي تؤثر سلبًيا على الدماغ. تخلق الأمراض الموروثة حالة حيث لا يتم إنتاج إنزيم ليزوزومي محدد، مما يؤدي إلى حالات خطيرة في الدماغ بما في ذلك التخلف العقلي، والمشاكل السلوكية، ثم الخرف. على الرغم من أن الإنزيم المفقود يمكن تصنيعه من قبل شركات الأدوية، فإن دواء الإنزيم وحده لا يعالج الدماغ، لأن الإنزيم وحده لا يعبر الحاجز الدموي الدماغي. أعاد أرماجين تصميم إنزيم الليزوزوم المفقود كبروتين انصهار حصان طروادة الذي يعبر الحاجز الدموي الدماغي. ستعالج التجارب السريرية الأولى لتقنية بروتين انصهار حصان طروادة الجديد الدماغ في اضطرابات تخزين الجسيمات الليزوزومية، بما في ذلك واحدة من أمراض عديد السكاريد المخاطي من النوع الأول، (MPSIH)، وتسمى أيضًا بمتلازمة هيرلر، و MPS من النوع الثاني، وتسمى أيضًا بمتلازمة هانتر.
اقترح باحثون في جينيتيك إنشاء جسم مضاد ثنائي الخصوصية يمكن أن يربط غشاء الحاجز الدموي الدماغي، ويحفز تحويل الخلايا عن طريق المستقبلات، ويطلق نفسه على الجانب الآخر في الدماغ والجهاز العصبي المركزي. استخدموا جسمًا مضادًا ثنائي الخصوصية للماوس مع موقعين نشطين يؤدون وظائف مختلفة. كان لذراع واحدة موقع ارتباط بمستقبلات مضادة للترانسفيرين منخفض التقارب يحث على تحول الخلايا. قد يؤدي موقع الارتباط عالي التقارب إلى عدم قدرة الجسم المضاد على الانطلاق من غشاء الحاجز الدموي الدماغي بعد عبر الخلايا. بهذه الطريقة، تعتمد كمية الأجسام المضادة المنقولة على تركيز الجسم المضاد على جانبي الحاجز. كان للذراع الآخر موقع ارتباط مضاد لـ BACE1 تم تطويره سابقًا والذي من شأنه أن يمنع وظيفة BACE1 ويمنع تكون اللويحات النشوانية. تمكن جينينتيك من إثبات في نماذج الفأر أن الجسم المضاد ثنائي الخصوصية الجديد كان قادرًا على الوصول إلى المستويات العلاجية في الدماغ.[24] يشار إلى طريقة جينينتيك في إخفاء ونقل الجسم المضاد العلاجي عن طريق ربطه بمحفز تحويل الخلايا بوساطة المستقبل المشار اليه باسم «حصان طروادة».
المراجع
- "cytopempsis"، The Free Dictionary، مؤرشف من الأصل في 17 أبريل 2019.
- Perez, J. H.؛ Branch, W. J.؛ Smith, L.؛ Mullock, B. M.؛ Luzio, J. P. (1988)، "Investigation of endosomal compartments involved in endocytosis and transcytosis of polymeric immunoglobulin a by subcellular fractionation of perfused isolated rat liver"، The Biochemical Journal، 251 (3): 763–770، doi:10.1042/bj2510763، PMID 3415644.
- Fishman, J. B.؛ Rubin, J. B.؛ Handrahan, J. V.؛ Connor, J. R.؛ Fine, R. E. (1987)، "Receptor-mediated transcytosis of transferrin across the blood-brain barrier"، Journal of Neuroscience Research، 18 (2): 299–304، doi:10.1002/jnr.490180206، PMID 3694713.
- Duffy, K. R.؛ Pardridge, W. M. (1987)، "Blood-brain barrier transcytosis of insulin in developing rabbits"، Brain Research، 420 (1): 32–38، doi:10.1016/0006-8993(87)90236-8، PMID 3315116.
- Williams, S. K.؛ Greener, D. A.؛ Solenski, N. J. (1984)، "Endocytosis and exocytosis of protein in capillary endothelium"، Journal of Cellular Physiology، 120 (2): 157–162، doi:10.1002/jcp.1041200208، PMID 6430919.
- Fabian, R. H. (1991)، "Retrograde axonal transport and transcytosis of immunoglobulins: Implications for the pathogenesis of autoimmune motor neuron disease"، Advances in Neurology، 56: 433–444، PMID 1853776.
- Salo, J.؛ Lehenkari, P.؛ Mulari, M.؛ Metsikkö, K.؛ Väänänen, H. K. (1997)، "Removal of osteoclast bone resorption products by transcytosis"، Science، 276 (5310): 270–273، doi:10.1126/science.276.5310.270، PMID 9092479.
- Landsverk, T. (1987)، "The follicle-associated epithelium of the ileal Peyer's patch in ruminants is distinguished by its shedding of 50 nm particles"، Immunology and Cell Biology، 65 (3): 251–261، doi:10.1038/icb.1987.28، PMID 3623609.
- Taub, M. E.؛ Shen, W. C. (1993)، "Regulation of pathways within cultured epithelial cells for the transcytosis of a basal membrane-bound peroxidase-polylysine conjugate"، Journal of Cell Science، 106 (4): 1313–1321، PMID 8126110.
- Hunziker, W.؛ Peters, P. J. (1998)، "Rab17 localizes to recycling endosomes and regulates receptor-mediated transcytosis in epithelial cells"، The Journal of Biological Chemistry، 273 (25): 15734–15741، doi:10.1074/jbc.273.25.15734، PMID 9624171.
- Casanova, J. E.؛ Wang, X.؛ Kumar, R.؛ Bhartur, S. G.؛ Navarre, J.؛ Woodrum, J. E.؛ Altschuler, Y.؛ Ray, G. S.؛ Goldenring, J. R. (1999)، "Association of Rab25 and Rab11a with the Apical Recycling System of Polarized Madin–Darby Canine Kidney Cells"، Molecular Biology of the Cell، 10 (1): 47–61، doi:10.1091/mbc.10.1.47، PMID 9880326.
- Su, T.؛ Bryant, D. M.؛ Luton, F. D. R.؛ Vergés, M.؛ Ulrich, S. M.؛ Hansen, K. C.؛ Datta, A.؛ Eastburn, D. J.؛ Burlingame, A. L. (2010)، "A kinase cascade leading to Rab11-FIP5 controls transcytosis of the polymeric immunoglobulin receptor"، Nature Cell Biology، 12 (12): 1143–1153، doi:10.1038/ncb2118، PMID 21037565.
- Rosato, R.؛ Jammes, H.؛ Belair, L.؛ Puissant, C.؛ Kraehenbuhl, J. P.؛ Djiane, J. (1995)، "Polymeric-Ig receptor gene expression in rabbit mammary gland during pregnancy and lactation: Evolution and hormonal regulation"، Molecular and Cellular Endocrinology، 110 (1–2): 81–87، doi:10.1016/0303-7207(95)03519-d، PMID 7672455.
- Sun, Y.؛ Hu, G.؛ Zhang, X.؛ Minshall, R. D. (2009)، "Phosphorylation of caveolin-1 regulates oxidant-induced pulmonary vascular permeability via paracellular and transcellular pathways"، Circulation Research، 105 (7): 676–685, 15 685 following 685، doi:10.1161/CIRCRESAHA.109.201673، PMID 19713536.
- Giri, C. P.؛ Shima, K.؛ Tall, B. D.؛ Curtis, S.؛ Sathyamoorthy, V.؛ Hanisch, B.؛ Kim, K. S.؛ Kopecko, D. J. (2011)، "Cronobacter spp. (previously Enterobacter sakazakii) invade and translocate across both cultured human intestinal epithelial cells and human brain microvascular endothelial cells"، Microbial Pathogenesis، 52 (2): 140–7، doi:10.1016/j.micpath.2011.10.003، PMID 22023990، مؤرشف من الأصل في 17 مايو 2020.
- Nikitas, G.؛ Deschamps, C.؛ Disson, O.؛ Niault, T.؛ Cossart, P.؛ Lecuit, M. (2011)، "Transcytosis of Listeria monocytogenes across the intestinal barrier upon specific targeting of goblet cell accessible E-cadherin"، Journal of Experimental Medicine، 208 (11): 2263–2277، doi:10.1084/jem.20110560، PMID 21967767.
- Lukyanenko, V.؛ Malyukova, I.؛ Hubbard, A.؛ Delannoy, M.؛ Boedeker, E.؛ Zhu, C.؛ Cebotaru, L.؛ Kovbasnjuk, O. (2011)، "Enterohemorrhagic Escherichia coli infection stimulates Shiga toxin 1 macropinocytosis and transcytosis across intestinal epithelial cells"، AJP: Cell Physiology، 301 (5): C1140–C1149، doi:10.1152/ajpcell.00036.2011، PMID 21832249.
- Simionescu, N.؛ Simionescu, M. (1985)، "Interactions of endogenous lipoproteins with capillary endothelium in spontaneously hyperlipoproteinemic rats"، Microvascular Research، 30 (3): 314–332، doi:10.1016/0026-2862(85)90063-9، PMID 4088094.
- Pardridge, W.M. (1986)، "Receptor-mediated peptide transport through the blood-brain barrier"، Endocrine Reviews، 7 (3): 314–330، doi:10.1210/edrv-7-3-314، PMID 3017689.
- Brightman, M.W.؛ Reese, T.S. (1969)، "Junctions between intimately apposed cell membranes in the vertebrate brain"، Journal of Cell Biology، 40 (3): 648–677، doi:10.1083/jcb.40.3.648، PMID 5765759.
- Bundgaard, M (1984)، "The three-dimensional organization of tight junctions in a capillary endothelium revealed by serial-section electron microscopy"، Journal of Ultrastructure Research، 88 (1): 1–17، doi:10.1016/s0022-5320(84)90177-1، PMID 6545375.
- Pardridge, W.M. (2007)، "Drug targeting to the brain"، Pharmaceutical Research، 24 (9): 1733–1744، doi:10.1007/s11095-007-9324-2، PMID 17554607.
- Pardridge, W.M.؛ Boado, R.J. (2012)، Reengineering biopharmaceuticals for targeted delivery across the blood-brain barrier، Methods in Enzymology، ج. 503، ص. 269–292، doi:10.1016/B978-0-12-396962-0.00011-2، ISBN 9780123969620، PMID 22230573.
- Yu, Y. Joy؛ وآخرون (2001)، "Boosting Brain Uptake of a Therapeutic Antibody by Reducing Its Affinity for a Transcytosis Target"، Science Translational Medicine، 3 (84): 84، doi:10.1126/scitranslmed.3002230، PMID 21613623.
- بوابة علم الأحياء الخلوي والجزيئي