حويصلة (أحياء)
الحويصلة في علم الأحياء الخلوي هي عضية خلوية تتواجد داخل الخلية وخارجها وتتكون من سائل محاط بغشاء لبيدي ثنائي الطبقة. تتشكل الحويصلات طبيعيا أثناء عمليات الإفراز (الإخراج الخلوي) والامتصاص (إدخال خلوي) ونقل المواد داخل الخلية، ويمكن تحضير الحويصلات اصطناعيا وفي تلك الحالة تسمى جسيمات شحمية. إن كان الغشاء مكون من طبقة لبيدية واحدة تسمى حينها حويصلات أجسام شحمية أحادية الصفيحية، وغير ذلك تسمى حويصلات عديدة الصفيحات. الغشاء الذي يحيط بالخلية هو كذلك طور صفيحي، وبشكل مماثل للغشاء البلازمي وغشاء الحويصلات يمكنه الاندماج مع الغشاء البلازمي لتحرير محتوياته خارج الخلية. يمكن للحويصى ت الاندماج مع عضيات أخرى في الخلية.
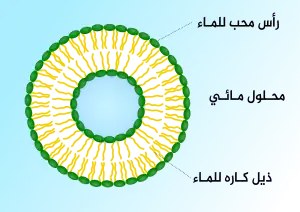
تقوم الحويصلات بوظائف متنوعة، ولأنها مفصولة عن العصارة الخلوية يمكن أن يكون لما بداخلها خصائص مختلفة عن بيئة العصارة الخلوية. لهذا السبب الحويصلات أداة أساسية مستخدمة من قبل الخلية لتنظيم المواد الخلوية. للحويصلات دور في الأيض، النقل، التحكم في الطفو،[1] والتخزين المؤقت للطعام والإنزيمات، كما يمكنها التصرف كغرف لتفاعلات كيميائية.
في سنة 2013 تشارك جيمس روثمان وراندي شيكمان وتوماس سودهوف جائزة نوبل في الطب أو علم وظائف الأعضاء لأدوارهم في توضيح (استنادا على أبحاث سابقة، بعضها من قبل معلميهم) تكوين ووظيفة الحويصلات الخلوية، خاصة لدى الخميرة والبشر، بما في ذلك معلومة على كل جزء من الحويصلة وكيفية تجمُّعها. يُعتقد أن الاختلال الوظيفي للحويصلات يساهم في مرض الألزهايمر، السكري، بعض حالات الصرع صعبة العلاج، بعض السرطانات والاختلالات المناعية وبعض الأمراض العصبية.[2][3]
أنواع الحويصلات
الفجوات
الفجوات هي حويصلات تحتوي في العادة على الماء، تحتوي الخلايا النباتية على فجوة مركزية كبيرة في مركز الخلية وتُستخدم في التنظيم الأسموزي وتخزين المغذيات. تتواجد الفجوات المنقبضة لدى بعض الطلائعيات وبشكل خاص لدى شعبة الهدبيات وتقوم هذه الفجوات بأخد الماء من السيتوبلازم وطرحه خارج الخلية لتجنب الانفجار بسبب الضغط الأسموزي.
اليحلولات
وظيفة اليحلولات هي الهضم الخلوي، يمكن للخلية الحصول على الطعام من الخارج عبر فجوات غذائية بواسطة عملية تسمى الإدخال الخلوي، تندمج هذه الفجوات الغذائية مع اليحلولات التي تقوم بفك محتواها لتتمكن الخلية من استخدامه، ويسمى هذا النوع من الأكل الخلوي بالبلعمة. تُستخدم اليحلولات كذلك في تدمير وتحليل العضيات المختلة أو المتضررة في عملية تسمى الإلتهام الذاتي، حيث تند مج مع غشاء هذه العضيات المتضررة وتبدأ في هضمها وتحليلها.
حويصلات ناقلة
تقوم الحويصلات الناقلة بنقل الجزيئات بين أجزاء مختلفة من الخلية، كمثال: نقل البروتينات من الشبكة الإندوبلازمية إلى جهاز غولجي. تُخلَّق البروتينات المندمجة بالأغشية والمُفرَزة في الريبوسومات المتواجدة في الشبكة الإندوبلازمية الخشنة، تنضج معظم هذه البروتينات في جهاز غولجي قبل أن تمضي إلى وجهتها الأخيرة والتي يمكن أن تكون اليحلولات أو البيروكسية أو خارج الخلية، تنتقل هذه البروتينات في أرجاء الخلية داخل الحويصلات الناقلة.
حويصلات إفرازية
تحتوي الحويصلات الإفرازية على مواد سيتم إفرازها خارج الخلية. للخلية أسباب عديدة لإفراز المواد خارجها، وأحد هذه الأسباب هو التخلص من الفضلات، توجد أسباب أخرى متعلقة بوظيفة الخلية فلدى الكائنات المعقدة تقوم بعض الخلايا المتخصصة بإنتاج جزيئات كيميائية محددة وتخزينها في حويصلات إفرازية ثم طرحا لاحقا عند الحاجة إليها. توجد أنواع عديدة من الحويصلات الإفرازية منها:
- الحويصلات التشابكية وتتواجد في المشبك الكيميائي في العصبونات وتخزن نواقل عصبية. حين تأتي الإشارة عبر المحور العصبي تندمج الحويصلات التشابكية مع الغشاء الخلوي محررة الناقل العصبي لكي تتمكن الجزيئات المستقبلة في الخلية العصبية المجاورة من التعرف عليه.
- تفرز أنسجة الغدد الصماء لدى الحيوانات هرمونات في مجرى الدم، تكون هذه الهرمونات مخزنَة في حويصلات إفرازية، ومن الأمثلة على ذلك نسيج الغدد الصماء الموجود في جزر لانغرهانس في البنكرياس. يحتوي هذا النسيج على أنواع عديدة من الخلايا تُعرَّف حسب الهرمون الذي تنتجه.
- الحويصلات الإفرازية التي تحتوي على الإنزيمات المستخدمة في بناء الجدران الخلوية لخلايا النباتات، الطلائعيات، الفطريات، البكتيريا والعتائق وكذلك النسيج البيني خارج الخلية للخلايا الحيوانية.
- تحرر البكتيريا والعتائق والفطريات والطفيليات حويصلات غشائية تحتوي على مركبات سمية متعددة لكن متخصصة وجزيئات تأشير بيوكيميائية والتي تُنقل إلى الخلايا المستهدفة لبدء عمليات لصالح المروب، والتي تشمل غزو خلايا المضيف وقتل المكروبات المنافسة.[4]
حويصلات خارج خلوية
تُنتج الحويصلات خارج الخلوية لدى جميع النطاقات البيولوجية بما في ذلك حقيقيات النوى المعقدة، البكتيريا سالبة وموجبة الغرام، المتفطرات والفطريات. وهي ذات أنواع مختلفة منها:
- الإكسوزومات وهي حويصلات غشائية أصلها من الإخال الخلوي (قطرها 50-100 نانومتر) وهي غنية بـ CD36 وCD81.[5]
- الحويصلة الميكروية (ويشار إليها كذلك بالحويصلات الميكروية المسكوبة) وهي حويصلات تُسكب مباشرة من الغشاء البلازمي وطولها حوالي (20-1000 نانومتر).[5]
- جسيمات غشائية: (50-80 نانومتر)، أو الحويصلات الغشائية الكبيرة (~600 نانومتر) وهي غنية بـ CD133+ وCD63−[5]
- فقاعة الاستماتة أو الحويصلات الفقاعية (1000-5000 نانومتر)، وتفرزها الخلايا التي تُحتضر.[5][6]
تصنف هذه الحويصلات عادة حسب الكثافة بواسطة الطرد المركزي التبايني.[5] تحصلت الإكتوزومات على اسمها سنة 2008 لكنها لم تعد تعتبر نوعا منفصلا من الحويصلات ابتداء من سنة 2012.[5]
لدى البشر، من المحتمل أن الحويصلات خارج الخلوية داخلية المنشأ تلعب دورا في تجلط الدم، التأشير بين الخلوي وإدارة الفضلات.[5] كما أن لها دورا في العمليات الفسيولوجية المرضية الخاصة بعدة أمراض منها السرطان.[7] حظيت الحويصلات خارج الخلوية باهتمامٍ لكونها مصدرا محتملا للاكتشافات بالوسم الحيوي بسبب دورها في الاتصالات بين الخلوية وبسبب إفرازها في سوائل جسدية الوصول إليها سهل وكذلك لتشابه محتواها الجزيئي مع المحتوى الخاص بالخلايا المفرِزة لها.[8] تتم حاليا دراسة الحويصلات خارج الخلوية الخاصة بالخلايا الجذعية اللحمية المتوسطة وتسمى كذلك مفروز الخلايا الجذعية وتطبيقها لأغراض علاجية لعلاج الأمراض التنكسية وأمراض المناعية الذاتية وأمراض الالتهاب الناتجة عنها.[9]
في البكتيريا سالبة الغرام تُفرز الحويصلات خارج الخلوية بتقرص الغشاء الخارجي، إلا أن كيفية انفلات الحويصلات الخارجية من الأغشية السميكة للبكتيريا موجبة الغرام والمتفطرات والفطريات مازال غير معروف. تحتوي هذه الحويصلات على شحنات متنوعة تشمل أحماضا نووية، ذيفانات وبروتينات ليبيدية وإنزيمات، ولها دور مهم في الفيسيولوجيا والإمراض البكتيري. في تآثرات إمراض المضيف، تُنتج البكتيريا سالبة الغرام حويصلات تلعب أدوارا في إنشاء مستعمرات عشية، حمل ونقل عوامل الضرواة إلى خلايا المضيف وتحوير الاستجابة الدفاعية للمضيف.[10]
وُجد أن البكتيريا الزرقاء المحيطية تحرر باستمرار حويصلات تحتوي على بروتينات، دنا ورنا في المحيط. تنتشر بكثرة حويصلاتٌ حاملةٌ للدنا من بكتيريا متنوعة في عينات المياه البحرية الساحلية ومياه المحيط المفتوح.[11]
أنواع أخرى
تُستخدم الحويصلات الغازية بواسطة العتائق والبكتيريا والعوالق الميكروبية، ربما للتحكم في الهجرة العمودية بتنظيم محتوى الغاز ومنه التحكم في الطفو، أو ربما لجعل الخلية تتموضع بطريقة تحصل فيها على القدر الأقصى من الضوء الشمسي. لهذه الحويصلات في العادة شكل ليموني أو أنابيب أسطوانية مصنوعة من البروتين، [12] تحدد أقطارها قوة الحويصلة مع كون الحويصلات الكبيرة هي الأضعف. يؤثر قطر الحويصلة كذلك في حجمها وفعاليتها في توفير الطفو. في البكتيريا الزرقاء عمل الاصطفاء الطبيعي على إنشاء حويصلات بأطول قطر ممكن مع بقائها مستقرة بنيويا، الغلاف البروتيني نفاذي للغازات لكن ليس للماء، وهذا يحول دون انغمار الحويصلات بالماء.[13]
تتواجد الحويصلات المطرسية في الفضاء بين الخلوي أو المطرس خارج الخلوي. اُكتشفت باستخدام المجهر الإلكتروني سنة 1967 بشكل منفصل سنة من قبل هـ. كلارك أندرسون وإرمانو بونوتشي.[14] هذه الحويصلات المشتقة من الخلايا متخصصة في بدء التمعدن الحيوي للمطرس في أنسجة متنوعة، منها العظم، الغضروف والعاج. أثناء التكلس العادي، يصاحب الإستماتة الخلوية (وهي تدمير ذاتي للخلية) تدفقٌ كبير لأيونات الكالسيوم والفوسفات وتشكلٌ للحويصلات المطرسية. تقود تعبئة الكالسيوم كذلك إلى تشكل الفوسفاتيديل سيرين وهي معقدات كالسيوم فوسفات في الغشاء البلازمي يتوسط تكونها بروتين يسمى أنكسين. تتبرعم الحويصلات المطرسية من الغشاء البلازمي من مواقع تآثره مع النسيج البيني خارج الخلوي، ومنه تنقل الحويصلات المطرسية إلى النسيج البيني كلا من الكالسيوم والفوسفات والليبيدات وبروتينات الأنكسين التي تعمل على تنوي تشكل المعادن. هذه العمليات منسقة بدقة في زمن ومكان مناسبين لتحقيق تمعدن مطرس النسيج، وهذا لا يحدث إن لم يتواجد جهاز غولجي.
الدخلول أو الجسيم متعدد الحويصلات واختصار (MVB) هي حويصلة غشائية تحتوي على العديد من الحويصلات الصغيرة.
التكون والنقل

تتكون بعض الحويصلات حين تتبرعم من غشائي الشبكة الإندوبلازمية وجهاز غولجي. وتتكون حويصلات أخرى حين يحيط الغشاء الخلوي بمواد خارج الخلية.
كساء الحويصلة وجزيئات الشحنة
كساء الحويصلة هو مجموعة من البروتينات التي عملها تحديد انحناء الغشاء المانح، مشكلة حويصلة كروية الشكل. تعمل البروتينات الكسائية كذلك على الارتباط بمختلف المستقبلات البروتينية عبر الغشائية وتسمى مستقبلات الشحنة. تساعد هذه المستقبلات في اختيار المواد التي تدخل الخلية خلال الإدخال الخلوي المتواسط بالمستقبل أو النقل داخل الخلوي.
توجد ثلاث أنواع من أكسية الحويصلات: كلاثرين، COPI وبروتين الغطاء المعقد الثانوي. تساعد بروتينات الكساء المختلفة في تصنيف وتوجيه الحويصلات لوجهاتها الأخيرة. تتواجد أكسية الكلاثرين في الحويصلات التي تعمل في النقل بين جهاز غولجي والغشاء البلازمي، جهاز غولجي والدخلولات، وبين الغشاء البلازمي والدخلولات. الحويصلات المكسوة بـCOPI مسؤولة على النقل الرجوعي من غولجي إلى الشبكة الإندوبلازمية، في حين أن الحويصلات المكسوة بـCOPII مسؤولة على النقل التقدمي من الشبكة إلى غولجي.
يُعتقد أن الكلاثرين يتجمع نتيجة استجابةٍ لـ G بروتين. يتجمع الكساء البروتيني ويتفكك بسبب البروتين عامل ربوزة الـADP (ARF).
رسو الحويصلة
تتعرف البروتينات السطحية المسماة SNARE (سنار) على شحنة الحويصلة وتعمل بروتينات الـسنار المكملة في الغشاء المستهدف على اندماج الحويصلة بالغشاء المستهدف. يُفترض وجود بروتينات السنار الحويصلية (v-SNARES) على غشاء الحويصلة، في حين أن بروتينات السنار المكملة تتواجد على الأغشية المستهدفة وتعرف بـ(t-SNAREs). غالبا ما تصنف بروتينات السنار الحويصلية أو تلك الخاصة بالغشاء المستهدف بـ سنار Qa ،Qb ،Qc أو R نتيجة أنواع أخرى عديدة بدل تلك الخاصة بالحويصلة والغشاء المستهدف. يمكن مشاهدة مصفوفة من معقدات السنار في مختلف الأنسجة والأحياز الخلوية، مع تحديد 36 متغايرة لدى البشر حتى لآن.
يُعتقد أن بروتينات الراب التنظيمية مسؤولة عن تجمع بروتينات السنار. بروتينات الراب هي بروتينات مرتبطة مع الـGTP تنظيمية وتتحكم في في ارتباط بروتينات السنار المكملة هذه لمدة كافية من الوقت ليُحلمِئ بروتين الراب رابطة الـGTP خاصته ويُثبّت الحويصلة بالغشاء.
اندماج الحويصلة
يحدث اندماج الحويصلة بطريقتين: الاندماج الكامل أو الاندماج الجزئي. يتطلب الاندماج أن يكون الغشاءان على مسافة 1.5 نانومتر من بعضهما، وليحدث ذلك يجب إزاحة الماء من سطح غشاء الحويصلة، وهذه العملية مستهلكة للطاقة وتقترح الأدلة أن هذه العملية تتطلب جزيئات ATP وأسيتيل مرافق الإنزيم-أ. للاندماج علاقة كذلك بالتبرعم، ومن ذلك يأتي استخدام المصطلح تبرعم واندماج.
تنظيم بالإنقاص في المستقبل
توسم البروتينات الغشائية التي تعمل كمستقبلات من أجل التنظيم بالإنقاص بإضافة اليوبيكويتين لها. بعد وصولها (البروتينات) إلى الدخلول عبر المسار الموضح بالأعلى، تبدأ الحويصلات بالتشكل داخل الدخلول آخذة معها البروتينات الغشائية التي كانت ستفكك، حين ينضج الدخلول ليصبح يحلولا أو يتحد مع واحد آخر، يتم تفكيك الحويصلات كليا. من دون هذه الآلية، لن يصل إلى لمعة اليحلول سوى الجزء خارج الخلوي من البروتينات الغشائية ويتم تفكيك هذا الجزء فقط.[15]
بسبب هذه الحويصلات يُسمى الدخلول أحيانا جسم متعدد الحويصلات. مسار تكونها غير مفهوم كليا وذلك عكس الحويصلات المذكورة بالأعلى، السطح الخارجي للحويصلات ليس على اتصال بالعصارة الخلوية.
التحضير
إنتاج الحويصلات الغشائية هو أحد طرق البحث في مختلف الأغشية الخلوية. بعد أن يتم سحق النسيج الحيوي إلى مستعلق، تشكل مختلف الأغشية فقاعات صغيرة مغلقة. يمكن التخلص من أجزاء كبير من الخلايا المسحوقة عبر الطرد المركزي بطيء السرعة وبعدها يمكن استخلاص الجزء المرغوب به (غشاء بلازمي، فجوات ...) عبر الطرد المركزي السريع الدقيق في تدرج الكثافة. يمكن باستخدام الصدمة التناضحية فتح الحويصلات مؤقتا (وملئها بالمحلول المطلوب) وبعدها القيام بالطرد المركزي مجددا ثم إعادة العملية في محاليل مختلفة. تطبيق حاملات الأيون مثل الفالينومايسين يمكن أن يُنشئ تدرجات كهروكيميائية مشابهة للتدرجات داخل الخلايا الحية. تُستخدم الحويصلات عادة في نوعين من البحوث:
- لإيجاد واستخلاص المستقبلات الغشائية التي ترتبط خصيصا بالهرمونات وعدة جزيئات مهمة أخرى.[16]
- لبحث وتقصي نقل مختلف الأيونات أو المواد الأخرى عبر نوع معين من الأغشية.[17] في حين أن تقصي النقل يكون أكثر سهولة مع تقنيات الالتقاط الرقعي، يمكن عزل الحويصلات كذلك من مواد لا يمكن تطبيق الالتقاط الرقعي عليها.
حويصلات اصطناعية
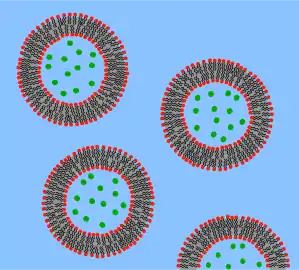
تمت دراسة الحويصلات الفوسفوليبيدية كذلك في الكيمياء الحيوية، من أجل تلك الدراسات يمكن تحضير مستعلق حويصلات فوسفولبيدية عبر تقنيتي البثق أو الصواتة،[18] أو بحقن محلول فوسفولبيدي إلى المحلول المنظم المائي الغشائي.[19] يمكن بهذه الطريقة تحضير محاليل حويصلات مائية ذات مكونات فوسفولبيدية مختلفة، وكذلك ذات حويصلات بأحجام مختلفة.
اقرأ أيضا
المراجع
- Walsby AE (1994)، "Gas vesicles"، Microbiological Reviews، 58 (1): 94–144، PMC 372955، PMID 8177173.
- "Nobel medical prize goes to 2 Americans, 1 German"، CNN، 19 أكتوبر 2005، مؤرشف من الأصل في 07 نوفمبر 2017، اطلع عليه بتاريخ 09 أكتوبر 2013.
- 2013 Nobel Prize in Physiology or Medicine, press release 2013-10-07 نسخة محفوظة 09 أغسطس 2018 على موقع واي باك مشين.
- Deatherage, B. L.؛ Cookson, B. T. (2012)، "Membrane Vesicle Release in Bacteria, Eukaryotes, and Archaea: a Conserved yet Underappreciated Aspect of Microbial Life"، Infection and Immunity، 80 (6): 1948–1957، doi:10.1128/IAI.06014-11، ISSN 0019-9567، PMC 3370574، PMID 22409932.
- van der Pol, Edwin؛ Böing, Anita N.؛ Harrison, Paul؛ Sturk, Augueste؛ Nieuwland, Rienk (01 يوليو 2012)، "Classification, functions, and clinical relevance of extracellular vesicles"، Pharmacological Reviews، 64 (3): 676–705، doi:10.1124/pr.112.005983، ISSN 1521-0081، PMID 22722893. Free full text
- van der Pol, E.؛ Böing, A. N.؛ Gool, E. L.؛ Nieuwland, R. (01 يناير 2016)، "Recent developments in the nomenclature, presence, isolation, detection and clinical impact of extracellular vesicles"، Journal of Thrombosis and Haemostasis (باللغة الإنجليزية)، 14 (1): 48–56، doi:10.1111/jth.13190، PMID 26564379.
- Dhondt, Bert؛ Rousseau, Quentin؛ De Wever, Olivier؛ Hendrix, An (11 يونيو 2016)، "Function of extracellular vesicle-associated miRNAs in metastasis"، Cell and Tissue Research، 365 (3): 621–641، doi:10.1007/s00441-016-2430-x، hdl:1854/LU-7250365، PMID 27289232.
- Dhondt, Bert؛ Van Deun, Jan؛ Vermaerke, Silke؛ de Marco, Ario؛ Lumen, Nicolaas؛ De Wever, Olivier؛ Hendrix, An (يونيو 2018)، "Urinary extracellular vesicle biomarkers in urological cancers: From discovery towards clinical implementation"، The International Journal of Biochemistry & Cell Biology، 99: 236–256، doi:10.1016/j.biocel.2018.04.009، hdl:1854/LU-8559155، PMID 29654900.
- Teixeira, Fábio G.؛ Carvalho, Miguel M.؛ Sousa, Nuno؛ Salgado, António J. (01 أكتوبر 2013)، "Mesenchymal stem cells secretome: a new paradigm for central nervous system regeneration?"، Cellular and Molecular Life Sciences (باللغة الإنجليزية)، 70 (20): 3871–3882، doi:10.1007/s00018-013-1290-8، ISSN 1420-682X، PMID 23456256.
- Kuehn, Meta J.؛ Kesty, Nicole C. (15 نوفمبر 2005)، "Bacterial outer membrane vesicles and the host-pathogen interaction"، Genes & Development، 19 (22): 2645–2655، doi:10.1101/gad.1299905، ISSN 0890-9369، PMID 16291643.
- Biller, Steven J.؛ Schubotz, Florence؛ Roggensack, Sara E؛ Thompson, Anne W.؛ Summons, Roger E.؛ Chisholm, Sallie W. (10 يناير 2014)، "Bacterial Vesicles in Marine Ecosystems"، Science (باللغة الإنجليزية)، 343 (6167): 183–186، doi:10.1126/science.1243457، ISSN 0036-8075، PMID 24408433.
- Pfeifer F (2012)، "Distribution, formation and regulation of gas vesicles"، Nature Reviews. Microbiology، 10 (10): 705–15، doi:10.1038/nrmicro2834، PMID 22941504.
- Walsby, Anthony (مارس 1994)، "Gas Vesicles"، Microbiological Reviews، 58: 94–144، PMC 372955، PMID 8177173.
- Bonucci E (1967)، "Fine structure of early cartilage calcification"، J. Ultrastruct. Res.، 20 (1): 33–50، doi:10.1016/S0022-5320(67)80034-0، PMID 4195919.
- Katzmann DJ, Odorizzi G, Emr SD (2002)، "Receptor downregulation and multivesicular-body sorting" (PDF)، Nat. Rev. Mol. Cell Biol.، 3 (12): 893–905، doi:10.1038/nrm973، PMID 12461556، مؤرشف من الأصل (PDF) في 29 نوفمبر 2007.
- Sidhu VK, Vorhölter FJ, Niehaus K, Watt SA (2008)، "Analysis of outer membrane vesicle associated proteins isolated from the plant pathogenic bacterium Xanthomonas campestris pv. campestris"، BMC Microbiol.، 8: 87، doi:10.1186/1471-2180-8-87، PMC 2438364، PMID 18518965.
- Scherer GG, Martiny-Baron G (1985)، "K+/H+ exchange transport in plantmembranevesicles is evidence for K+ transport"، Plant Science، 41 (3): 161–8، doi:10.1016/0168-9452(85)90083-4، مؤرشف من الأصل في 25 مارس 2019.
- Barenholz, Y.؛ Gibbes, D.؛ Litman, B. J.؛ Goll, J.؛ Thompson, T. E.؛ Carlson, F. D. (1977)، "A simple method for the preparation of homogeneous phospholipid vesicles"، Biochemistry، 16 (12): 2806–10، doi:10.1021/bi00631a035، PMID 889789.
- Batzri S, Korn ED (أبريل 1973)، "Single bilayer liposomes prepared without sonication"، Biochim. Biophys. Acta، 298 (4): 1015–9، doi:10.1016/0005-2736(73)90408-2، PMID 4738145، مؤرشف من الأصل في 25 مارس 2019.
- بوابة علم الأحياء الخلوي والجزيئي